Zobrazení: 0 Autor: Editor webu Čas publikování: 23. 1. 2025 Původ: místo








Cirhóza představuje konečnou fázi chronického poškození jater způsobené různými stavy, včetně autoimunitních onemocnění, hepatitidy a nadměrné konzumace alkoholu. Játra, jako regenerační orgán, se po každém zranění snaží samy uzdravit. Opakované poškození však vede k hromadění zjizvené tkáně, což zhoršuje její schopnost vykonávat základní funkce, jako je detoxikace krve, syntetizace bílkovin a regulace metabolismu. Postupem času se játra postupně stávají méně výkonnými, což vede ke komplikacím, které mohou ohrozit život člověka.
Autoimunitní onemocnění jater, jako je autoimunitní hepatitida (AIH), primární biliární cholangitida (PBC) a primární sklerotizující cholangitida (PSC), jsou hlavními příčinami cirhóza . Tyto stavy vznikají, když imunitní systém omylem napadne játra, což způsobí chronický zánět a progresivní jizvy.
Autoimunitní cirhóza je oblastí rostoucího zájmu kvůli jejímu potenciálu zůstat nediagnostikovaná až do dosažení pokročilého stadia. Aby vědci lépe porozuměli jeho patofyziologii a vyvinuli účinné terapie, spoléhají se silně na modely malých zvířat, které replikují lidské autoimunitní reakce.
Malá zvířata, jako jsou myši a krysy, jsou široce používána v biomedicínském výzkumu kvůli jejich genetické podobnosti s lidmi, snadné manipulaci a rychlé reprodukci. Nabízejí účinný a eticky zvládnutelný model pro studium komplexních onemocnění, jako je cirhóza. Zde je důvod, proč jsou nepostradatelné:
Genetické inženýrství: Pokroky v genetické modifikaci umožňují výzkumníkům vytvářet zvířata se specifickými imunitními vlastnostmi podobnými těm, které se vyskytují u lidských autoimunitních stavů.
Efektivita nákladů: Malá zvířata jsou cenově dostupnější na údržbu ve srovnání s většími druhy, což umožňuje rozsáhlé experimenty.
Reprodukovatelnost: Nabízejí konzistentní výsledky za kontrolovaných experimentálních podmínek a zajišťují spolehlivá data.
1. Geneticky upravené modely
Knockout a transgenní myši: Tyto myši jsou navrženy tak, aby postrádaly určité geny nebo nadměrně exprimovaly jiné, což pomáhá výzkumníkům pochopit, jak specifické geny ovlivňují autoimunitní reakce a progresi cirhózy.
Humanizované myši: Myši zkonstruované tak, aby nesly složky lidského imunitního systému a poskytovaly informace o tom, jak se u lidí vyvíjejí autoimunitní onemocnění.
2. Chemicky indukované modely
Chemikálie jako chlorid uhličitý (CCl₄) nebo thioacetamid (TAA) se používají k vyvolání poškození jater u hlodavců, což napodobuje chronické poškození pozorované u autoimunitních onemocnění.
3.Spontánní modely
U některých kmenů myší se přirozeně vyvíjejí autoimunitní stavy, takže jsou ideální pro studium progrese onemocnění a potenciálních zásahů bez vnější manipulace.
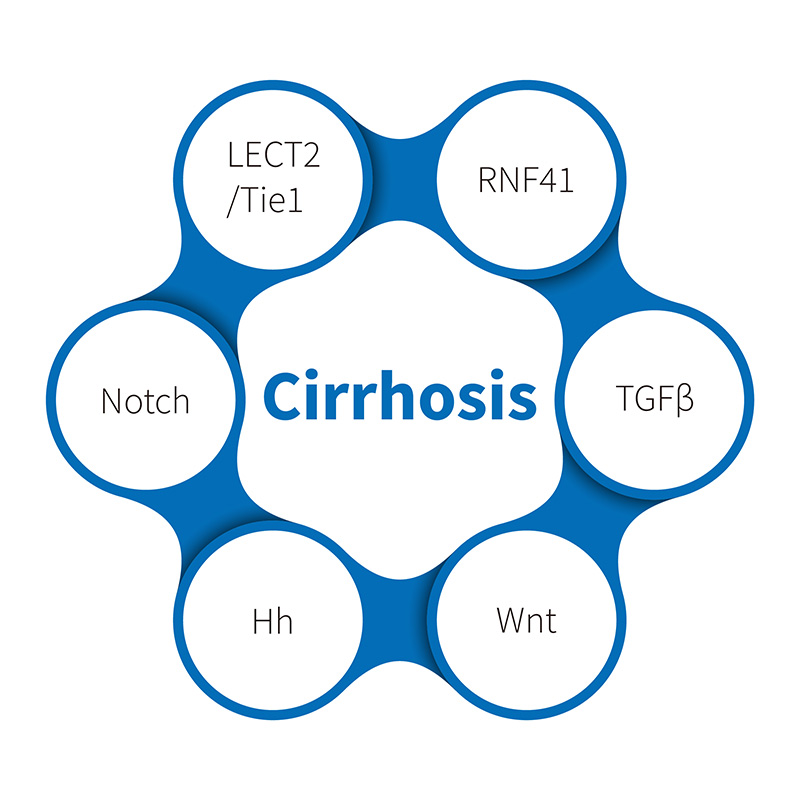
1. Porozumění dysfunkci imunitního systému
Autoimunitní cirhóza zahrnuje komplexní souhru imunitních buněk, cytokinů a genetických faktorů. Studie na malých zvířatech odhalily:
· Role T-helper buněk (Th17) při podpoře zánětu.
· Příspěvek regulačních T lymfocytů (Tregs) k potlačení škodlivých imunitních reakcí, zdůraznění potenciálních terapeutických cílů.
· Účast cytokinů jako IL-1β, TNF-α a IFN-γ na poškození jater.
2. Vývoj biomarkerů
Pro zvládnutí autoimunitní cirhózy je zásadní včasná diagnostika. Výzkum využívající modely malých zvířat vedl k objevu biomarkerů, jako jsou:
· Zvýšené transaminázy (ALT a AST).
· Autoprotilátky, jako jsou mikrozomální protilátky proti játrům/ledvinám (LKM) a protilátky proti hladkému svalstvu (SMA).
3. Testování a vývoj léčiv
Malá zvířata byla široce používána k hodnocení léčby autoimunitních onemocnění jater, jako jsou:
· Imunomodulátory: Léky jako azathioprin a mykofenolát mofetil byly testovány za účelem posouzení jejich schopnosti potlačit imunitně zprostředkované poškození jater.
· Biologické terapie: Monoklonální protilátky zaměřené na prozánětlivé cytokiny se v preklinických studiích ukázaly jako slibné.
· Vznikající terapie: Na zvířecích modelech se zkoumají techniky úpravy genů, jako je CRISPR-Cas9 a léčba založená na RNA.
4. Studie interakce střeva a jater
Střevní mikrobiom hraje klíčovou roli při onemocněních jater. Modely na malých zvířatech ukázaly, jak změny střevních bakterií ovlivňují imunitní aktivaci a zánět jater. Probiotika, prebiotika a dietní intervence jsou testovány jako doplňkové terapie.
HKeybio, přední smluvní výzkumná organizace (CRO) , se specializuje na preklinické studie autoimunitních onemocnění. Jejich zařízení na testování malých zvířat a detekce v průmyslovém parku Suzhou a testovací základna na nelidské primáty v Guangxi podtrhují jejich odhodlání provádět špičkový výzkum.
2. Nejmodernější zařízení: Jejich pokročilé vybavení podporuje sofistikované preklinické studie, včetně zobrazování, analýzy biomarkerů a molekulárního testování.
3. Komplexní modely: HKeybio využitím malých zvířat i subhumánních primátů umožňuje komplexní pochopení autoimunitních onemocnění a usnadňuje translační výzkum.
Prostřednictvím těchto schopností hraje HKeybio klíčovou roli v pokroku v oblasti výzkumu autoimunitní cirhózy.
Jaké jsou nejběžnější zvířecí modely používané při výzkumu cirhózy?
Nejčastěji používanými modely jsou myši a krysy. Mohou být geneticky modifikované, chemicky indukované nebo přirozeně náchylné k autoimunitním onemocněním.
Jak střevní mikrobiom ovlivňuje autoimunitní cirhózu?
Výzkum ukazuje, že střevní bakterie hrají klíčovou roli v regulaci imunitního systému. Dysbióza (nerovnováha střevních bakterií) může zhoršit zánět jater a zjizvení.
Jaká je role HKeybio v autoimunitním výzkumu?
HKeybio je CRO, která se specializuje na preklinické studie autoimunitních onemocnění, využívající modely malých zvířat a primátů k podpoře inovací v diagnostice a léčbě.
Použití malých zvířecích modelů ve výzkumu autoimunitní cirhózy způsobilo revoluci v našem chápání této nemoci. Od identifikace dysfunkcí imunitního systému až po testování průkopnických terapií zůstávají malá zvířata neocenitelným nástrojem v boji proti cirhóze. Organizace, jako je HKeybio, jsou v čele s využitím pokročilých technologií a odborných znalostí k posunutí hranic preklinického výzkumu.
Jak pokračujeme v odhalování mechanismů stojících za autoimunitními onemocněními a jejich progresí do cirhózy , role malých zvířecích modelů zůstane ústřední. Překlenutím propasti mezi základním výzkumem a klinickými aplikacemi tyto modely dláždí cestu pro inovativní léčbu, která by mohla výrazně zlepšit životy pacientů po celém světě.
