| Disponibilité : | |
|---|---|
| Quantité : | |











Cliniquement pertinent – Imite la douleur postopératoire humaine avec blessure par incision, allodynie mécanique et réponse inflammatoire.
Critères de jugement quantifiables – Seuil de retrait mécanique (filaments de von Frey), score de douleur spontanée, asymétrie de mise en charge, en option : sensibilité thermique.
Hautement reproductible – Un protocole chirurgical standardisé garantit un comportement cohérent de la douleur d’une expérience à l’autre.
Valeur translationnelle – Idéal pour tester les analgésiques non opioïdes, les AINS, les anesthésiques locaux et les nouvelles stratégies de gestion de la douleur.
Ensembles de données prêts pour l'IND – Les études peuvent être menées conformément aux principes BPL.
Modèle PSP induit par incision chirurgicale en C57BL/6
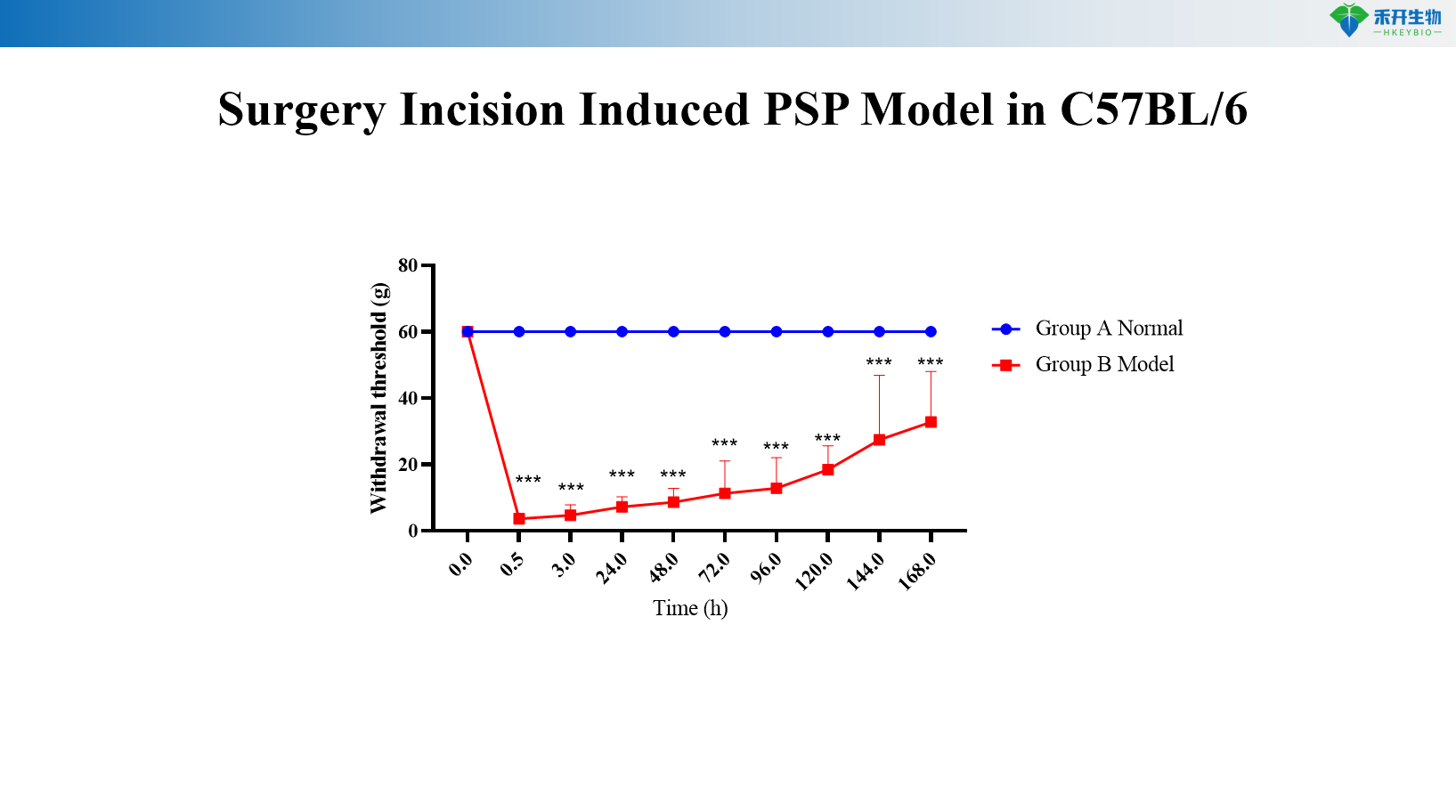
• Tests d'efficacité des analgésiques non opioïdes (AINS, inhibiteurs de la COX-2, acétaminophène)
• Évaluation de nouveaux analgésiques, notamment les inhibiteurs des canaux sodiques, les antagonistes du TRPV1 et les antagonistes des récepteurs de la neurokinine.
• Validation des cibles pour les voies de sensibilisation périphériques et centrales
• Découverte de biomarqueurs (médiateurs inflammatoires, neuropeptides liés à la douleur)
• Études pharmacologiques et toxicologiques permettant l'IND
Paramètre |
Spécification |
Espèce/souche |
Souris C57BL/6 |
Méthode d'induction |
Incision plantaire (incision longitudinale de 1 cm à travers la peau, le fascia et le muscle de la patte postérieure) sous anesthésie à l'isoflurane |
Durée des études |
1 à 14 jours (phase de douleur aiguë) |
Points de terminaison clés |
Seuil de retrait mécanique (filaments de von Frey), score de douleur spontanée (garde, léchage, levage), asymétrie de mise en charge (incapamètre), en option : hyperalgésie thermique (Hargreaves), analyse de la marche, taux de cytokines inflammatoires (ELISA/qPCR) |
| Contrôle positif | AINS (par exemple, ibuprofène, kétorolac) ou gabapentine disponibles comme composés de référence |
Paquet de données |
Données brutes, rapports d'analyses, données comportementales, bioinformatique (facultatif) |
Q : Comment l’incision chirurgicale induit-elle une douleur postopératoire chez la souris ?
R : L'incision perturbe la peau, les fascias et les tissus musculaires, déclenchant une inflammation aiguë, une sensibilisation périphérique et des altérations du système nerveux central. Il en résulte une allodynie mécanique et des comportements douloureux spontanés qui culminent en quelques heures et persistent pendant des jours, imitant fidèlement la douleur postopératoire humaine.
Q : Quelles sont les principales similitudes avec la douleur postopératoire humaine ?
R : Le modèle présente une allodynie mécanique (douleur provoquée par des stimuli normalement non douloureux), un comportement de garde spontané et une réponse inflammatoire au site de l'incision, qui sont tous des caractéristiques de la douleur postopératoire humaine.
Q : Ce modèle peut-il être utilisé pour des études permettant l’IND ?
R : Oui. Les études peuvent être menées conformément aux principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différentes tailles d'incision, traitement préventif ou postopératoire) ?
R : Absolument. Notre équipe scientifique adapte les protocoles d'incision, les programmes de traitement (préventifs, postopératoires) et les analyses des paramètres à votre candidat-médicament spécifique.
Q : Quel est le calendrier typique d’une étude pilote d’efficacité ?
R : Les études sur la douleur aiguë sont généralement réalisées dans les 7 jours suivant l'incision, avec des tests comportementaux au départ, après l'intervention chirurgicale et à plusieurs moments (par exemple, 2 h, 6 h, 24 h, 48 h, 72 h, 7 jours).
