| Disponibilité : | |
|---|---|
| Quantité : | |











Cliniquement pertinent – Récapitule le KOA humain : dégénérescence du cartilage, gonflement des articulations et comportements liés à la douleur.
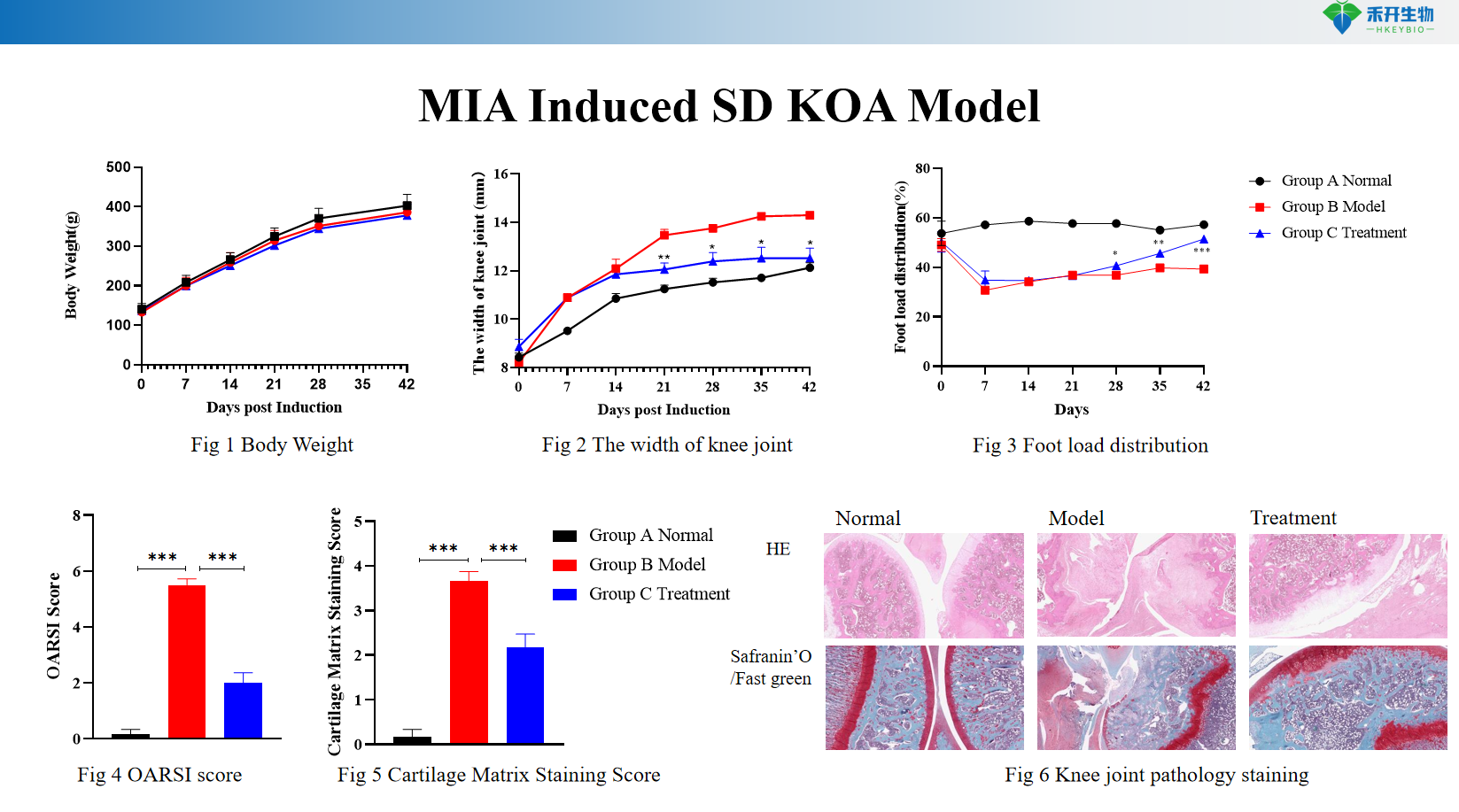
Critères d'évaluation quantifiables : poids corporel, largeur de l'articulation du genou (mesure au pied à coulisse), répartition de la charge du pied (asymétrie de mise en charge), score de coloration de la matrice cartilagineuse (Safranin O/Fast green), histopathologie (HE, bleu de toluidine).
Axé sur un mécanisme – MIA inhibe la glycolyse des chondrocytes, induisant l’apoptose et la dégradation progressive du cartilage, imitant les changements métaboliques et structurels de l’arthrose.
Valeur translationnelle – Idéal pour tester les médicaments modificateurs de la maladie contre l’arthrose (DMOAD), les analgésiques (AINS, opioïdes) et les agents anti-inflammatoires.
Ensembles de données prêts pour l'IND – Les études peuvent être menées conformément aux principes BPL.
Modèle SD KOA induit par MIA
• Tests d'efficacité des médicaments modificateurs de la maladie contre l'arthrose (DMOAD), notamment les inhibiteurs de la cathepsine K, les modulateurs de la voie Wnt et les agents anabolisants.
• Évaluation des analgésiques (AINS, inhibiteurs de la COX-2, opioïdes, cannabinoïdes) dans les douleurs arthrosiques
• Validation des cibles pour la dégradation du cartilage et les voies de la douleur
• Découverte de biomarqueurs (marqueurs de dégradation du cartilage, médiateurs inflammatoires)
• Études pharmacologiques et toxicologiques permettant l'IND
Paramètre |
Spécification |
Espèce/souche |
Rat Sprague-Dawley (SD) |
Méthode d'induction |
Injection intra-articulaire de monoiodoacétate (MIA, 1 à 3 mg dans 50 μL de solution saline) dans l'articulation du genou |
Durée des études |
1 à 8 semaines (phases aiguës à chroniques) |
Points de terminaison clés |
Poids corporel, largeur de l'articulation du genou (étrier), répartition de la charge du pied (asymétrie de mise en charge), score de coloration de la matrice cartilagineuse (Safranin O/Fast green), histopathologie (HE, bleu de toluidine, score OARSI), en option : allodynie mécanique (von Frey), analyse de la marche, biomarqueurs sériques (COMP, CTX-II) |
| Contrôle positif | AINS (par exemple, indométacine) ou DMOAD disponibles comme composés de référence |
Paquet de données |
Données brutes, rapports d'analyse, lames histologiques, données comportementales, bioinformatique (facultatif) |
Q : Comment le MIA induit-il l’arthrose ?
R : Le monoiodoacétate (MIA) inhibe la glycéraldéhyde-3-phosphate déshydrogénase, une enzyme clé de la glycolyse, entraînant une perturbation métabolique et l'apoptose des chondrocytes. Cela déclenche une dégradation progressive du cartilage, des modifications des os sous-chondraux et des comportements douloureux qui imitent étroitement l’arthrose humaine.
Q : Quelles sont les principales similitudes avec l’arthrose du genou chez l’humain ?
R : Le modèle présente une perte de matrice cartilagineuse, un gonflement des articulations, une altération de la mise en charge et des changements histopathologiques (fibrillation, perte de chondrocytes, sclérose osseuse sous-chondrale), reflétant étroitement la pathologie humaine du KOA et les déficits fonctionnels liés à la douleur.
Q : Ce modèle peut-il être utilisé pour des études permettant l’IND ?
R : Oui. Les études peuvent être menées conformément aux principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différentes doses de MIA, dosage prophylactique ou thérapeutique) ?
R : Absolument. Notre équipe scientifique adapte les doses de MIA, les programmes de traitement et les analyses des paramètres à votre candidat-médicament spécifique.
Q : Quel est le calendrier typique d’une étude pilote d’efficacité ?
R : Les études sur la douleur aiguë peuvent être réalisées en 1 à 2 semaines ; les études structurelles chroniques nécessitent généralement 4 à 8 semaines après l'injection de MIA.
