| Disponibilità: | |
|---|---|
| Quantità: | |











Clinicamente rilevante – Imita il dolore postoperatorio umano con lesioni incisionali, allodinia meccanica e risposta infiammatoria.
Endpoint quantificabili – Soglia di ritiro meccanica (filamenti di von Frey), punteggio del dolore spontaneo, asimmetria del carico, opzionale: sensibilità termica.
Altamente riproducibile – Il protocollo chirurgico standardizzato garantisce un comportamento del dolore coerente in tutti gli esperimenti.
Valore traslazionale – Ideale per testare analgesici non oppioidi, FANS, anestetici locali e nuove strategie di gestione del dolore.
Pacchetti dati pronti per IND – Gli studi possono essere condotti in conformità con i principi GLP.
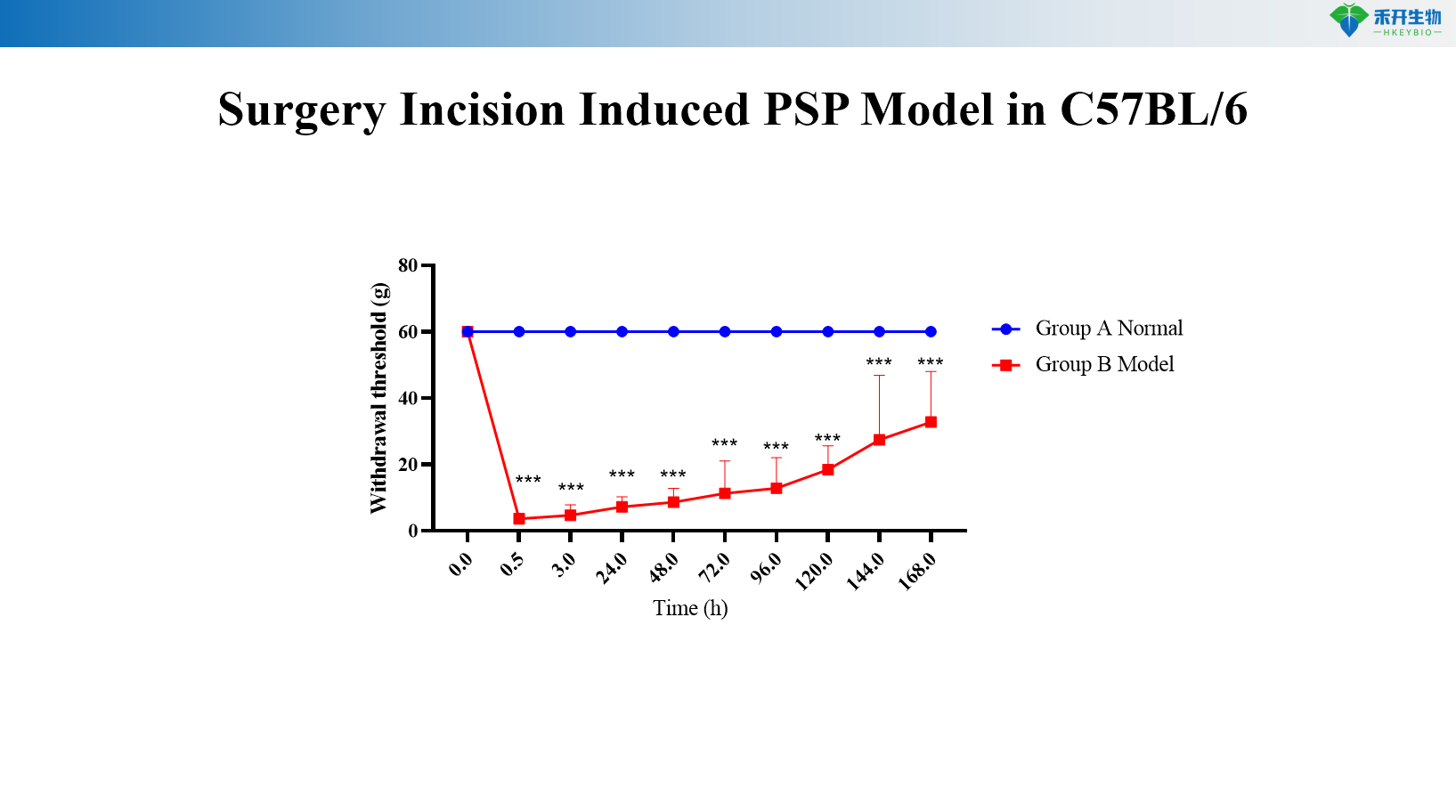
Modello PSP indotto da incisione chirurgica in C57BL/6
• Test di efficacia degli analgesici non oppioidi (FANS, inibitori della COX-2, paracetamolo)
• Valutazione di nuovi analgesici tra cui bloccanti dei canali del sodio, antagonisti del TRPV1 e antagonisti dei recettori della neurochinina
• Convalida degli obiettivi per i percorsi di sensibilizzazione periferici e centrali
• Scoperta di biomarcatori (mediatori dell'infiammazione, neuropeptidi legati al dolore)
• Studi farmacologici e tossicologici che consentono l'IND
Parametro |
Specifica |
Specie/ceppo |
Mouse C57BL/6 |
Metodo di induzione |
Incisione plantare (incisione longitudinale di 1 cm attraverso la pelle, la fascia e il muscolo della zampa posteriore) in anestesia con isoflurano |
Durata dello studio |
1–14 giorni (fase del dolore acuto) |
Endpoint chiave |
Soglia di ritiro meccanica (filamenti di von Frey), punteggio del dolore spontaneo (protezione, leccata, sollevamento), asimmetria del carico (misuratore di incapacità), opzionale: iperalgesia termica (Hargreaves), analisi dell'andatura, livelli di citochine infiammatorie (ELISA/qPCR) |
| Controllo positivo | FANS (ad esempio ibuprofene, ketorolac) o gabapentin disponibili come composti di riferimento |
Pacchetto dati |
Dati grezzi, rapporti di analisi, dati comportamentali, bioinformatica (facoltativo) |
D: In che modo l'incisione chirurgica induce dolore postoperatorio nei topi?
R: L'incisione distrugge la pelle, la fascia e i tessuti muscolari, innescando infiammazione acuta, sensibilizzazione periferica e alterazioni del sistema nervoso centrale. Ciò si traduce in allodinia meccanica e comportamenti dolorosi spontanei che raggiungono il picco entro poche ore e persistono per giorni, imitando da vicino il dolore postoperatorio umano.
D: Quali sono le principali somiglianze con il dolore postoperatorio umano?
R: Il modello mostra allodinia meccanica (dolore derivante da stimoli normalmente non dolorosi), comportamento di guardia spontaneo e risposta infiammatoria nel sito dell'incisione, che sono tutti segni distintivi del dolore postoperatorio umano.
D: Questo modello può essere utilizzato per studi abilitanti all’IND?
R: Sì. Gli studi possono essere condotti in conformità con i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diverse dimensioni di incisione, trattamento preventivo o postoperatorio)?
R: Assolutamente. Il nostro team scientifico personalizza i protocolli di incisione, i programmi di trattamento (preventivi, post-operatori) e le analisi degli endpoint in base al vostro specifico farmaco candidato.
D: Qual è la tempistica tipica per uno studio pilota sull'efficacia?
R: Gli studi sul dolore acuto vengono generalmente completati entro 7 giorni dopo l'incisione, con test comportamentali al basale, dopo l'intervento chirurgico e in più punti temporali (ad esempio, 2 ore, 6 ore, 24 ore, 48 ore, 72 ore, 7 giorni).
