| Disponibilità: | |
|---|---|
| Quantità: | |











Clinicamente rilevante – Riepiloga la KOA umana: degenerazione della cartilagine, gonfiore articolare e comportamenti legati al dolore.
Endpoint quantificabili : peso corporeo, larghezza dell'articolazione del ginocchio (misurazione del calibro), distribuzione del carico del piede (asimmetria del carico), punteggio della colorazione della matrice cartilaginea (Safranin O/Fast green), istopatologia (HE, blu di toluidina).
Guidato dal meccanismo – MIA inibisce la glicolisi dei condrociti, inducendo l’apoptosi e la progressiva degradazione della cartilagine, imitando i cambiamenti metabolici e strutturali nell’osteoartrosi.
Valore traslazionale – Ideale per testare farmaci per l'osteoartrite modificanti la malattia (DMOAD), analgesici (FANS, oppioidi) e agenti antinfiammatori.
Pacchetti dati pronti per IND – Gli studi possono essere condotti in conformità con i principi GLP.
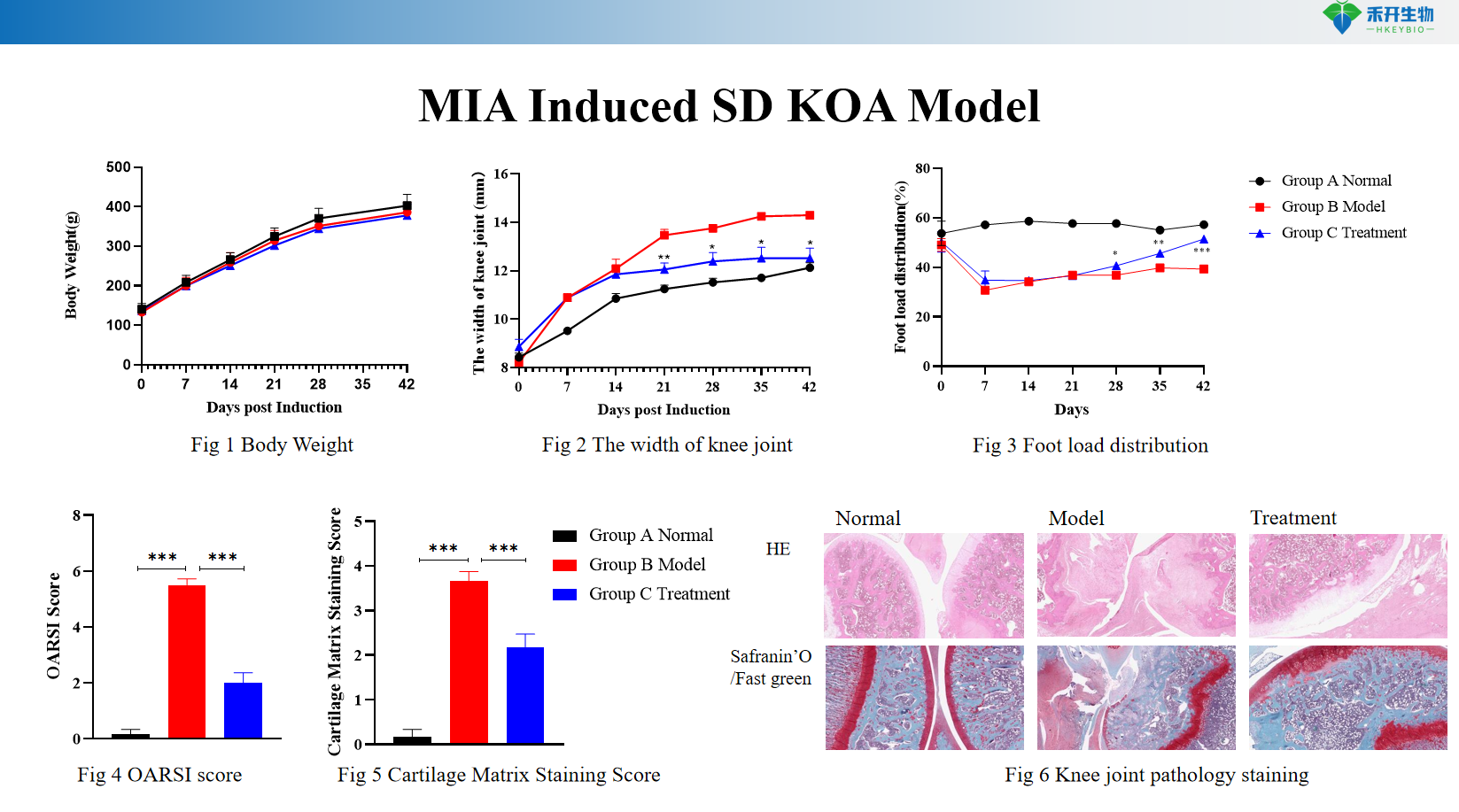
Modello SD KOA indotto da MIA
• Test di efficacia di farmaci per l'osteoartrite modificanti la malattia (DMOAD), inclusi gli inibitori della catepsina K, i modulatori della via Wnt e gli agenti anabolizzanti
• Valutazione degli analgesici (FANS, inibitori della COX-2, oppioidi, cannabinoidi) per il dolore da osteoartrosi
• Convalida degli obiettivi per la degradazione della cartilagine e le vie del dolore
• Scoperta di biomarcatori (marcatori di degradazione della cartilagine, mediatori dell'infiammazione)
• Studi farmacologici e tossicologici che consentono l'IND
Parametro |
Specifica |
Specie/ceppo |
Ratto Sprague-Dawley (SD). |
Metodo di induzione |
Iniezione intrarticolare di monoiodoacetato (MIA, 1–3 mg in 50 μL di soluzione salina) nell'articolazione del ginocchio |
Durata dello studio |
1–8 settimane (fasi da acute a croniche) |
Endpoint chiave |
Peso corporeo, larghezza dell'articolazione del ginocchio (calibro), distribuzione del carico del piede (asimmetria del carico), punteggio di colorazione della matrice cartilaginea (Safranin O/Fast green), istopatologia (HE, blu di toluidina, punteggio OARSI), opzionale: allodinia meccanica (von Frey), analisi dell'andatura, biomarcatori sierici (COMP, CTX-II) |
| Controllo positivo | FANS (ad esempio, indometacina) o DMOAD disponibili come composti di riferimento |
Pacchetto dati |
Dati grezzi, rapporti di analisi, vetrini istologici, dati comportamentali, bioinformatica (facoltativo) |
D: In che modo la MIA induce l'osteoartrosi?
R: Il monoiodoacetato (MIA) inibisce la gliceraldeide-3-fosfato deidrogenasi, un enzima chiave nella glicolisi, portando alla distruzione metabolica dei condrociti e all'apoptosi. Ciò innesca la progressiva degradazione della cartilagine, cambiamenti dell’osso subcondrale e comportamenti dolorosi che imitano da vicino l’osteoartrosi umana.
D: Quali sono le principali somiglianze con l'artrosi del ginocchio umano?
R: Il modello mostra perdita di matrice cartilaginea, gonfiore articolare, carico alterato e cambiamenti istopatologici (fibrillazione, perdita di condrociti, sclerosi ossea subcondrale), rispecchiando da vicino la patologia umana KOA e i deficit funzionali legati al dolore.
D: Questo modello può essere utilizzato per studi abilitanti all’IND?
R: Sì. Gli studi possono essere condotti in conformità con i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diverse dosi di MIA, dosaggio profilattico o terapeutico)?
R: Assolutamente. Il nostro team scientifico adatta le dosi MIA, i programmi di trattamento e le analisi degli endpoint al tuo specifico farmaco candidato.
D: Qual è la tempistica tipica per uno studio pilota sull'efficacia?
R: Gli studi sul dolore acuto possono essere completati in 1-2 settimane; gli studi strutturali cronici richiedono in genere 4-8 settimane dopo l'iniezione MIA.
