| Disponibilità: | |
|---|---|
| Quantità: | |











Ampia copertura della malattia : disponibili modelli Xenogenici (PBMC umani), GVHD simil-lupus acuto e cronico non corrispondenti MHC non corrispondenti.
Endpoint quantificabili : peso corporeo, tasso di sopravvivenza, punteggio clinico GVHD (scala 0-10 con postura, attività, pelo, pelle), autoanticorpi sierici (anti-dsDNA, IgG), proteinuria, istopatologia.
Basato su meccanismi – Modello PBMC umano per terapie specifiche per l’uomo; modelli allogenici per GVHD mediata da cellule T; modello cronico per la patologia mediata da autoanticorpi.
Valore traslazionale – Ideale per testare immunosoppressori (inibitori della calcineurina, inibitori di mTOR), farmaci biologici (anti-TNF, anti-IL-6R) e terapie cellulari.
Pacchetti dati pronti per IND – Gli studi possono essere condotti in conformità con i principi GLP.
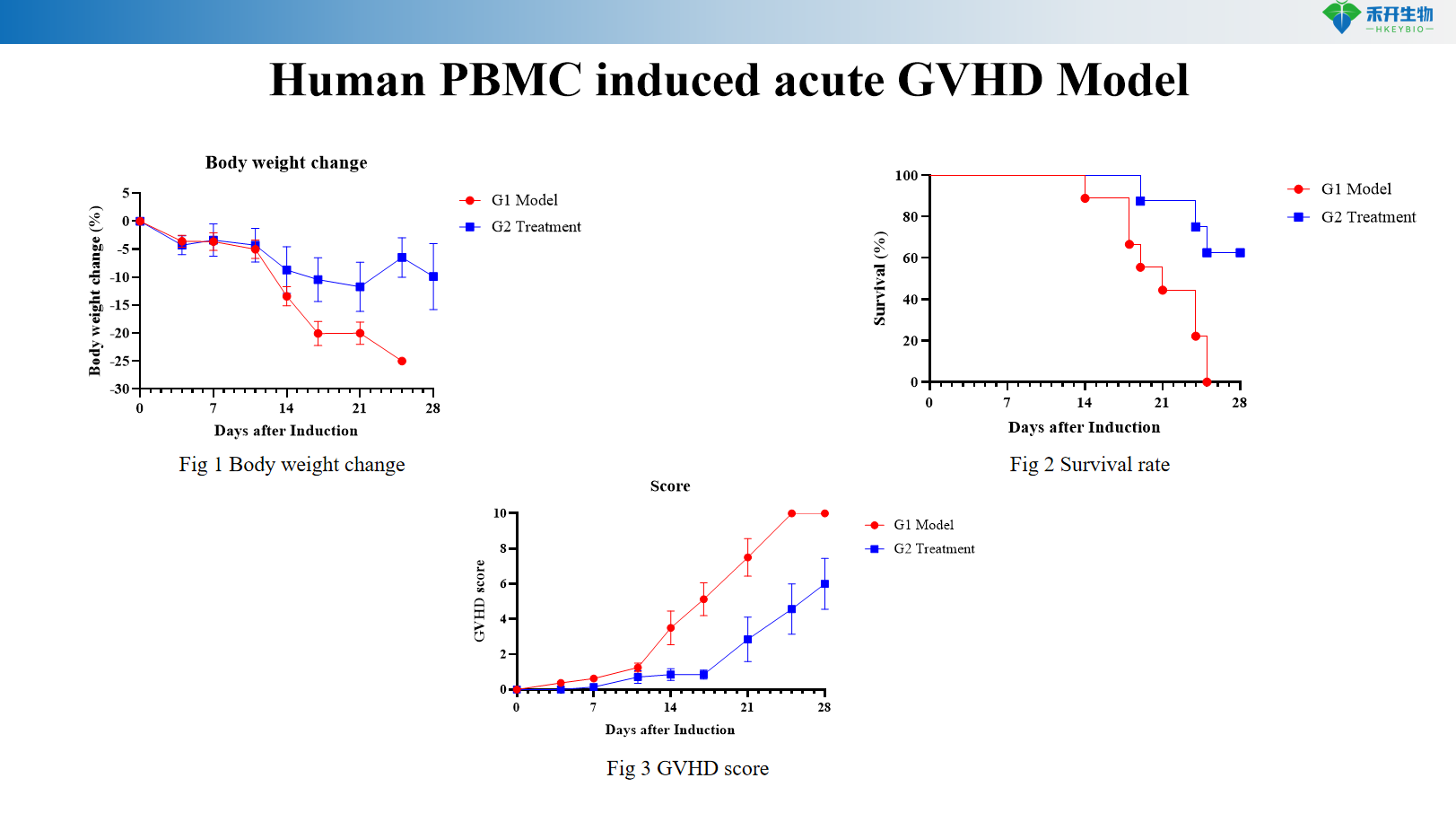
Modello GVHD acuto indotto da PBMC umano
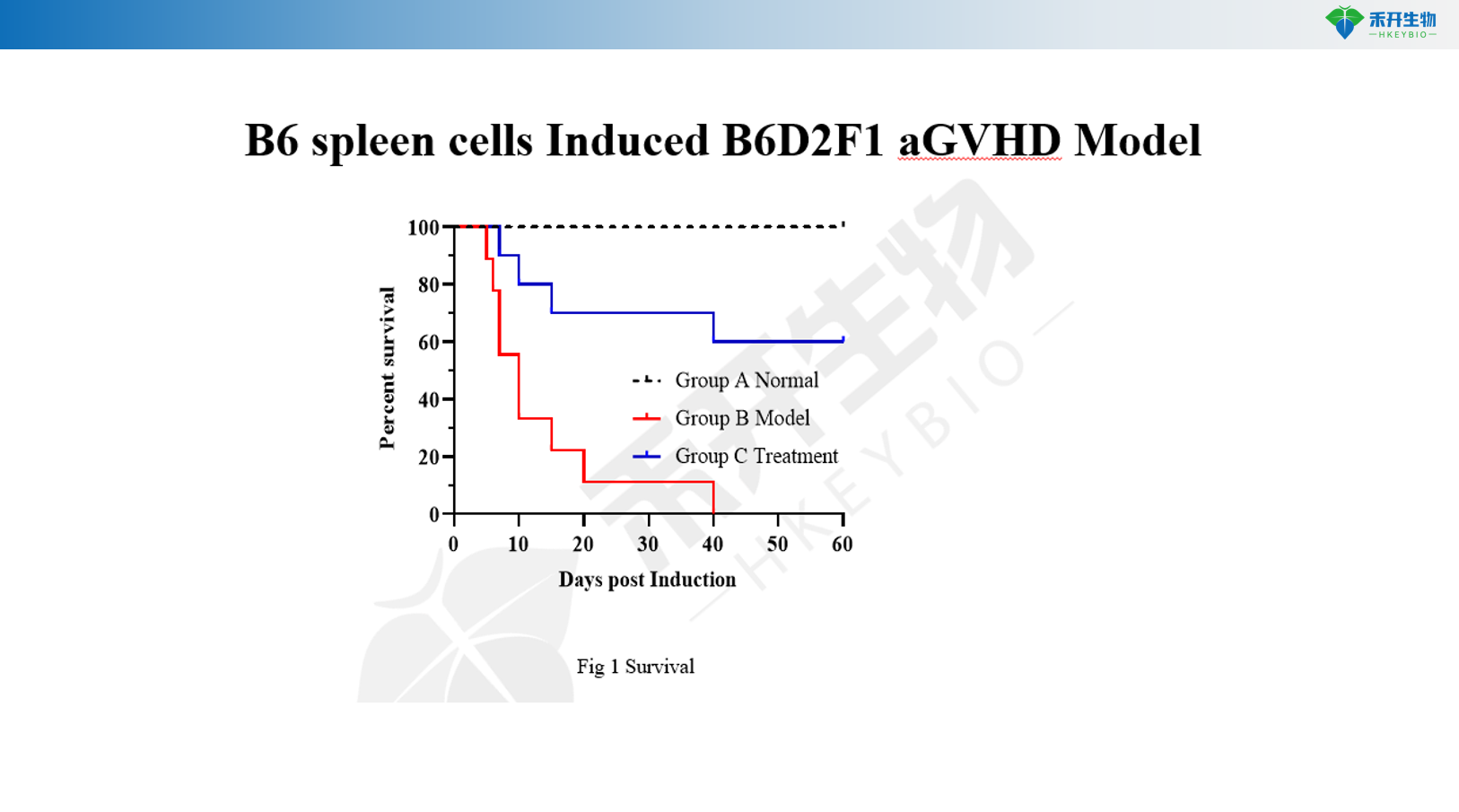
Cellule della milza B6 Modello aGVHD B6D2F1 indotto
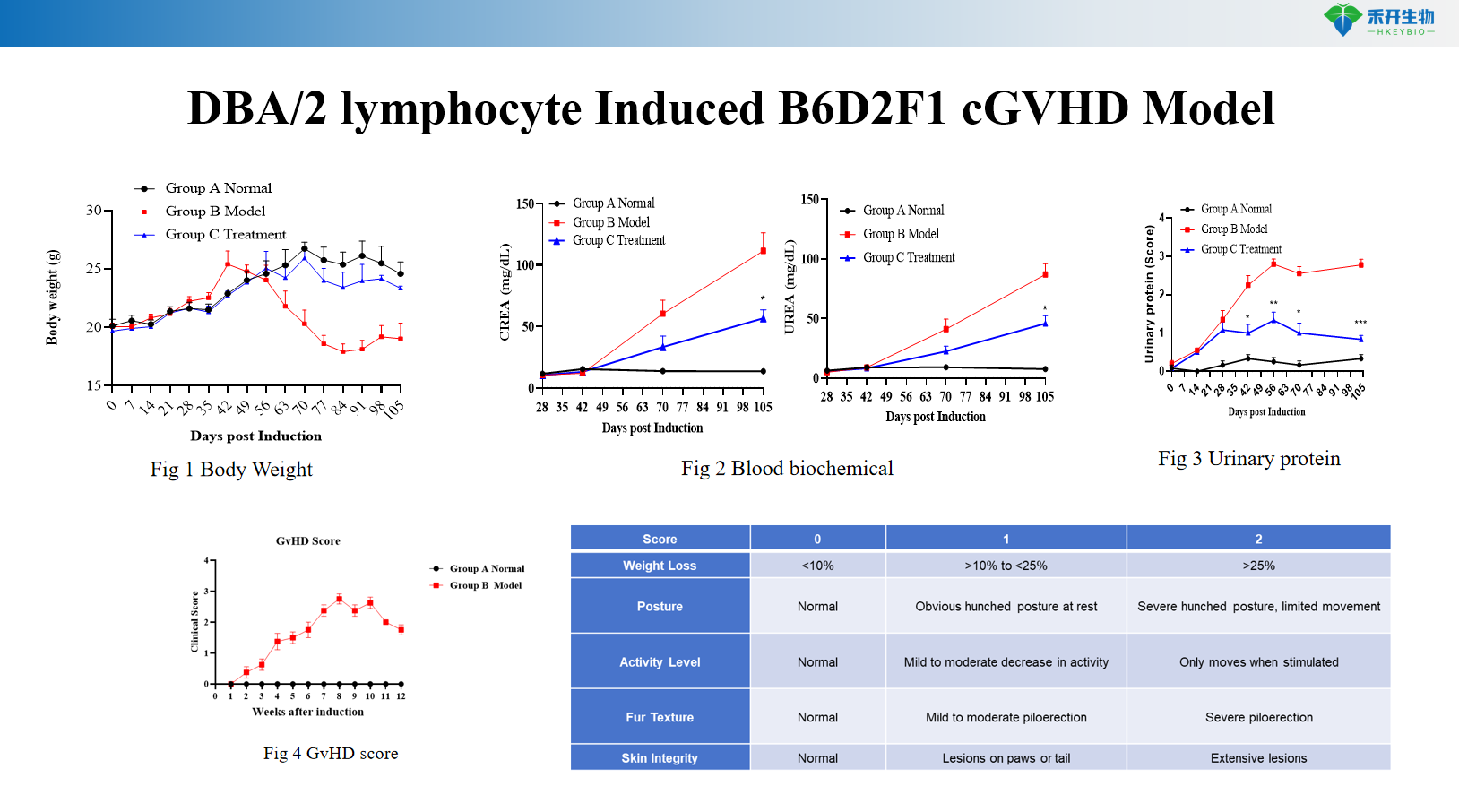
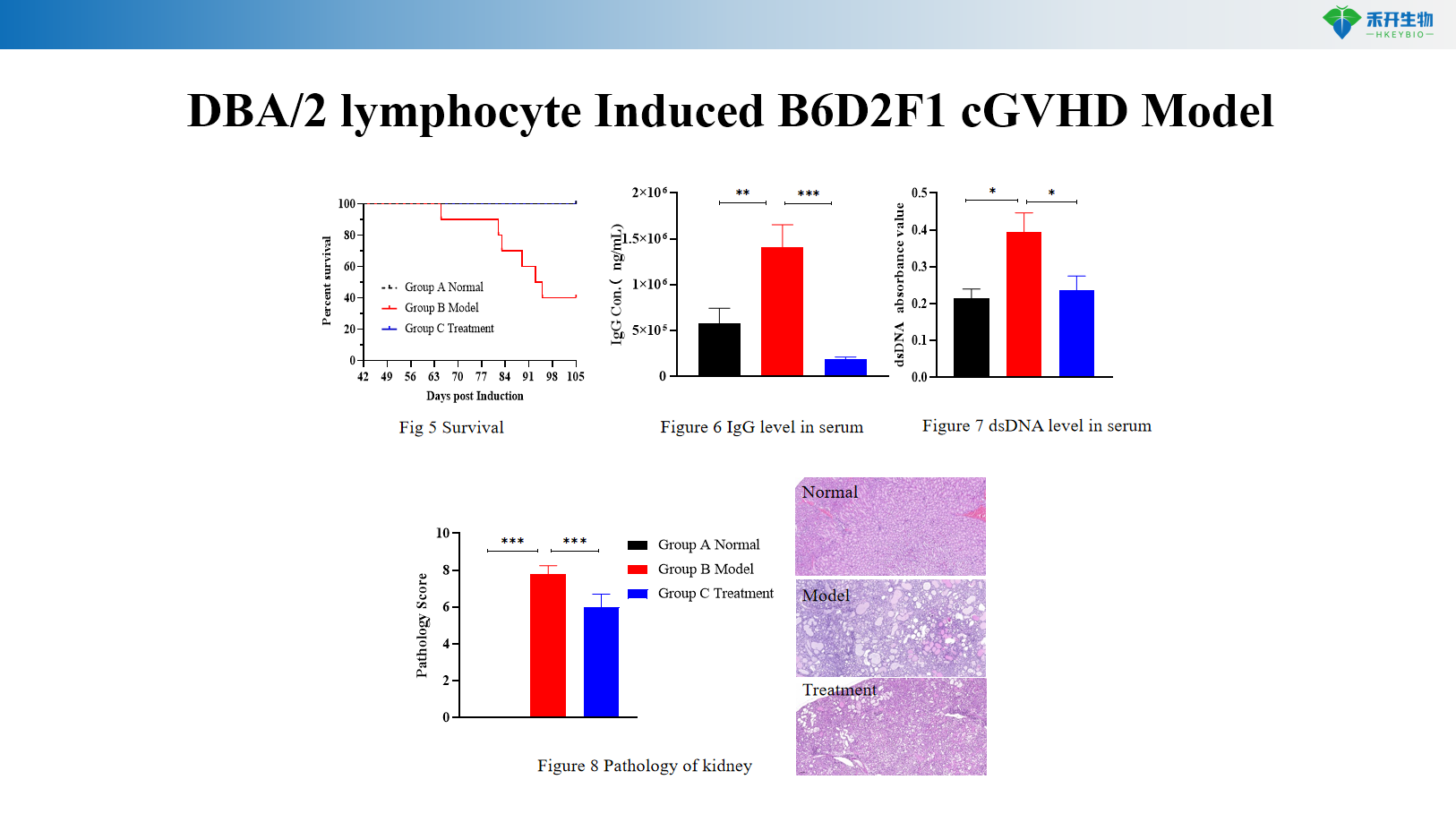
Modello cGVHD B6D2F1 indotto da linfociti DBA/2
• Test di efficacia degli immunosoppressori (tacrolimus, ciclosporina, micofenolato mofetile, inibitori di mTOR) per la prevenzione e il trattamento della GVHD
• Valutazione di farmaci biologici mirati alle cellule T (anti-CD3, anti-CD4), alle citochine (anti-IL-6R, anti-TNF) e alle vie di costimolazione (CTLA-4-Ig)
• Sperimentazione di terapie cellulari (Tregs, MSC) e strategie di deplezione degli anticorpi
• Convalida del target per l'attivazione delle cellule T, la produzione di autoanticorpi e la patologia multiorgano
• Studi farmacologici e tossicologici che consentono l'IND
Parametro |
Modello aGVHD PBMC umano |
B6 → B6D2F1 Modello aGVHD | DBA/2 → Modello cGVHD B6D2F1 |
Specie/ceppo |
Mouse NSG (destinatario) |
B6 → B6D2F1 | DBA/2 → B6D2F1 |
Tipo di malattia |
Acuto (xenogenico) | Acuto (allogenico) | Cronico (simile al lupus) |
Endpoint chiave |
Peso corporeo, sopravvivenza, punteggio GVHD | Sopravvivenza, punteggio GVHD | Peso corporeo, sopravvivenza, punteggio GVHD, IgG sieriche, anti-dsDNA, proteinuria, biochimica del sangue, patologia renale |
D: Quali sono le differenze tra i tre modelli GVHD?
R: Il modello PBMC umano è xenogenico, ideale per testare terapie specifiche per l'uomo. Il modello B6 → B6D2F1 è una GVHD acuta allogenica non corrispondente per MHC. Il modello DBA/2 → B6D2F1 è una GVHD cronica, simile al lupus, con produzione di autoanticorpi, nefrite e fibrosi multiorgano.
D: Quale modello è più adatto per testare prodotti biologici antiumani?
R: Il modello aGVHD indotto da PBMC umano nei topi NSG è la scelta preferita per valutare gli anticorpi specifici dell'uomo (ad esempio, anti-CD3, anti-CD4, anti-IL-6R) poiché le cellule T del donatore sono umane.
D: Questi modelli possono essere utilizzati per studi abilitanti all’IND?
R: Sì. Gli studi possono essere condotti in conformità con i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diversi numeri di cellule del donatore, tempi di trattamento)?
R: Assolutamente. Il nostro team scientifico adatta protocolli di induzione, programmi di trattamento e analisi degli endpoint al tuo specifico farmaco candidato.
D: Qual è la tempistica tipica per uno studio pilota sull'efficacia?
R: Gli studi sulla GVHD acuta si svolgono generalmente 4-6 settimane dopo il trapianto; Gli studi sulla GVHD cronica possono estendersi fino a 8-12 settimane per lo sviluppo completo di autoanticorpi e patologie d'organo.
