| Disponibilità: | |
|---|---|
| Quantità: | |











Ampio portafoglio di modelli : modelli di allergeni (OVA, HDM, Fel d 1), combinati con adiuvanti (LPS, c‑di‑GMP) e guidati da TSLP (MC903) che coprono endotipi di asma granulocitico eosinofilo, neutrofilo e misto.
Ceppi multipli : topi transgenici C57BL/6, BALB/c, HIS umanizzati e IL4/IL4R disponibili.
Endpoint completi : peso corporeo, AHR (Penh, resistenza), conta delle cellule BALF (eosinofili, neutrofili, macrofagi), IgE sieriche totali e IgE allergene-specifiche, profilo delle citochine (IL‑4, IL‑5, IL‑13, IL‑17), istopatologia polmonare (HE, Masson, PAS), ematologia.
Valore traslazionale – Ideale per testare farmaci biologici (anti‑IL‑4Rα, anti‑IL‑5, anti‑IL‑13, anti‑TSLP, anti‑IL‑33), inibitori JAK, corticosteroidi e broncodilatatori.
Pacchetti dati pronti per IND : gli studi possono essere condotti in conformità con i principi GLP.
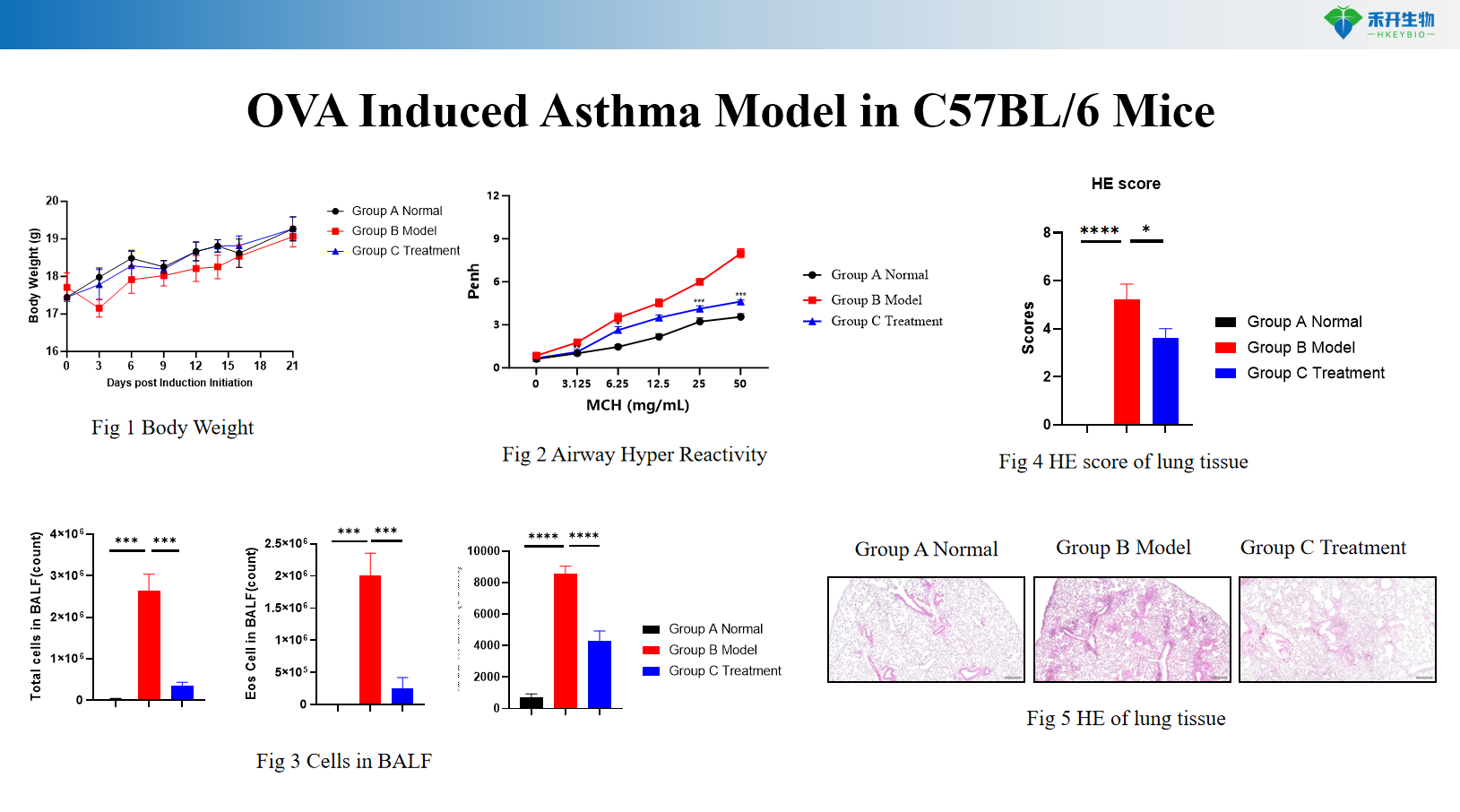
Modello di asma indotto da OVA in topi C57BL/6
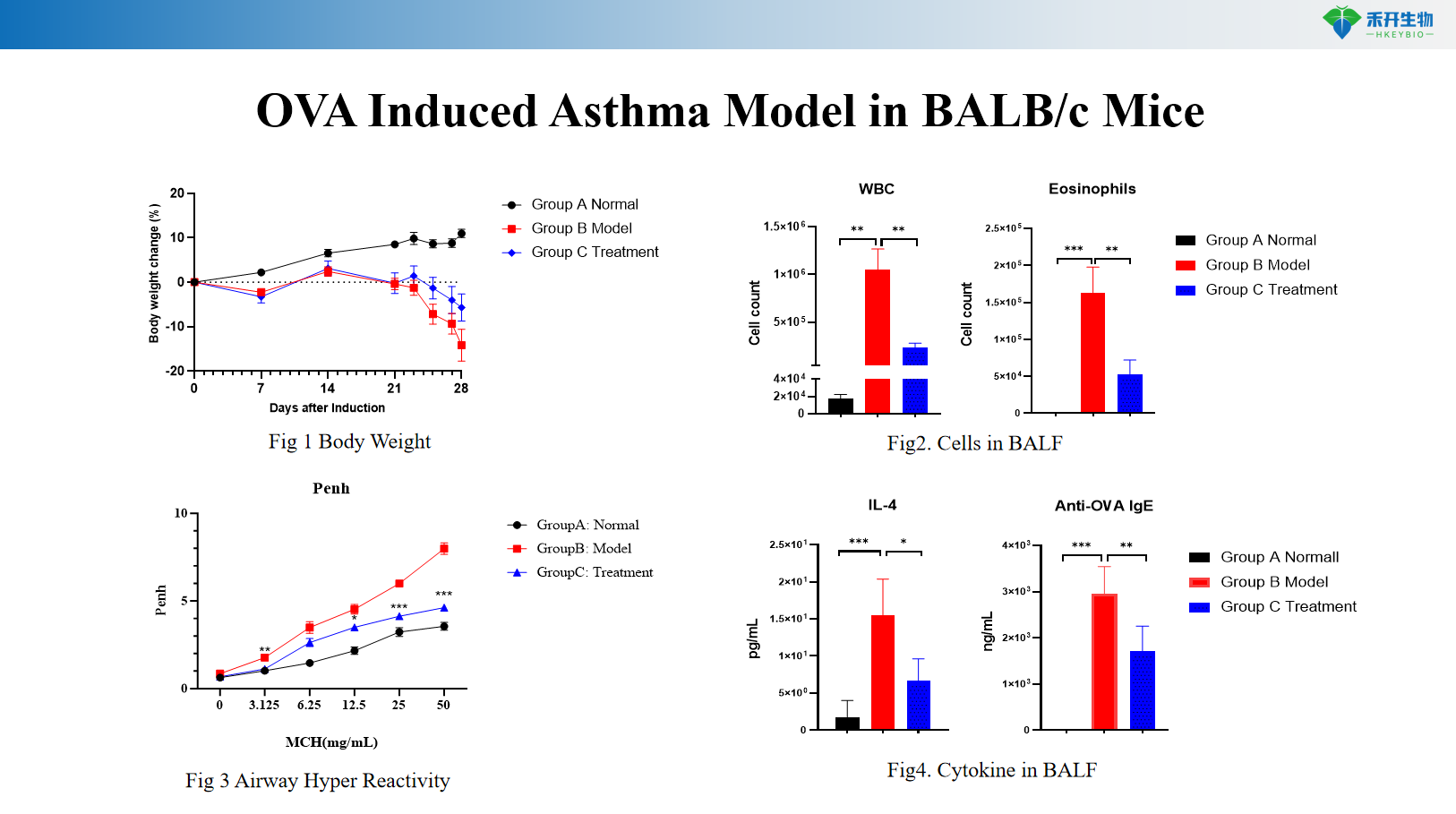
Modello di asma indotto da OVA nei topi BALB/c
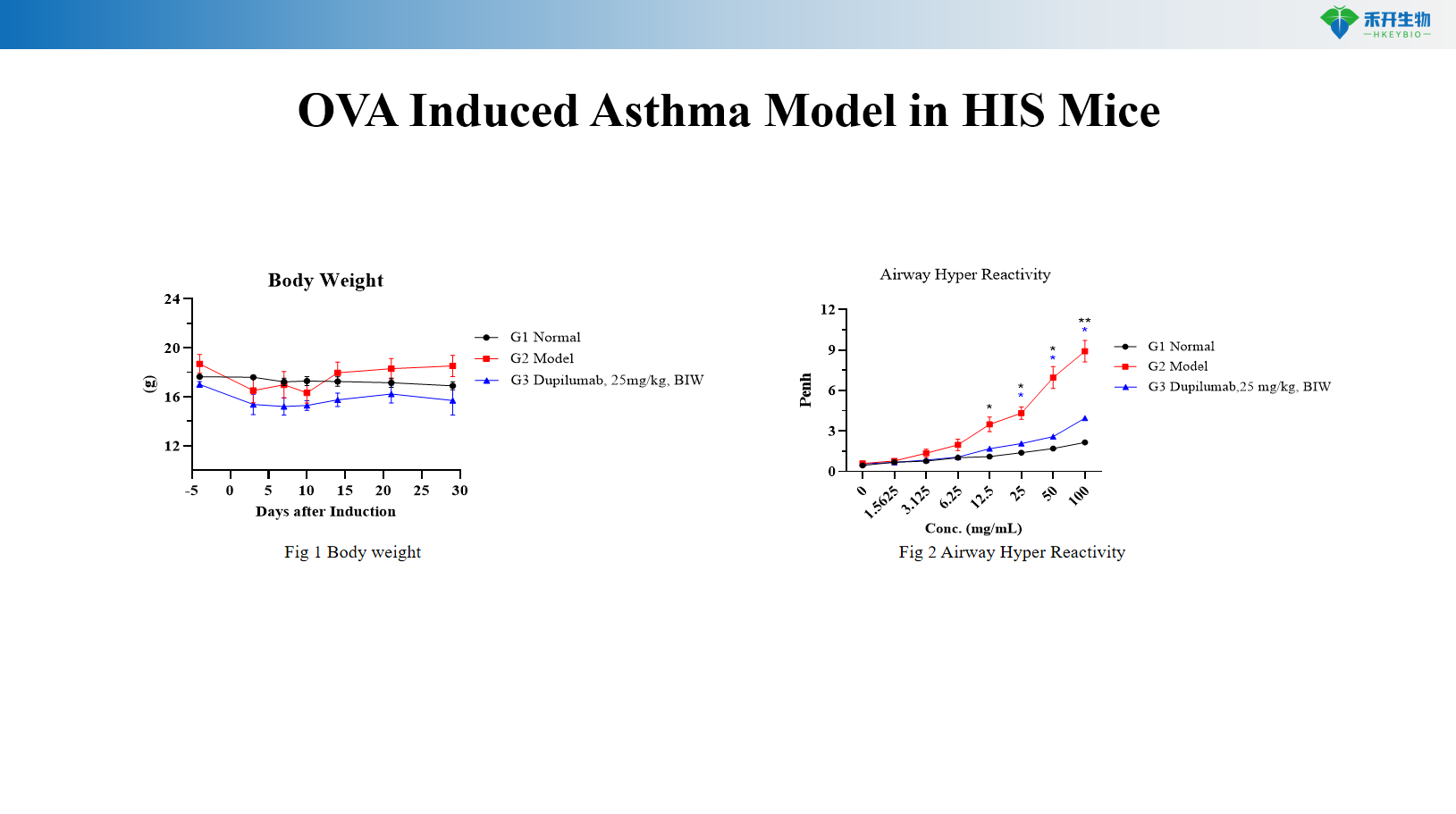
Modello di asma indotto da OVA nei topi HIS
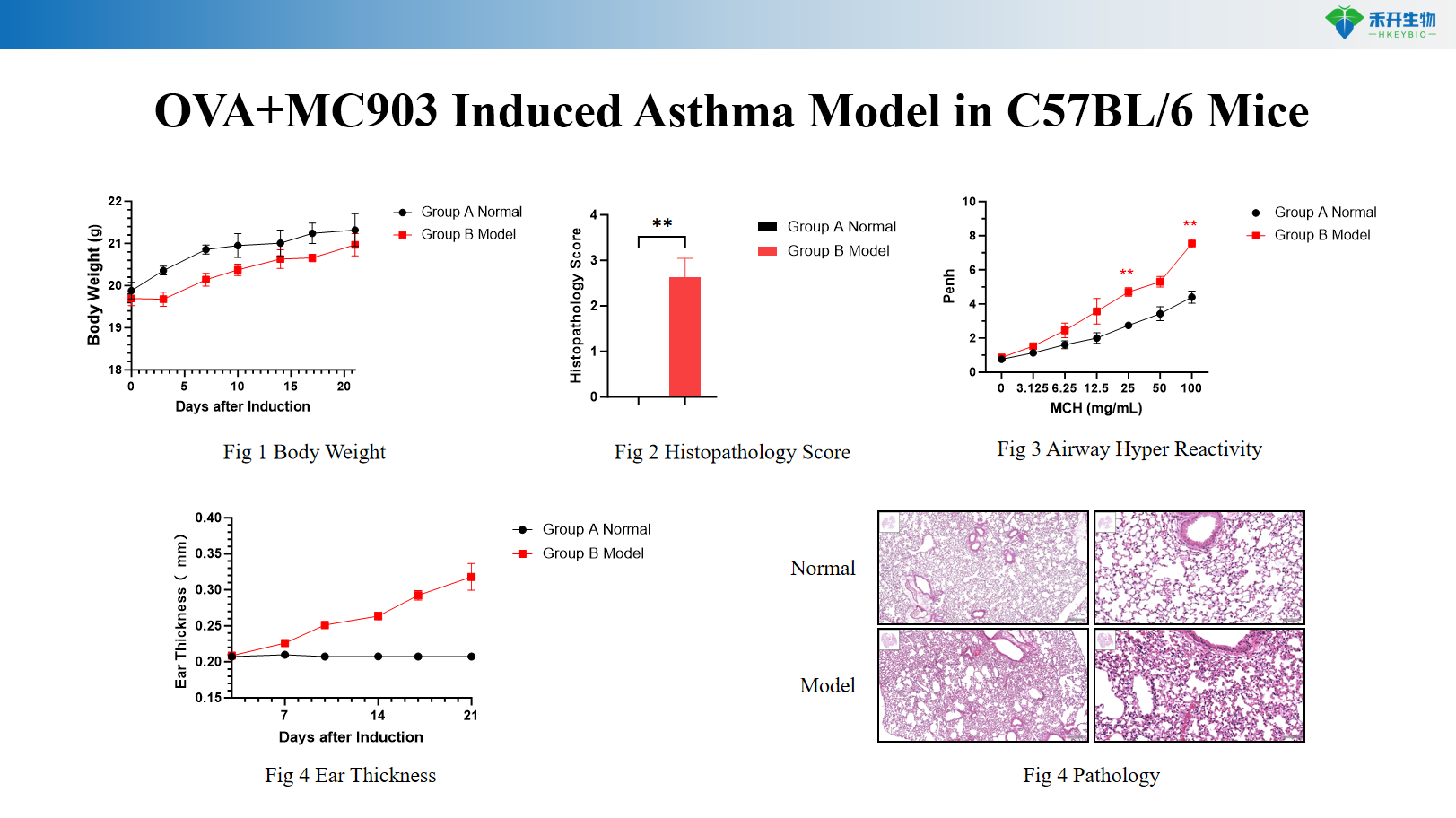
Modello di asma indotto OVA+MC903 in topi C57BL/6
Modello di asma neutrofilo indotto da OVA+LPS in topi C57BL/6
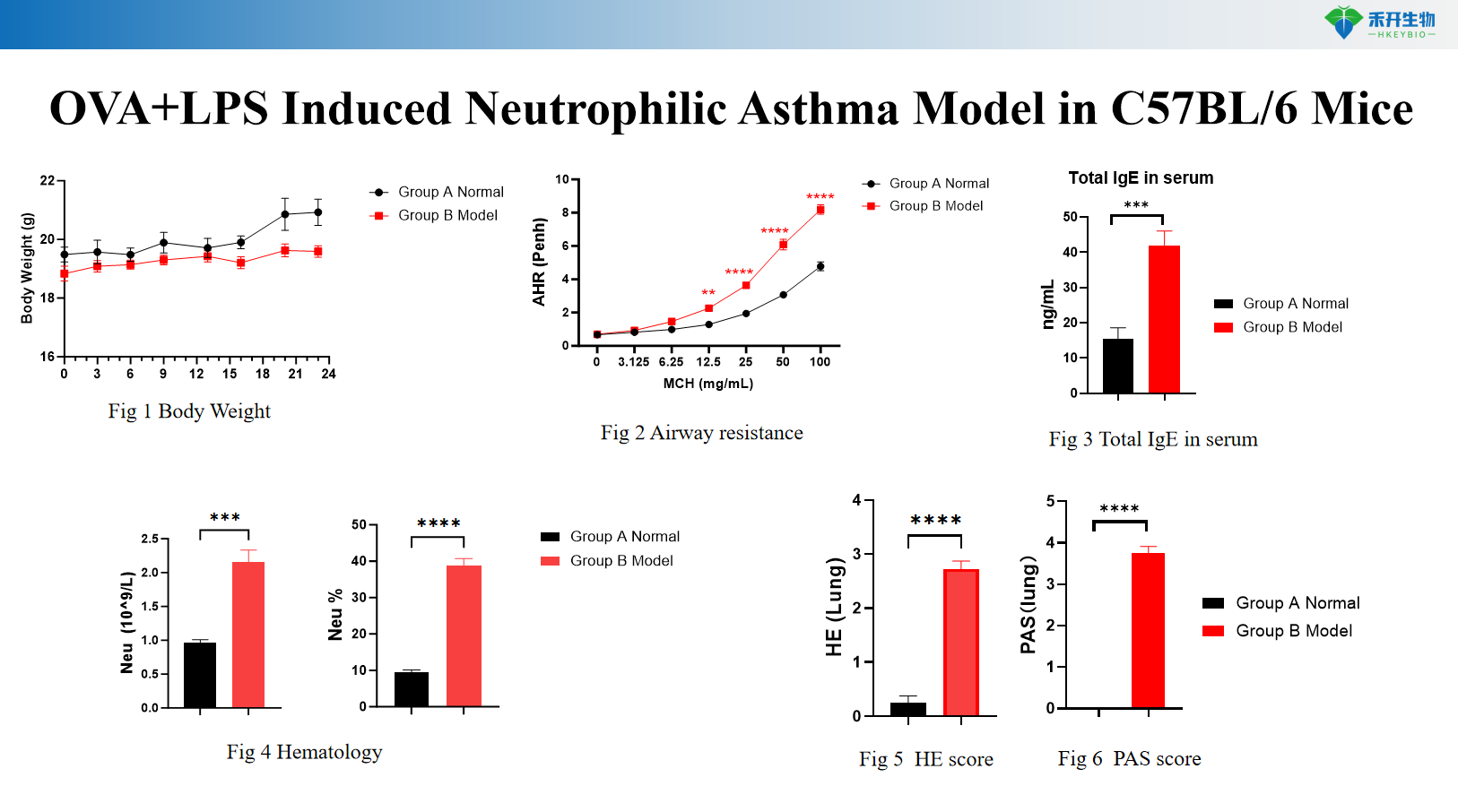
Modello di asma indotto da HDM nei topi C57BL/6
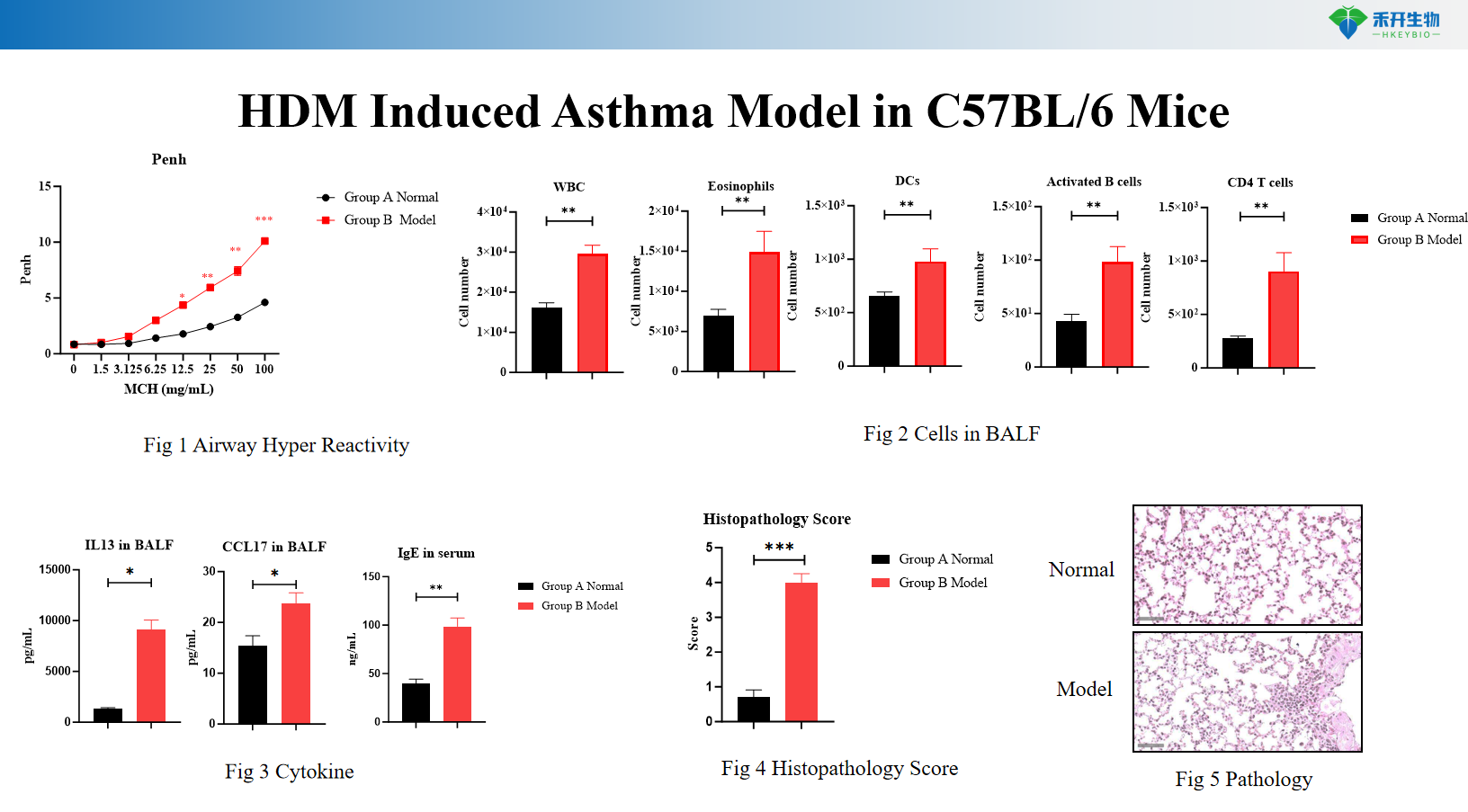
Modello di asma indotto da HDM nei topi IL4/IL4R
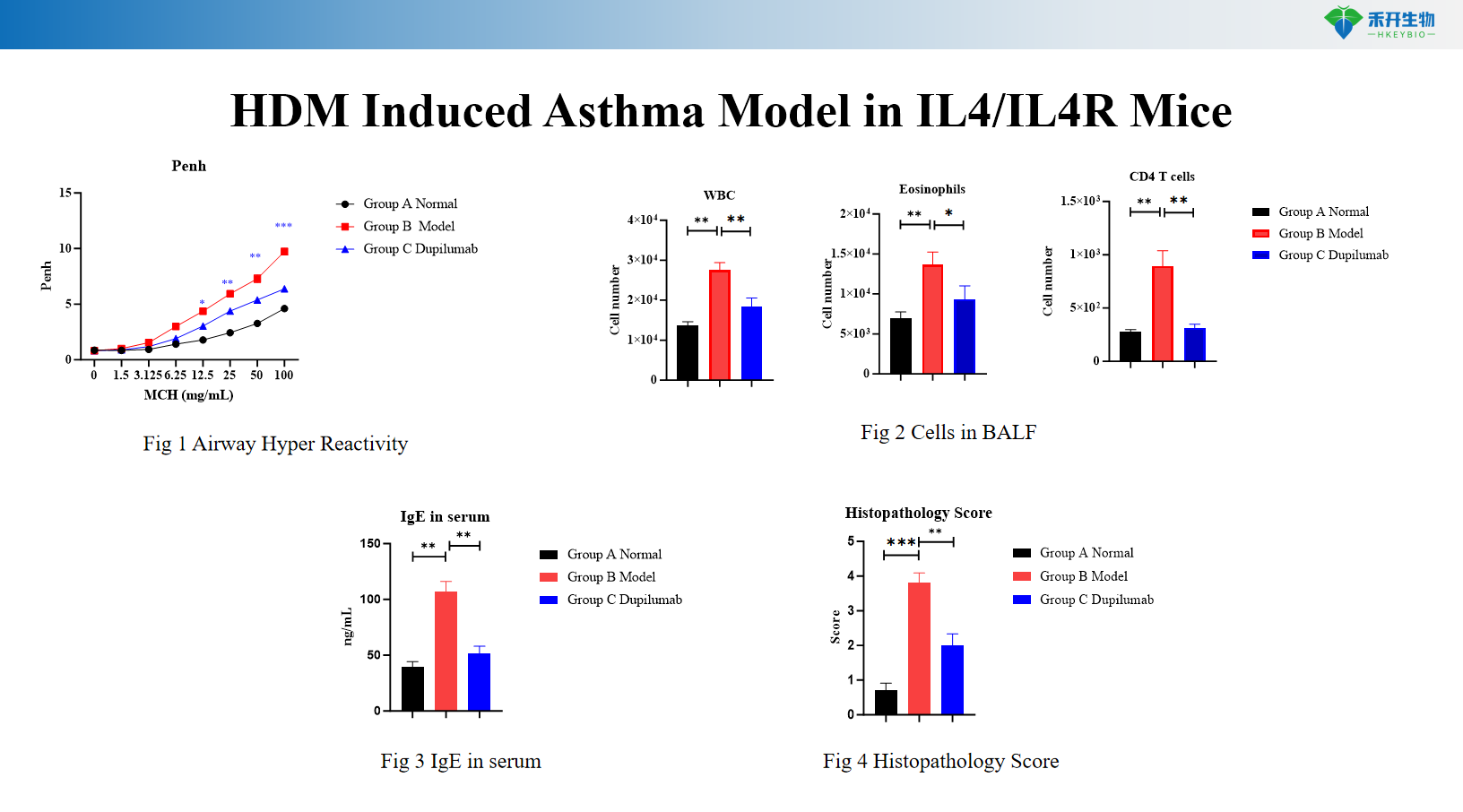
Modello di asma indotto HDM+LPS nei topi C57BL/6
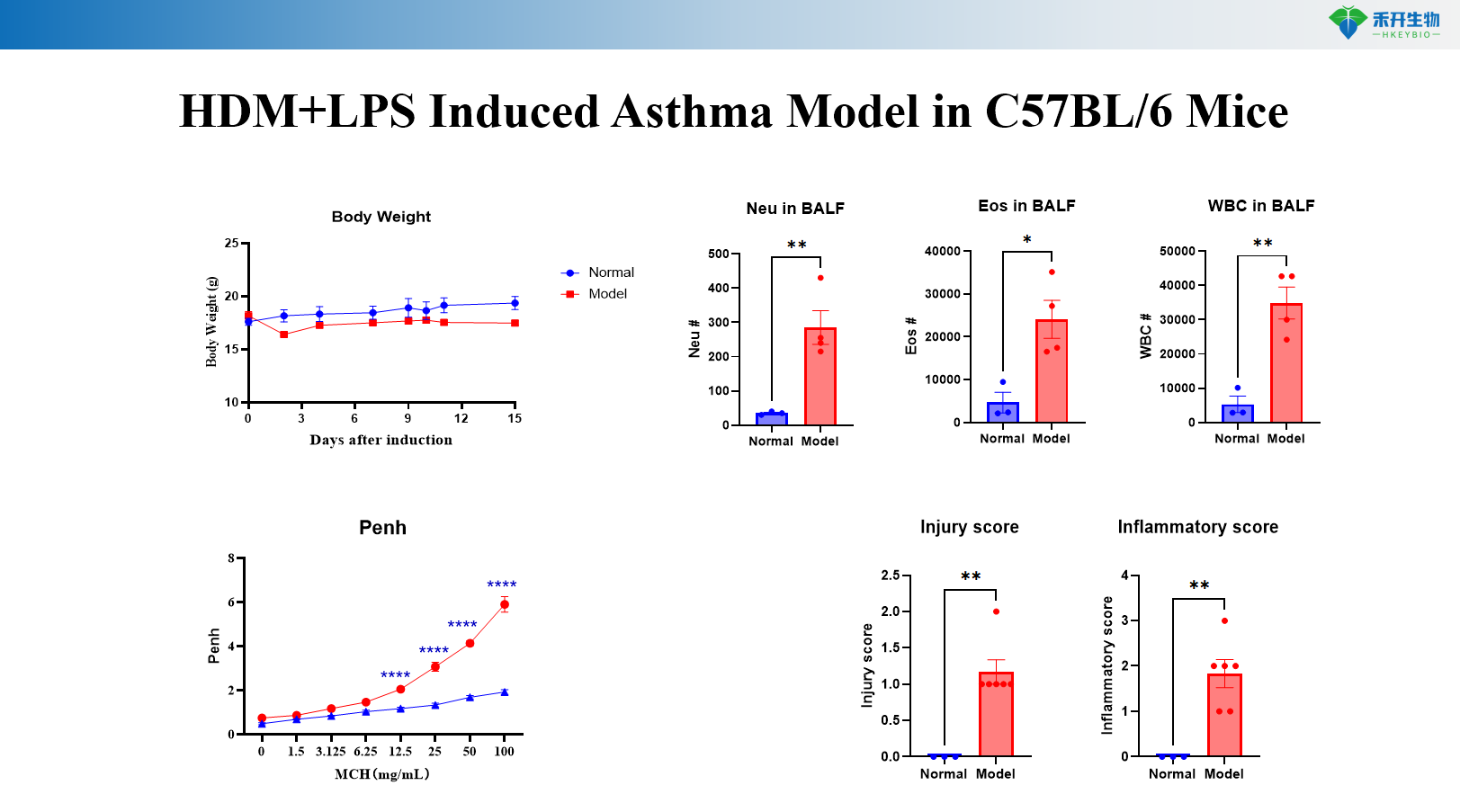
Modello di asma indotto HDM+MC903 nei topi C57BL/6

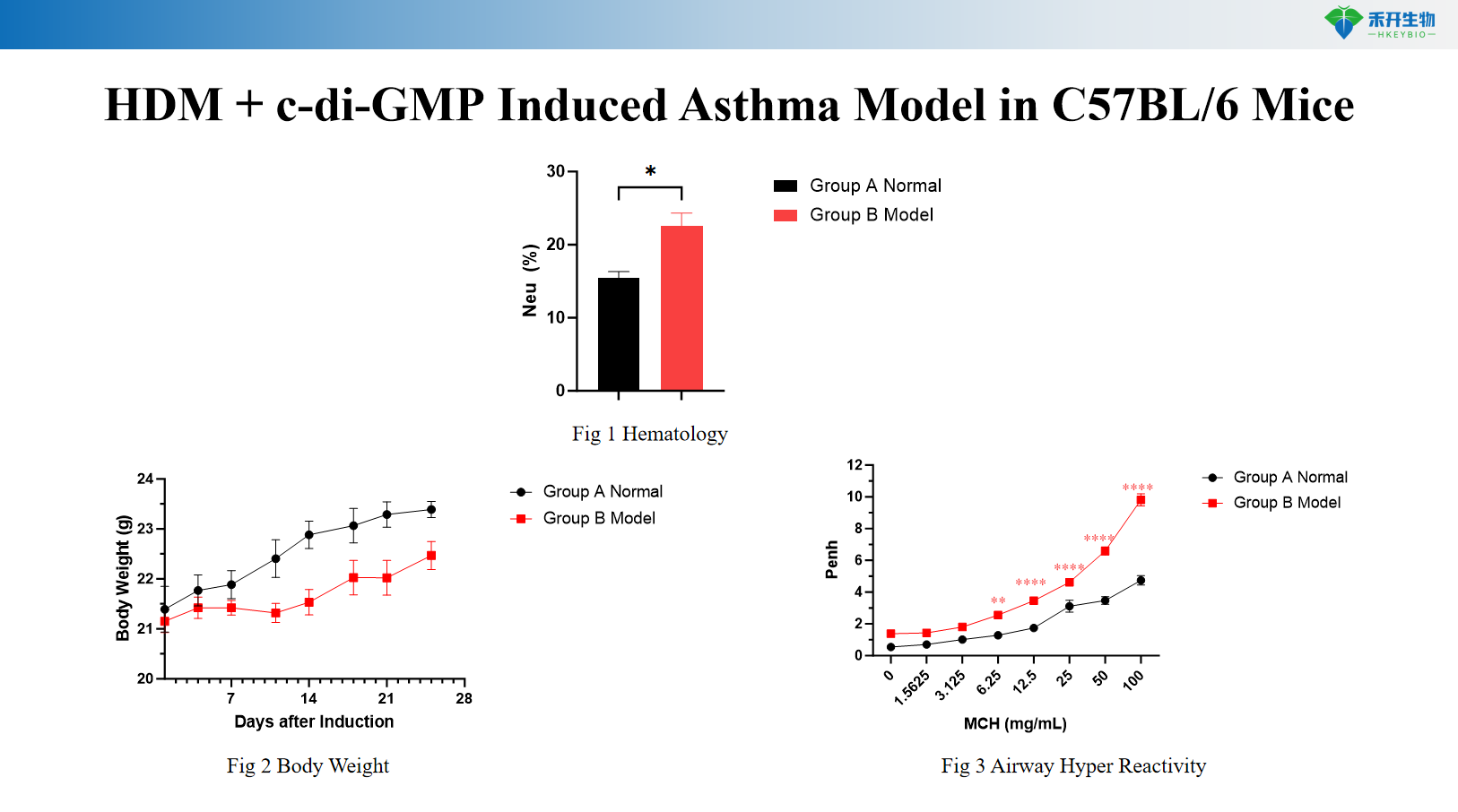
Modello di asma indotto HDM + c-di-GMP in topi C57BL/6
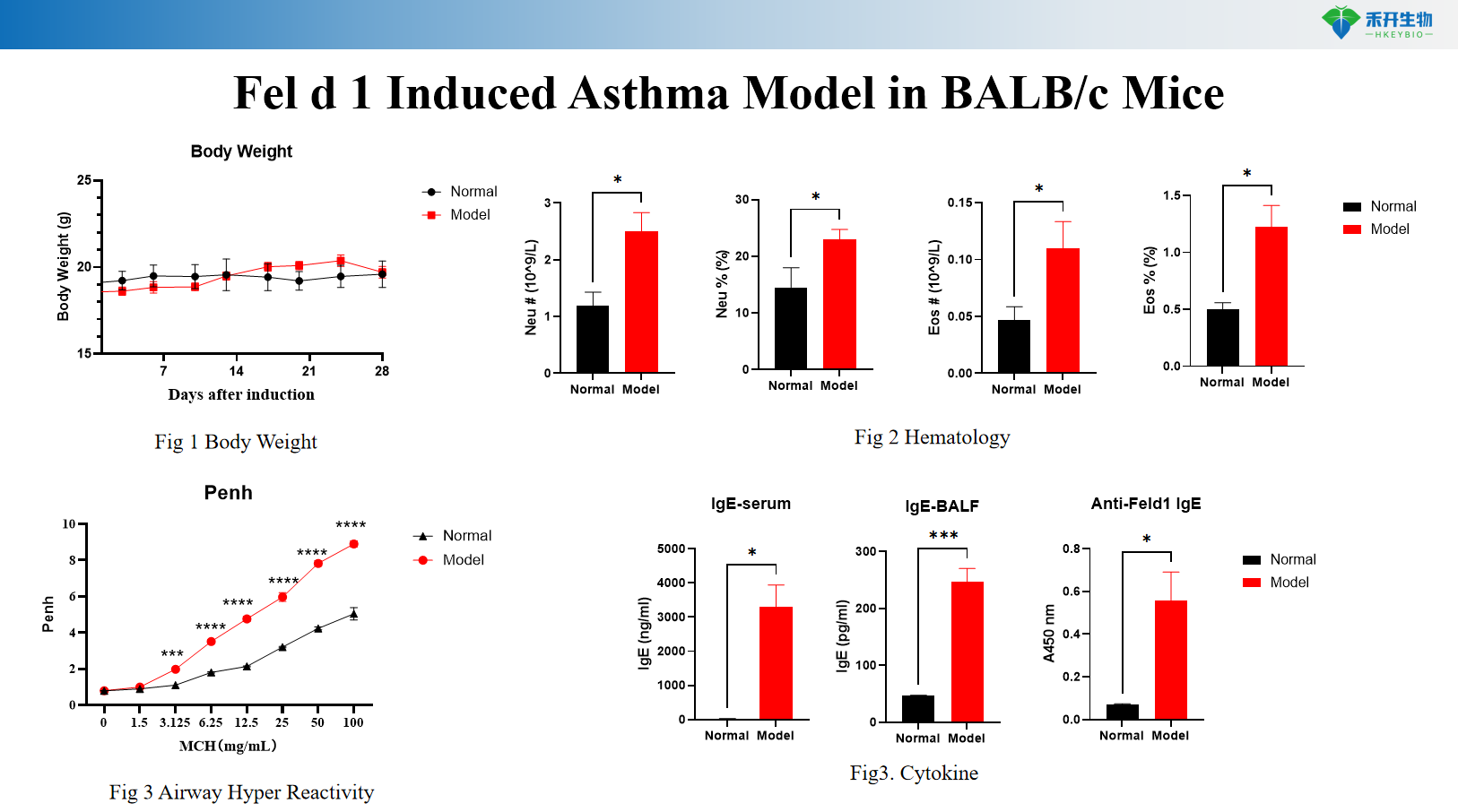
Modello Fel d 1 di asma indotto nei topi BALB/c
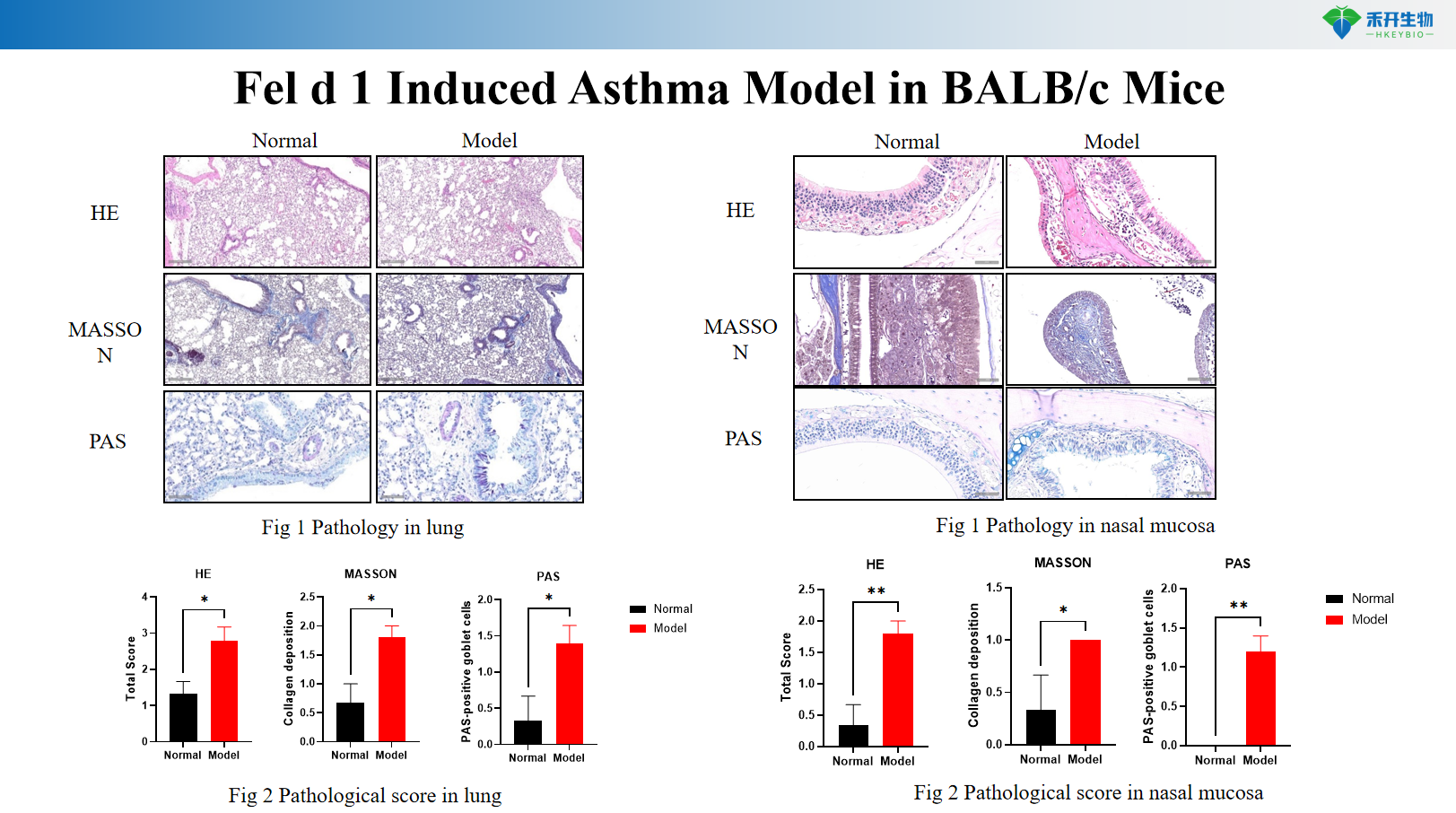
• Test di efficacia dei farmaci biologici (anti-IL-4Rα, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33)
• Valutazione di inibitori di piccole molecole (inibitori JAK, inibitori PDE4, antagonisti CRTH2)
• Convalida del target per le vie delle citochine Th2, Th17 e di derivazione epiteliale
• Scoperta di biomarcatori (IgE, firme di citochine, marcatori di eosinofili/neutrofili)
• Studi farmacologici e tossicologici che consentono l'IND
Parametro |
Specificazione |
Specie/ceppo |
C57BL/6, BALB/c, HIS umanizzato, IL4/IL4R transgenico |
Metodo di induzione |
OVA ± allume ± MC903 ± LPS; HDM ± LPS ± MC903 ± c‑di‑GMP; Fel d 1 + allume |
Durata dello studio |
3–8 settimane (fasi di sensibilizzazione + sfida) |
Endpoint chiave |
Peso corporeo, AHR (invasivo/non invasivo), citologia BALF (eosinofili, neutrofili, macrofagi), IgE sieriche totali e IgE allergene-specifiche, livelli di citochine (IL‑4, IL‑5, IL‑13, IL‑17, IFN‑γ), istopatologia polmonare (HE, Masson, PAS) con punteggio, ematologia (facoltativa) |
| Controllo positivo | Desametasone o anticorpo anti‑IL‑4Rα disponibili come composti di riferimento |
Pacchetto dati |
Dati grezzi, rapporti di analisi, conteggi cellulari BALF, risultati ELISA, vetrini istologici, dati sulla funzionalità polmonare, bioinformatica (facoltativo) |
D: Come faccio a scegliere il modello AD giusto per il mio farmaco candidato?
R: Per l'asma eosinofilo (Th2‑alto), si consigliano i modelli OVA o HDM in BALB/c o C57BL/6. Per l'asma granulocitico neutrofilo o misto, sono appropriati i modelli OVA+LPS o HDM+c‑di‑GMP in C57BL/6. I topi umanizzati HIS sono ideali per testare prodotti biologici specifici per l'uomo. I topi transgenici IL4/IL4R sono adatti per gli studi sulla via Th2. Il nostro team scientifico può guidare la selezione del modello in base al tuo target specifico.
D: Qual è la differenza tra i modelli indotti da OVA e HDM?
R: L'OVA è un allergene modello che richiede un adiuvante per la sensibilizzazione, producendo robuste risposte Th2. L’HDM è un allergene umano clinicamente rilevante contenente proteasi che attivano sia l’immunità innata che quella adattativa, imitando più da vicino la patogenesi dell’asma allergico umano.
D: Questi modelli possono essere utilizzati per studi abilitanti all’IND?
R: Sì. Gli studi possono essere condotti in conformità con i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diversi programmi di sensibilizzazione/challenge, terapie combinate)?
R: Assolutamente. Il nostro team scientifico adatta protocolli di induzione, programmi di trattamento e analisi degli endpoint al tuo specifico farmaco candidato.
D: Qual è la tempistica tipica per uno studio pilota sull'efficacia?
R: La maggior parte dei modelli sull'asma vengono completati entro 4-6 settimane, compresa l'analisi di sensibilizzazione, provocazione, trattamento e endpoint.
