| Disponibilità: | |
|---|---|
| Quantità: | |











Clinicamente rilevante – Riepiloga la SSc-ILD umana con fibrosi polmonare, fibrosi cutanea e patologia mediata da TGF-β.
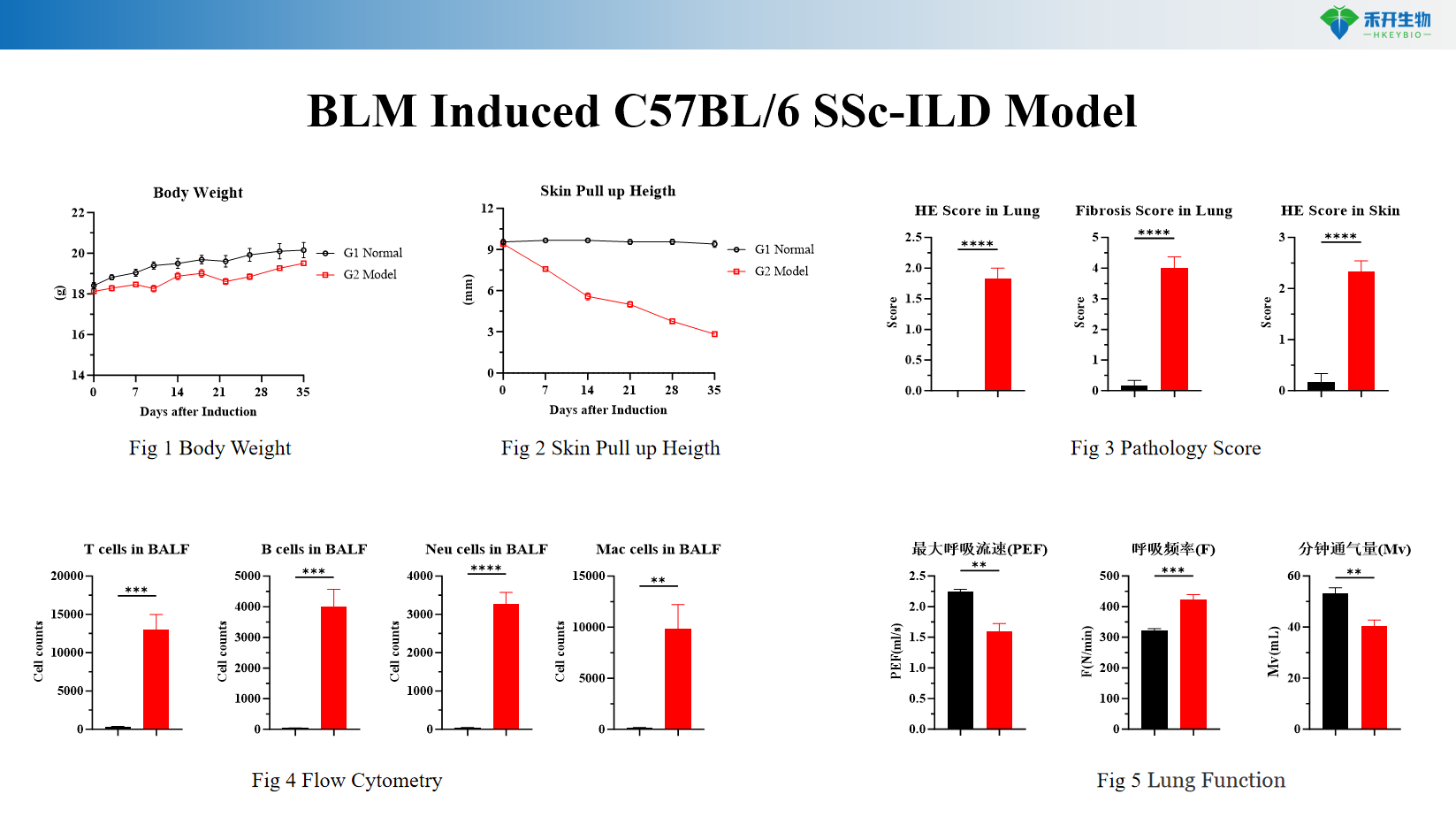
Endpoint completi : peso corporeo, altezza del pull-up della pelle (fibrosi cutanea), funzione polmonare, citometria a flusso (infiltrazione di cellule immunitarie), istopatologia polmonare (colorazione HE e Masson).
Guidato dal meccanismo : il BLM induce danno al DNA, stress ossidativo e attivazione della via del TGF-β, rispecchiando la patogenesi della SSc-ILD umana.
Valore traslazionale – Ideale per testare agenti antifibrotici (nintedanib, pirfenidone), inibitori del TGF-β e immunomodulatori.
Pacchetti dati pronti per IND – Gli studi possono essere condotti in conformità con i principi GLP.
Modello C57BL/6 SSc-ILD indotto da BLM
• Test di efficacia di agenti antifibrotici (nintedanib, pirfenidone, inibitori del TGF-β, inibitori della galectina-3)
• Valutazione di immunomodulatori mirati all'infiammazione e alla fibrosi
• Convalida del target per la segnalazione del TGF-β e le vie fibrotiche
• Scoperta di biomarcatori (marcatori di collagene, mediatori infiammatori, firme di cellule immunitarie)
• Studi farmacologici e tossicologici che consentono l'IND
Parametro |
Specifica |
Specie/ceppo |
Mouse C57BL/6 |
Metodo di induzione |
Instillazione intratracheale di bleomicina (BLM, 1–2 U/kg) in soluzione salina, dose singola |
Durata dello studio |
14-28 giorni (sviluppo di fibrosi) |
Endpoint chiave |
Peso corporeo, altezza del pull-up della pelle (fibrosi cutanea), funzione polmonare (compliance, resistenza), citometria a flusso (infiltrazione di cellule immunitarie: macrofagi, neutrofili, cellule T), istopatologia polmonare (colorazione tricromica HE e Masson con punteggio Ashcroft), opzionale: contenuto di idrossiprolina, conta delle cellule BALF, livelli di citochine |
| Controllo positivo | Nintedanib o pirfenidone disponibili come composti antifibrotici di riferimento |
Pacchetto dati |
Dati grezzi, rapporti di analisi, dati sulla funzionalità polmonare, file di citometria a flusso, vetrini istologici (HE, Masson), bioinformatica (opzionale) |
D: In che modo la bleomicina induce la SSc-ILD nei topi?
R: La bleomicina intratracheale innesca danni al DNA e stress ossidativo nel tessuto polmonare, portando a infiammazione persistente, attivazione della via di segnalazione del TGF-β ed eccessiva deposizione di matrice extracellulare, imitando la fibrosi cutanea e polmonare osservata nella SSc-ILD umana.
D: Quali sono le principali somiglianze con la SSc-ILD umana?
R: Il modello mostra fibrosi polmonare progressiva (colorazione HE e Masson), declino della funzione polmonare, fibrosi cutanea e infiltrazione di cellule immunitarie, rispecchiando da vicino la patologia SSc-ILD umana.
D: Questo modello può essere utilizzato per studi abilitanti all’IND?
R: Sì. Gli studi possono essere condotti in conformità con i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diverse dosi di BLM, tempi di trattamento, combinazione con altri agenti)?
R: Assolutamente. Il nostro team scientifico adatta protocolli di induzione, programmi di trattamento e analisi degli endpoint al tuo specifico farmaco candidato.
D: Qual è la tempistica tipica per uno studio pilota sull'efficacia?
R: Gli studi pilota in genere si svolgono 21-28 giorni dopo l'instillazione del BLM, con lo sviluppo della fibrosi nell'arco di 14-21 giorni e il trattamento somministrato durante o dopo l'induzione.
