| Disponibilità: | |
|---|---|
| Quantità: | |











Clinicamente rilevante : l’ALI indotta da LPS imita da vicino l’ALI/ARDS umana con infiammazione acuta, infiltrazione leucocitaria ed edema polmonare.
Endpoint completi : conta delle cellule BALF (linfociti, neutrofili, macrofagi), profilazione delle citochine (MCP-1, IL-6, IL-10), istopatologia polmonare (HE, IHC), valutazione dell'edema polmonare (rapporto umido/secco).
Guidato dal meccanismo – LPS attiva la segnalazione TLR4, innescando la via NF-κB e una robusta risposta infiammatoria, rispecchiando il danno polmonare indotto dalla sepsi Gram-negativi.
Valore traslazionale – Ideale per testare farmaci antinfiammatori, inibitori delle citochine, inibitori dell'elastasi dei neutrofili e terapie cellulari.
Pacchetti dati pronti per IND – Gli studi possono essere condotti in conformità con i principi GLP.
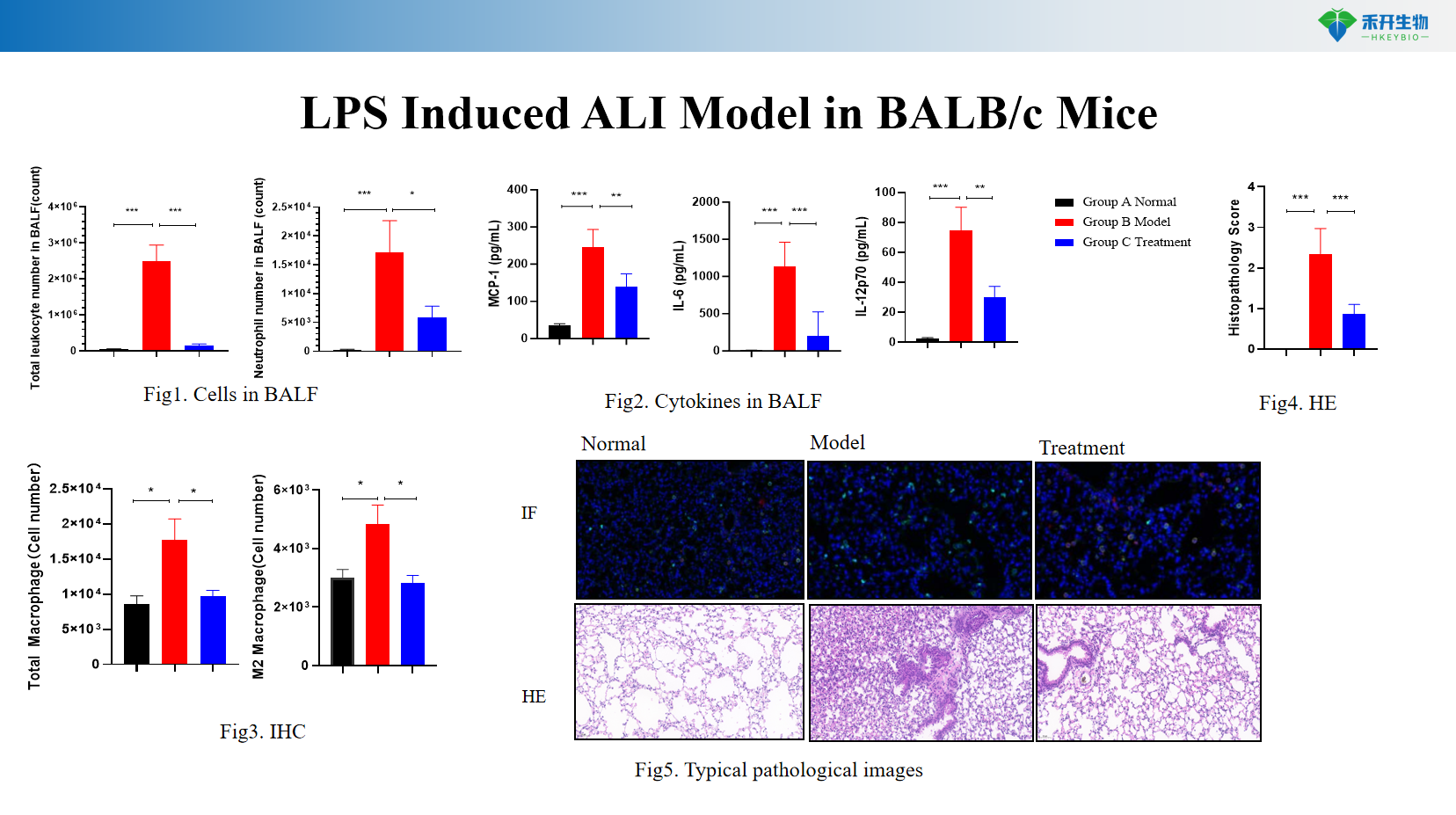
Modello ALI indotto da LPS nei topi BALB/c
• Test di efficacia di farmaci antinfiammatori (corticosteroidi, FANS), inibitori delle citochine (anti-IL-6, anti-TNF-α) e inibitori dell'elastasi neutrofila
• Valutazione della terapia con cellule staminali mesenchimali (MSC) e trattamenti basati su vescicole extracellulari
• Convalida del target per la segnalazione TLR4, la via NF-κB e le cascate infiammatorie
• Scoperta di biomarcatori (profili cellulari BALF, firme di citochine, marcatori di lesioni polmonari)
• Studi farmacologici e tossicologici che consentono l'IND
Parametro |
Specifica |
Specie/ceppo |
Mouse BALB/c |
Metodo di induzione |
Somministrazione intratracheale, intranasale o intraperitoneale di lipopolisaccaride (LPS, 5-10 mg/kg) |
Durata dello studio |
Acuto: 6–48 ore dopo la somministrazione di LPS |
Endpoint chiave |
Conta delle cellule BALF (totale e differenziale: neutrofili, macrofagi, linfociti), livelli di citochine BALF (MCP-1, IL-6, IL-10 mediante ELISA), istopatologia polmonare (colorazione HE con punteggio di danno polmonare), immunoistochimica (IHC) per marcatori infiammatori, rapporto peso umido/secco del polmone (edema polmonare), opzionale: attività MPO, marcatori di stress ossidativo |
Pacchetto dati |
Dati grezzi, rapporti di analisi, conteggi cellulari BALF, risultati ELISA, vetrini istologici (HE, IHC), bioinformatica (opzionale) |
D: In che modo l'LPS induce un danno polmonare acuto nei topi?
R: LPS si lega a TLR4 sulle cellule immunitarie, attivando le vie NF-κB e MAPK, portando a una robusta risposta infiammatoria con rilascio di citochine (IL-6, TNF-α, MCP-1), reclutamento di neutrofili nei polmoni, aumento della permeabilità vascolare e danno alveolare, imitando da vicino l'ALI indotta dalla sepsi Gram-negativa.
D: Quali sono le principali somiglianze con l'ALI/ARDS umana?
R: Il modello presenta infiltrazione di neutrofili, elevate citochine proinfiammatorie, edema polmonare e caratteristiche istopatologiche (ispessimento alveolare, formazione di membrana ialina) identiche all'ALI/ARDS umana.
D: Questo modello può essere utilizzato per studi abilitanti all’IND?
R: Sì. Gli studi possono essere condotti in conformità con i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diverse dosi di LPS, vie di somministrazione, punti temporali)?
R: Assolutamente. Il nostro team scientifico adatta i regimi di dosaggio degli LPS, le vie di somministrazione e le analisi degli endpoint al tuo specifico farmaco candidato.
