| Tình trạng sẵn có: | |
|---|---|
| Số lượng: | |











Danh mục mô hình rộng – Các mô hình gây dị ứng (OVA, HDM, Fel d 1), kết hợp bổ trợ (LPS, c‑di‑GMP) và TSLP (MC903) bao gồm các kiểu bệnh hen suyễn tăng bạch cầu ái toan, bạch cầu trung tính và hỗn hợp.
Nhiều chủng – có sẵn chuột biến đổi gen C57BL/6, BALB/c, HIS được nhân hóa và IL4/IL4R.
Tiêu chí toàn diện – Trọng lượng cơ thể, AHR (Penh, sức đề kháng), số lượng tế bào BALF (bạch cầu ái toan, bạch cầu trung tính, đại thực bào), tổng lượng IgE trong huyết thanh và IgE đặc hiệu với chất gây dị ứng, hồ sơ phân tích cytokine (IL-4, IL-5, IL-13, IL-17), mô bệnh học phổi (HE, Masson, PAS), huyết học.
Giá trị tịnh tiến – Lý tưởng để thử nghiệm các chế phẩm sinh học (kháng IL‑4Rα, kháng IL‑5, kháng IL‑13, kháng TSLP, kháng IL‑33), thuốc ức chế JAK, corticosteroid và thuốc giãn phế quản.
Gói dữ liệu sẵn có của IND – Các nghiên cứu có thể được tiến hành theo nguyên tắc GLP.
Mô hình bệnh hen suyễn do OVA ở chuột C57BL/6
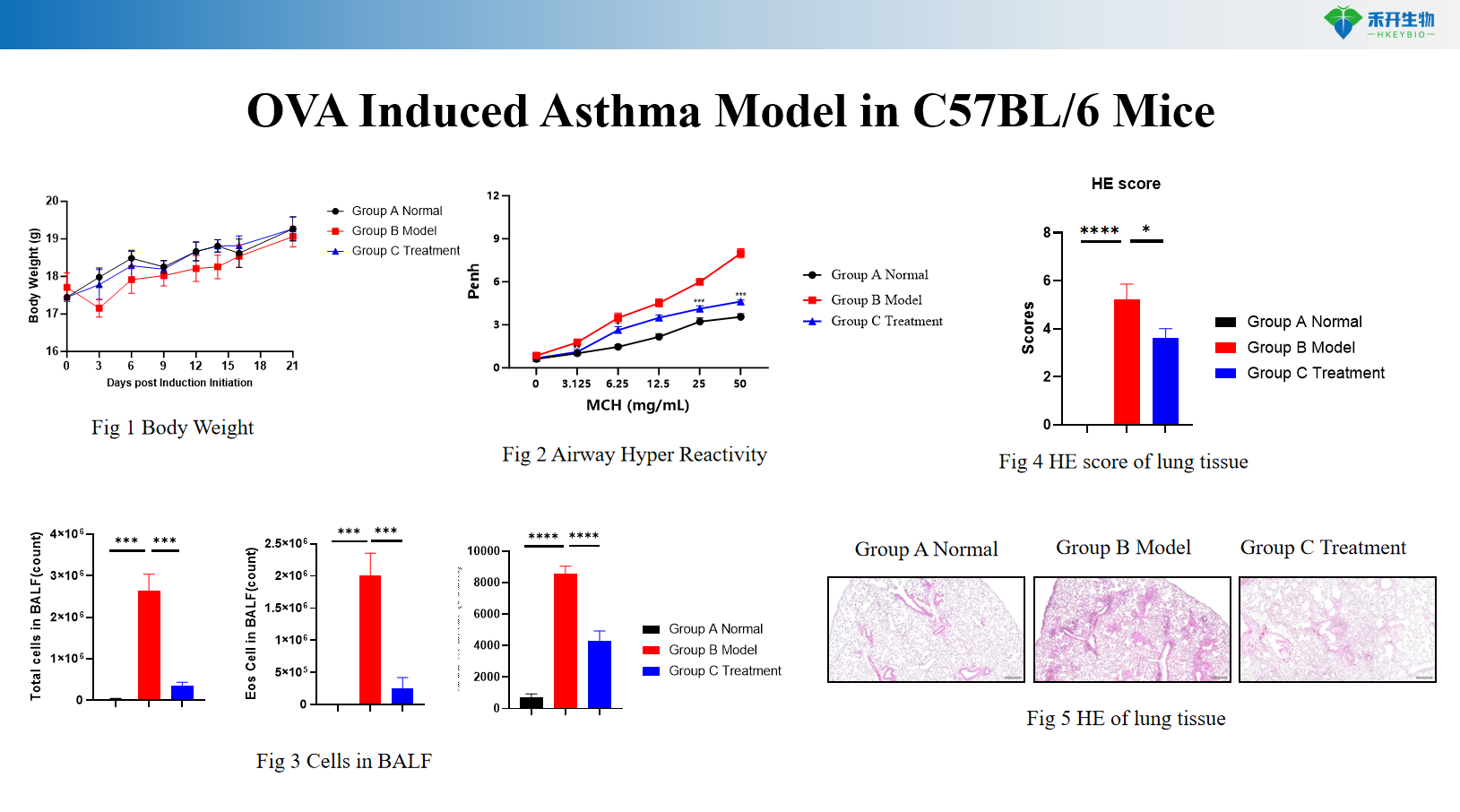
Mô hình bệnh hen suyễn do OVA gây ra ở chuột BALB/c
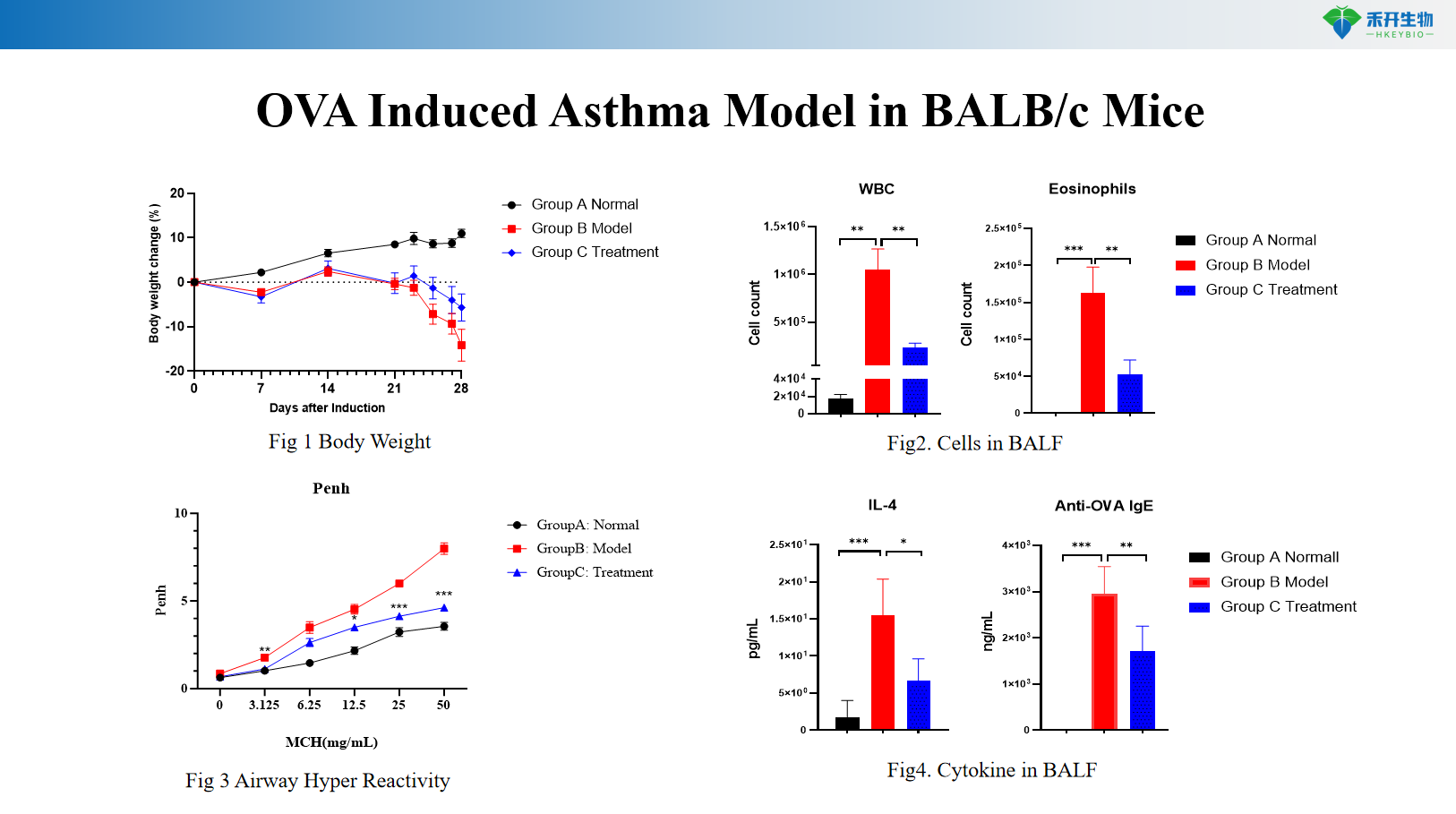
Mô hình bệnh hen suyễn do OVA gây ra ở chuột HIS
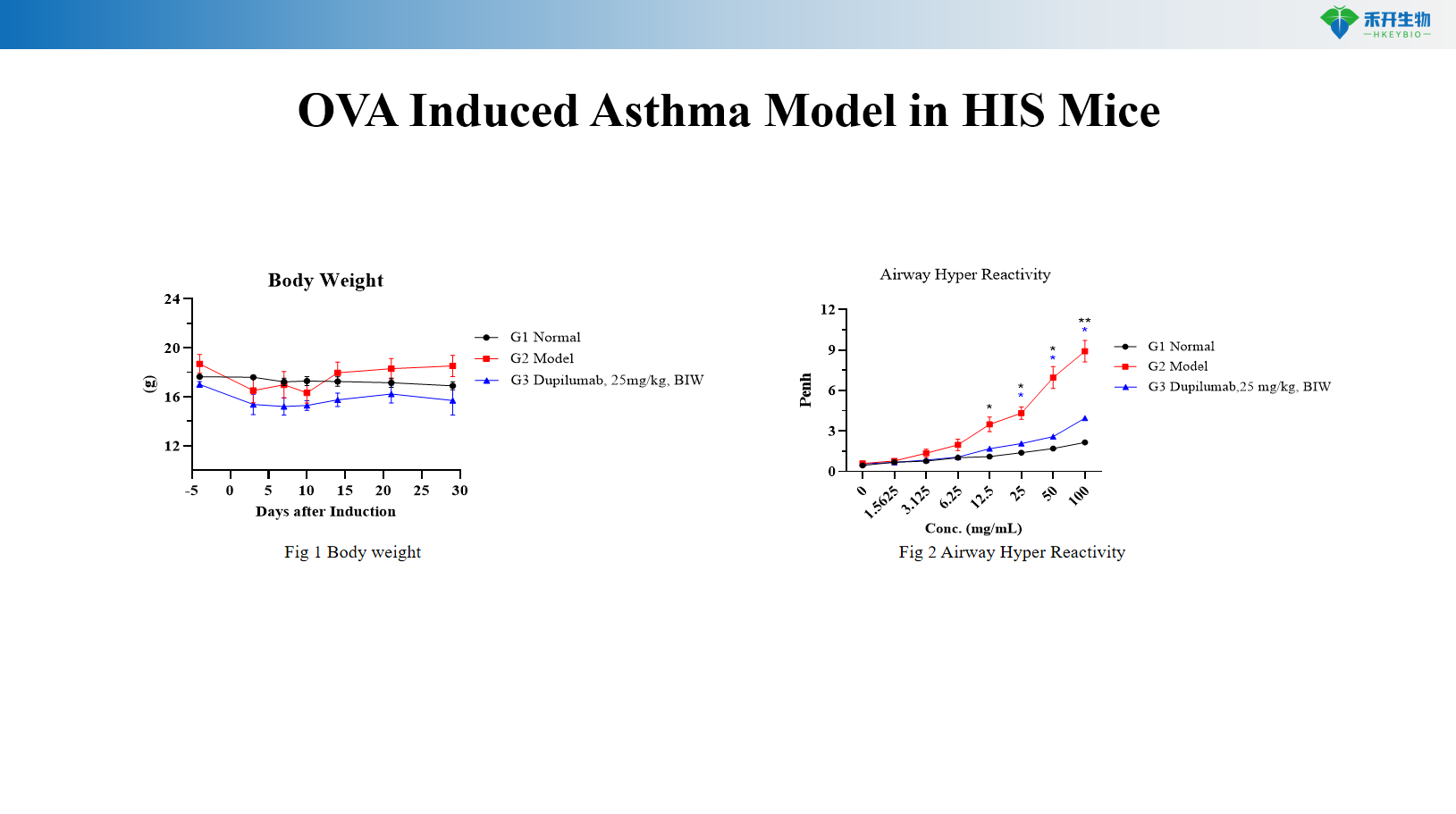
Mô hình bệnh hen suyễn gây ra OVA+MC903 ở chuột C57BL/6
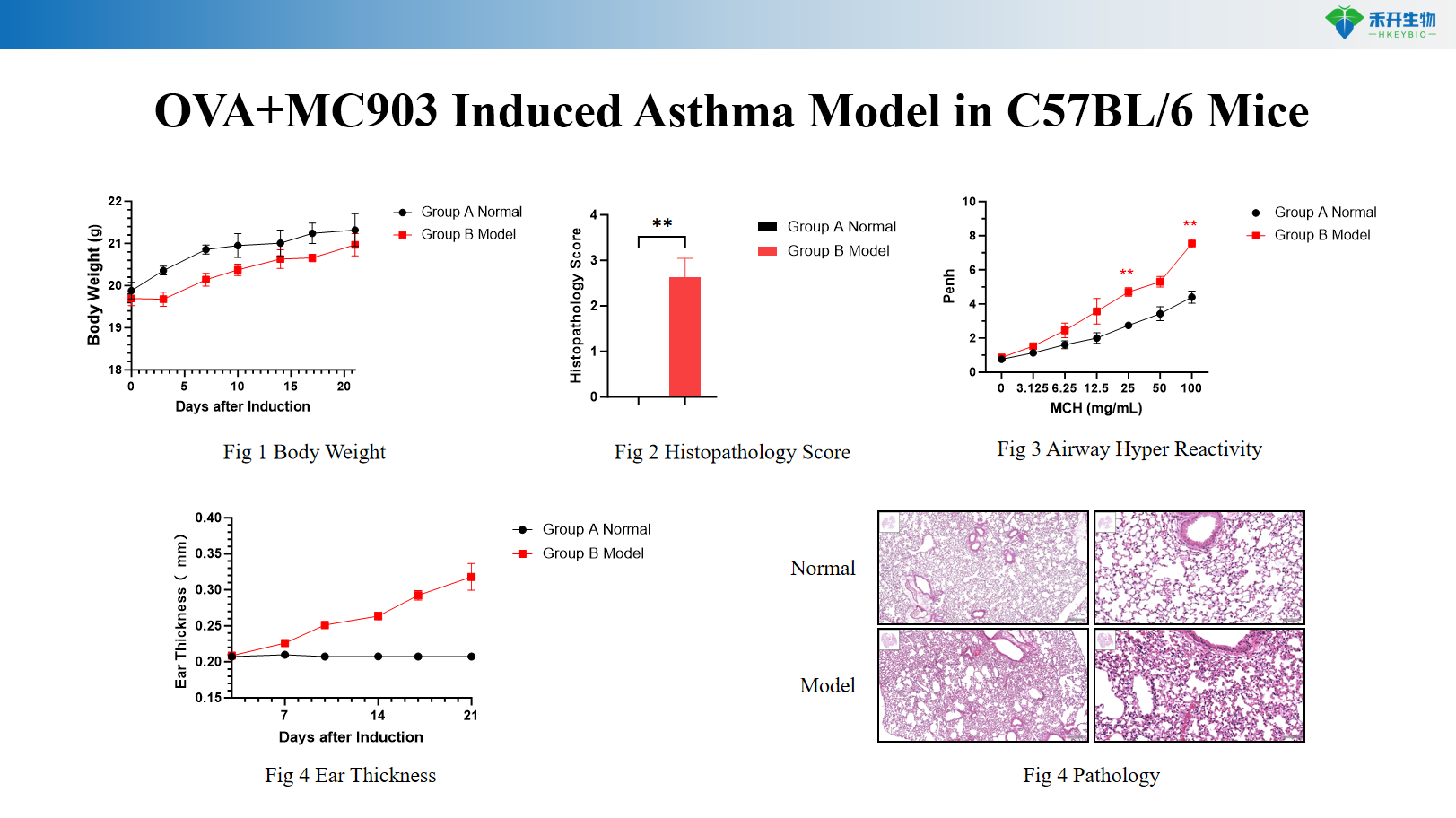
Mô hình bệnh hen suyễn bạch cầu trung tính gây ra OVA + LPS ở chuột C57BL/6
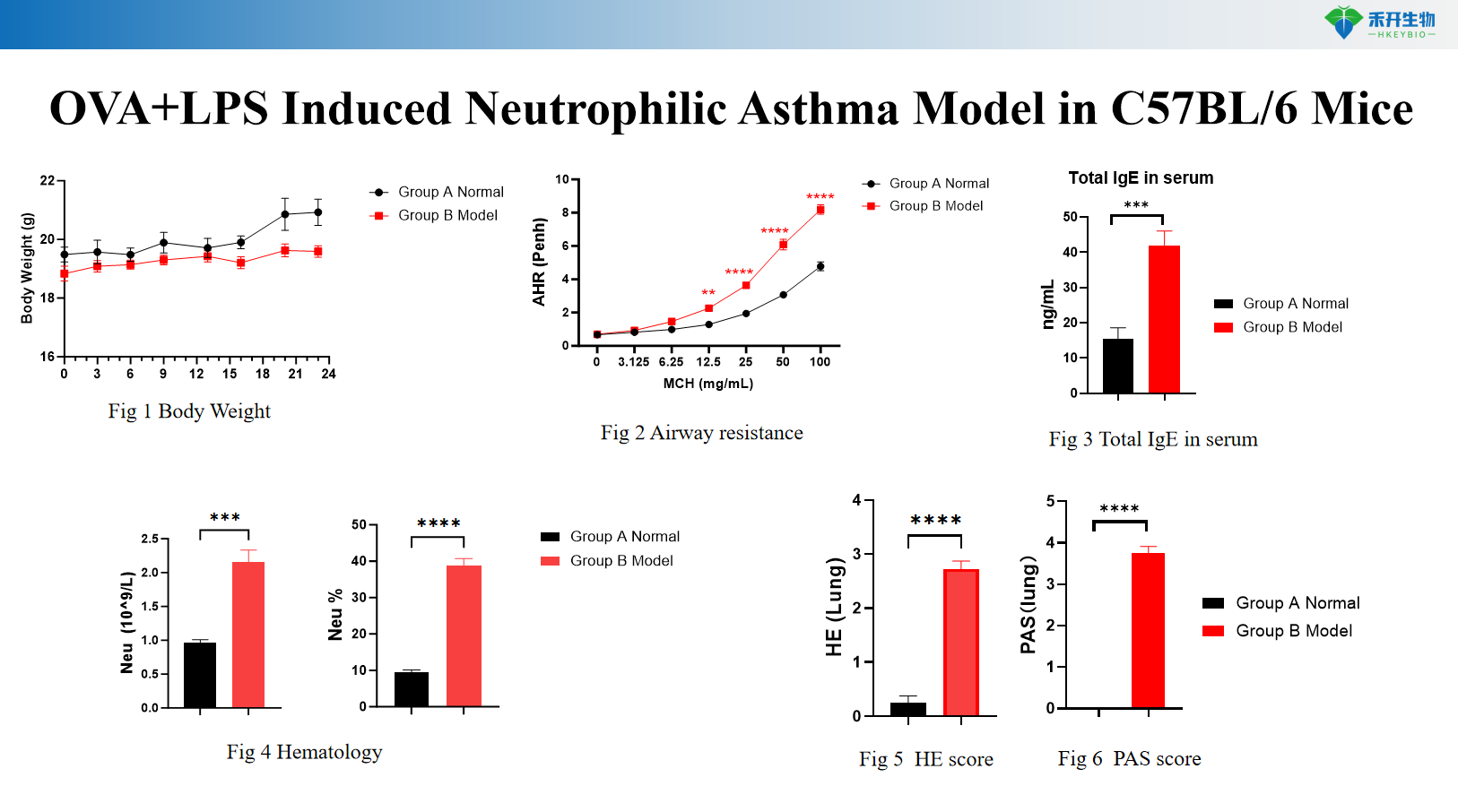
Mô hình bệnh hen suyễn do HDM ở chuột C57BL/6
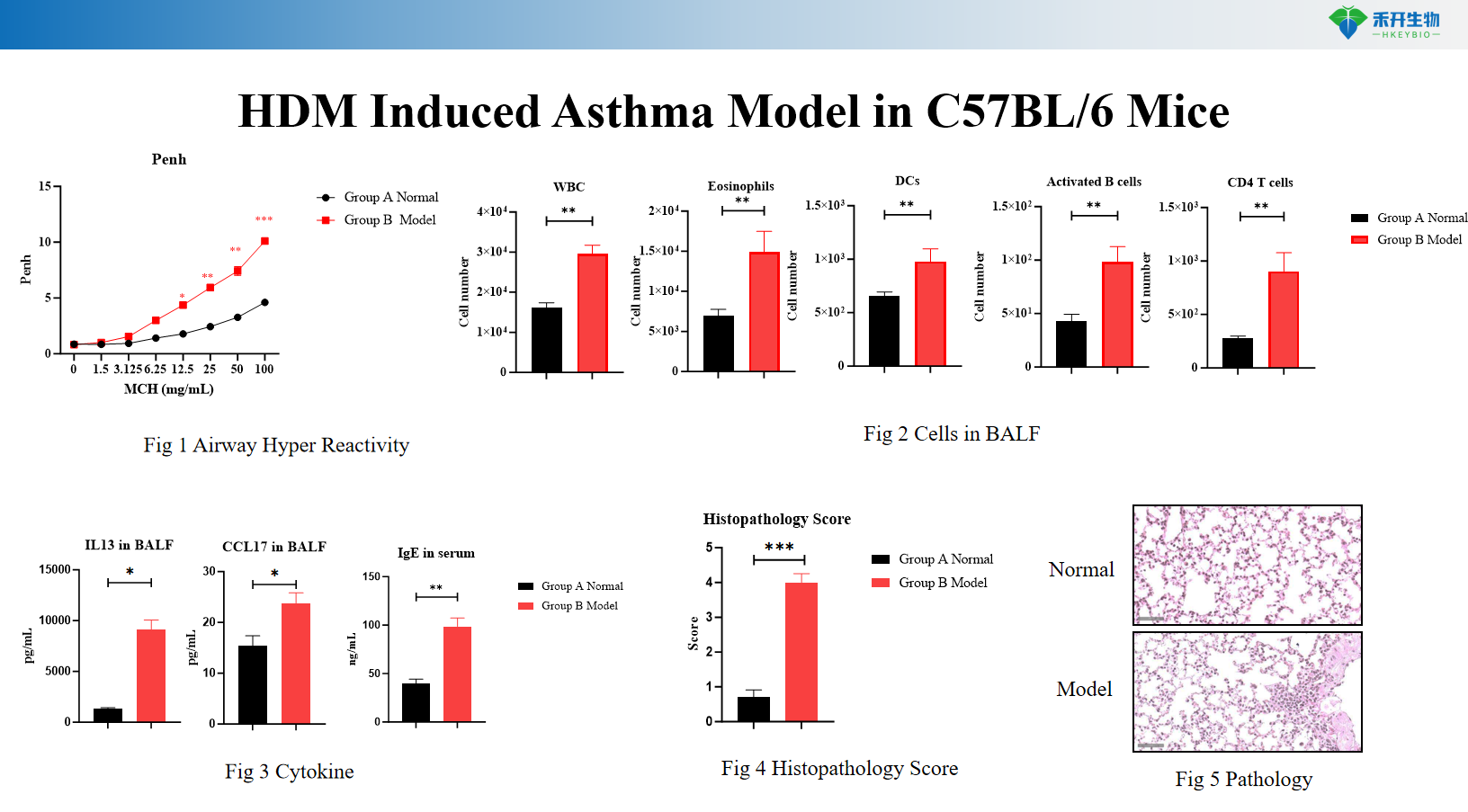
Mô hình bệnh hen suyễn do HDM ở chuột IL4/IL4R
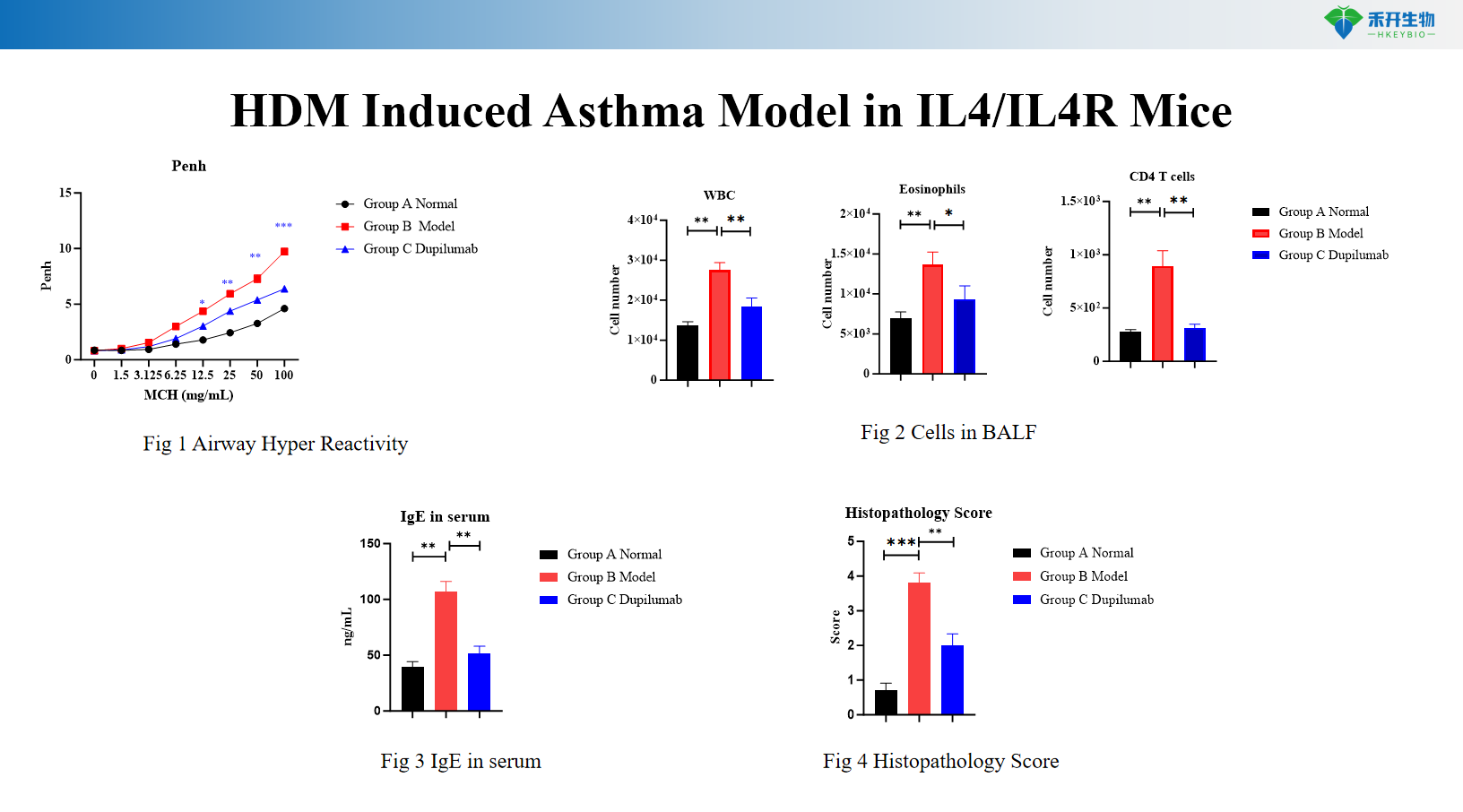
Mô hình bệnh hen suyễn do HDM+LPS ở chuột C57BL/6
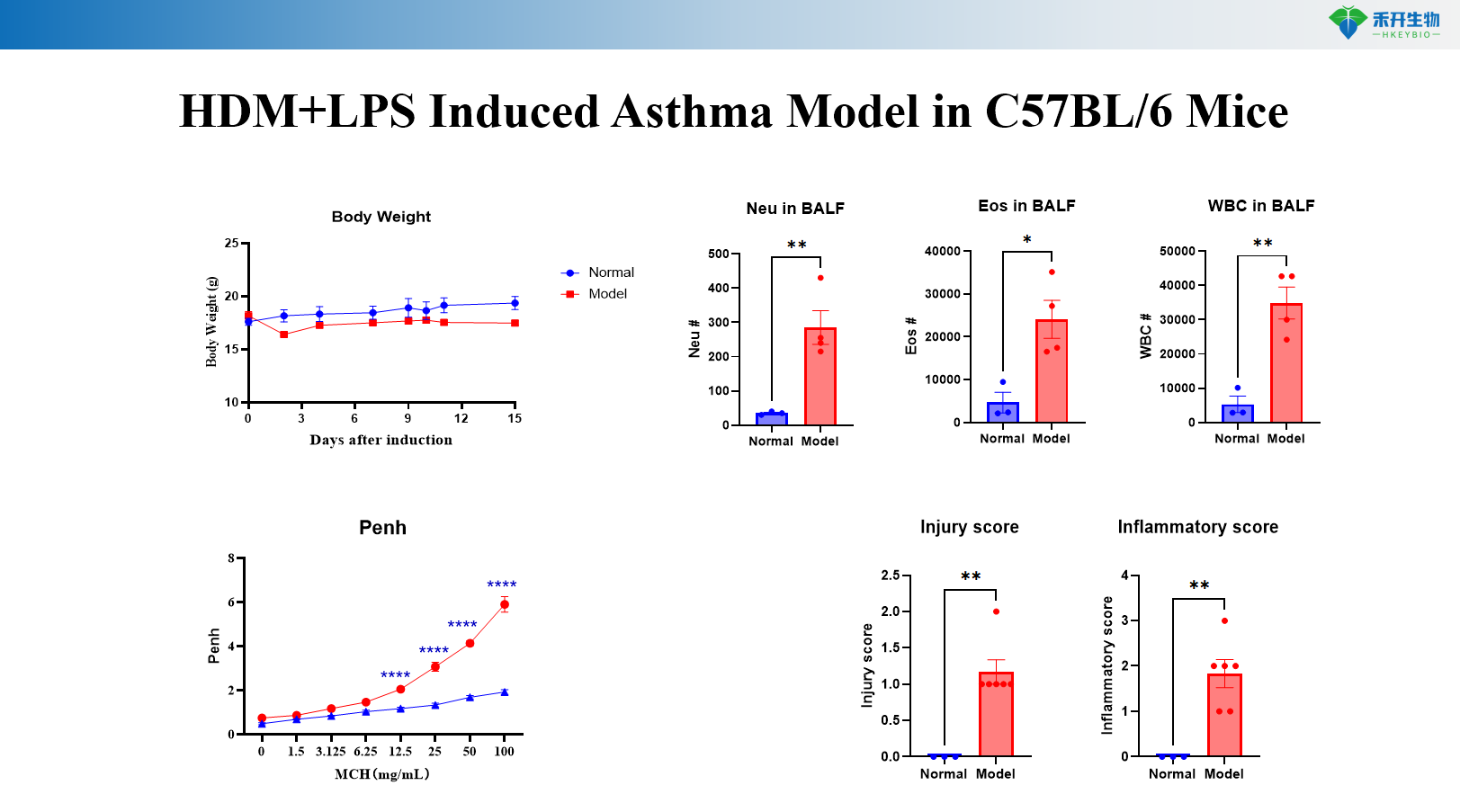
Mô hình bệnh hen suyễn do HDM+MC903 ở chuột C57BL/6

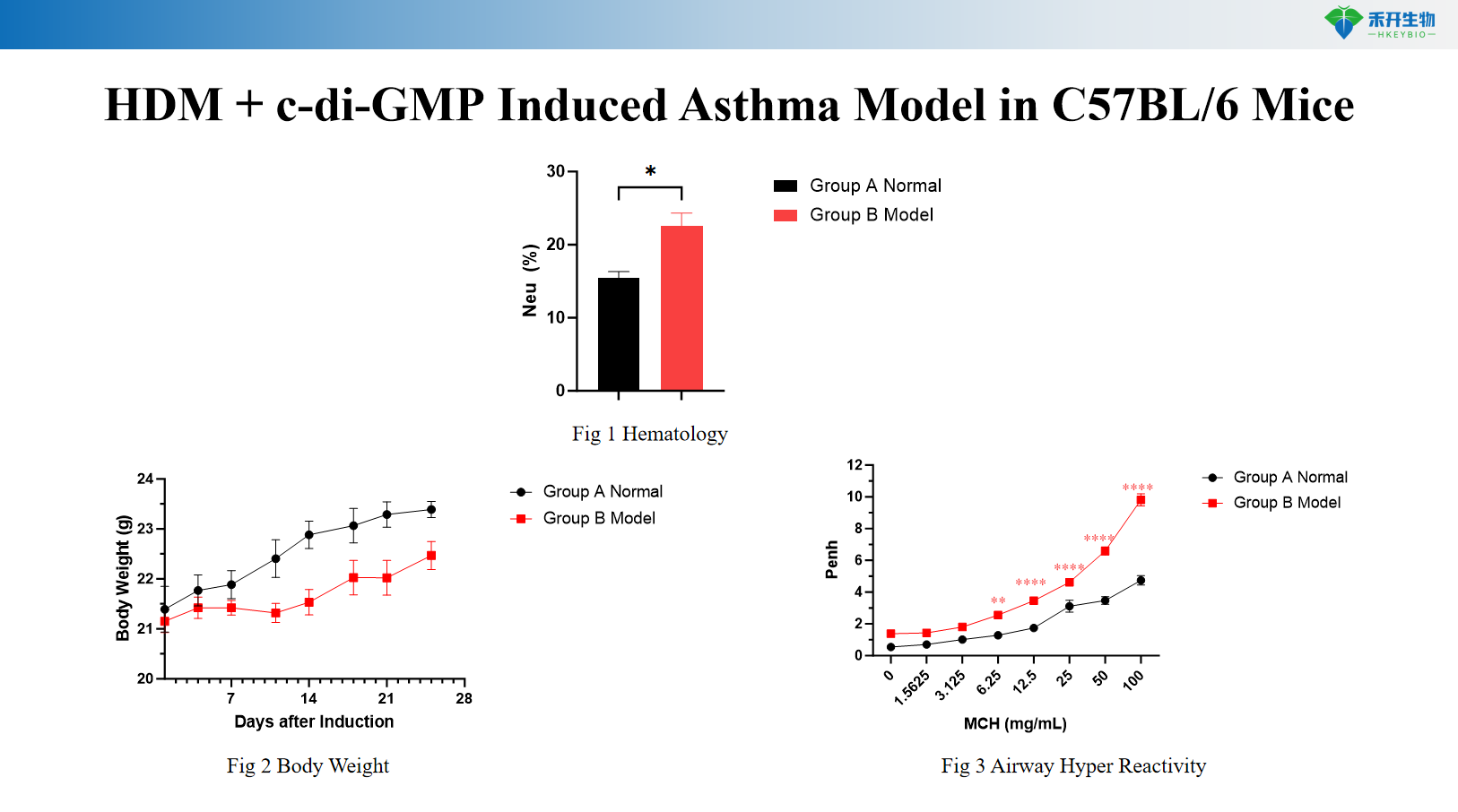
Mô hình bệnh hen suyễn do HDM + c-di-GMP ở chuột C57BL/6
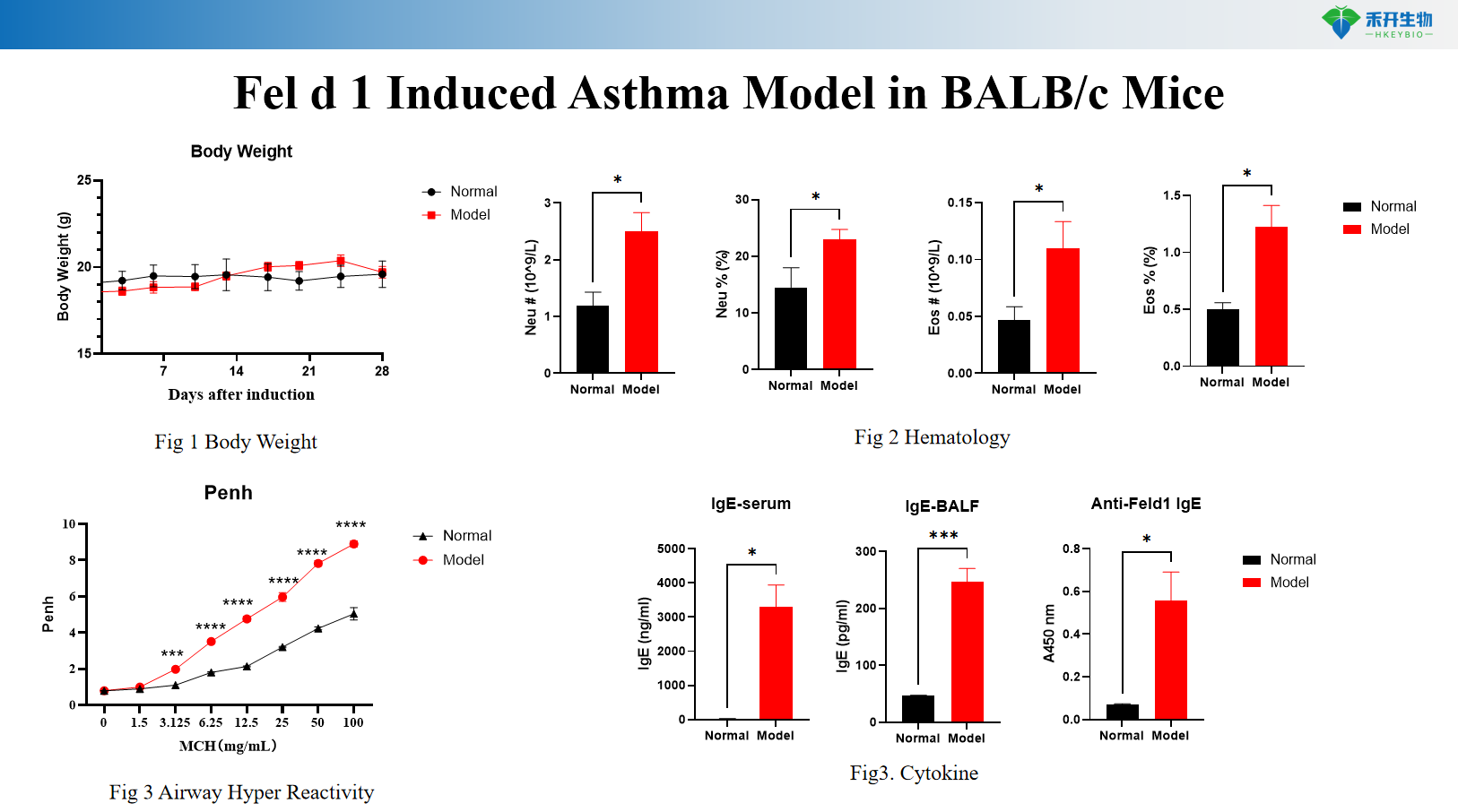
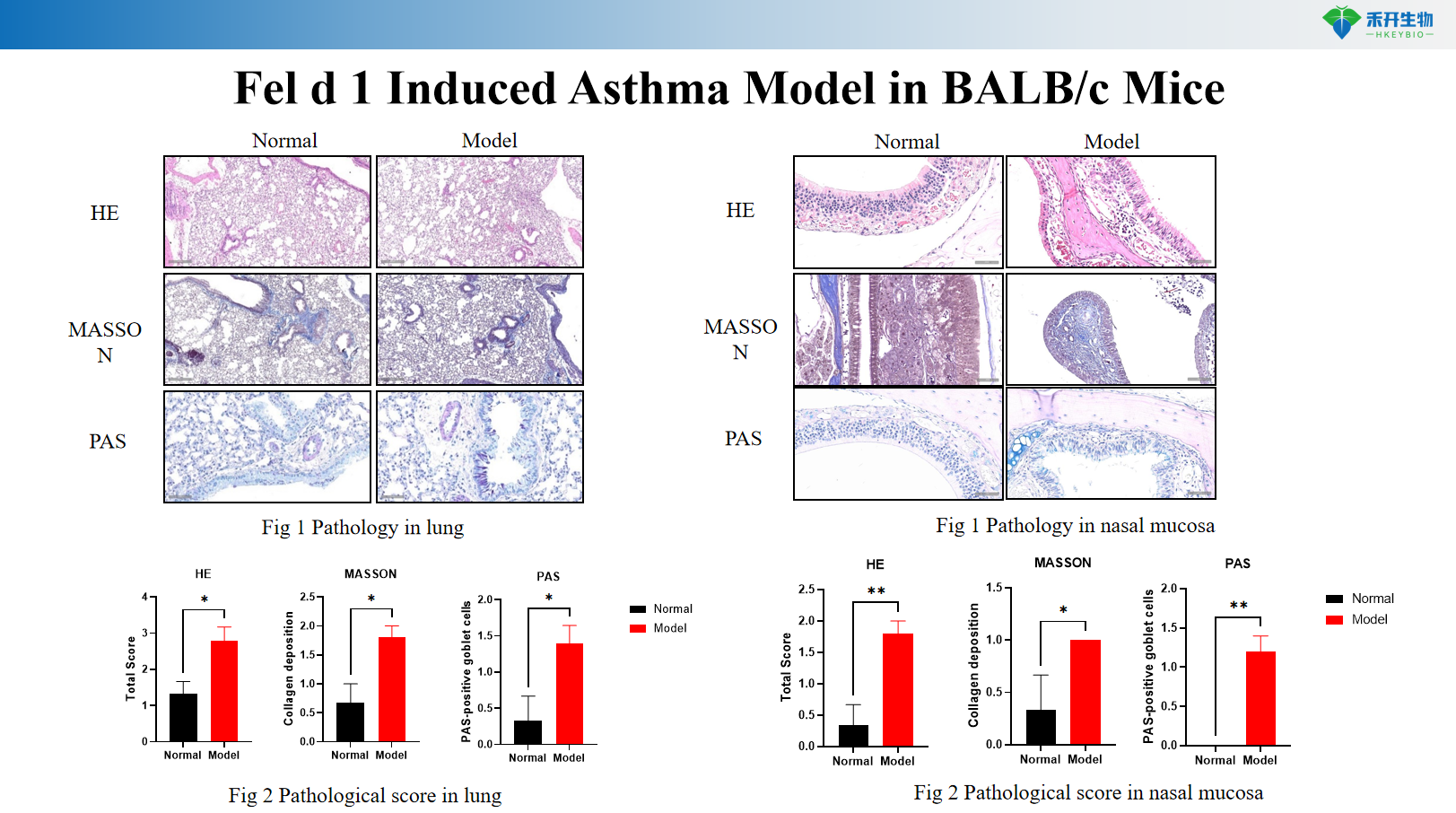
Fel d 1 Mô hình gây ra bệnh hen suyễn trên chuột BALB/c
• Thử nghiệm hiệu quả của chế phẩm sinh học (anti-IL-4Rα, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33)
• Đánh giá các chất ức chế phân tử nhỏ (chất ức chế JAK, chất ức chế PDE4, chất đối kháng CRTH2)
• Xác nhận mục tiêu cho các con đường của Th2, Th17 và cytokine có nguồn gốc từ biểu mô
• Phát hiện dấu ấn sinh học (IgE, dấu hiệu cytokine, dấu hiệu bạch cầu ái toan/bạch cầu trung tính)
• IND cho phép nghiên cứu dược lý và độc tính
tham số |
Thông số kỹ thuật |
Loài/Chủng |
C57BL/6, BALB/c, HIS được nhân hóa, chuyển gen IL4/IL4R |
Phương pháp cảm ứng |
OVA ± phèn ± MC903 ± LPS; HDM ± LPS ± MC903 ± c-di-GMP; Fel d 1 + phèn chua |
Thời gian học |
3–8 tuần (giai đoạn nhạy cảm + thử thách) |
Điểm cuối chính |
Trọng lượng cơ thể, AHR (xâm lấn/không xâm lấn), tế bào học BALF (bạch cầu ái toan, bạch cầu trung tính, đại thực bào), tổng IgE trong huyết thanh & IgE đặc hiệu với chất gây dị ứng, nồng độ cytokine (IL‑4, IL‑5, IL‑13, IL‑17, IFN‑γ), mô bệnh học phổi (HE, Masson, PAS) với tính điểm, huyết học (tùy chọn) |
| Kiểm soát tích cực | Dexamethasone hoặc kháng thể kháng IL-4Rα có sẵn dưới dạng hợp chất đối chiếu |
Gói dữ liệu |
Dữ liệu thô, báo cáo phân tích, số lượng tế bào BALF, kết quả ELISA, slide mô học, dữ liệu chức năng phổi, tin sinh học (tùy chọn) |
Hỏi: Làm cách nào để chọn mô hình AD phù hợp cho loại thuốc của tôi?
Đáp: Đối với bệnh hen suyễn tăng bạch cầu ái toan (Th2-cao), nên sử dụng mô hình OVA hoặc HDM ở BALB/c hoặc C57BL/6. Đối với bệnh hen suyễn tăng bạch cầu hạt trung tính hoặc hỗn hợp, mô hình OVA+LPS hoặc HDM+c-di-GMP trong C57BL/6 là phù hợp. Chuột được nhân bản hóa của HIS là lựa chọn lý tưởng để thử nghiệm các sản phẩm sinh học dành riêng cho con người. Chuột biến đổi gen IL4/IL4R thích hợp cho các nghiên cứu về con đường Th2. Nhóm khoa học của chúng tôi có thể hướng dẫn lựa chọn mô hình dựa trên mục tiêu cụ thể của bạn.
Hỏi: Sự khác biệt giữa mô hình cảm ứng OVA và HDM là gì?
Trả lời: OVA là một chất gây dị ứng mẫu cần có chất bổ trợ để gây mẫn cảm, tạo ra phản ứng Th2 mạnh mẽ. HDM là một chất gây dị ứng ở người có liên quan đến lâm sàng có chứa protease kích hoạt cả khả năng miễn dịch bẩm sinh và thích nghi, mô phỏng chặt chẽ hơn cơ chế bệnh sinh hen suyễn dị ứng ở người.
Câu hỏi: Những mô hình này có thể được sử dụng cho các nghiên cứu hỗ trợ IND không?
Đ: Vâng. Các nghiên cứu có thể được thực hiện theo các nguyên tắc GLP khi nộp hồ sơ quản lý (FDA, EMA).
Hỏi: Bạn có cung cấp các phác đồ nghiên cứu tùy chỉnh (ví dụ: lịch trình thử thách/nhạy cảm khác nhau, các liệu pháp kết hợp) không?
Đ: Chắc chắn rồi. Nhóm khoa học của chúng tôi điều chỉnh các phác đồ cảm ứng, lịch trình điều trị và phân tích điểm cuối cho phù hợp với loại thuốc cụ thể của bạn.
Hỏi: Thời gian điển hình cho một nghiên cứu hiệu quả thí điểm là gì?
Đáp: Hầu hết các mô hình hen suyễn đều được hoàn thành trong vòng 4–6 tuần, bao gồm xác định độ nhạy, thử thách, điều trị và phân tích điểm cuối.
