| Tilgjengelighet: | |
|---|---|
| Antall: | |











Bred modellportefølje – Allergen (OVA, HDM, Fel d 1), adjuvans-kombinert (LPS, c-di-GMP) og TSLP-drevne (MC903) modeller som dekker eosinofile, nøytrofile og blandede granulocytiske astmaendotyper.
Flere stammer – C57BL/6, BALB/c, HIS humaniserte og IL4/IL4R transgene mus tilgjengelig.
Omfattende endepunkter – Kroppsvekt, AHR (Penh, resistens), BALF-celletall (eosinofiler, nøytrofiler, makrofager), totalt serum-IgE og allergen-spesifikk IgE, cytokinprofilering (IL-4, IL-5, IL-13, IL-17), (PHE, Mahistoatology), (PHE, Mahistoatology, AS).
Translasjonsverdi – Ideell for testing av biologiske legemidler (anti-IL-4Ra, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33), JAK-hemmere, kortikosteroider og bronkodilatorer.
IND-klare datapakker – Studier kan utføres i samsvar med GLP-prinsipper.
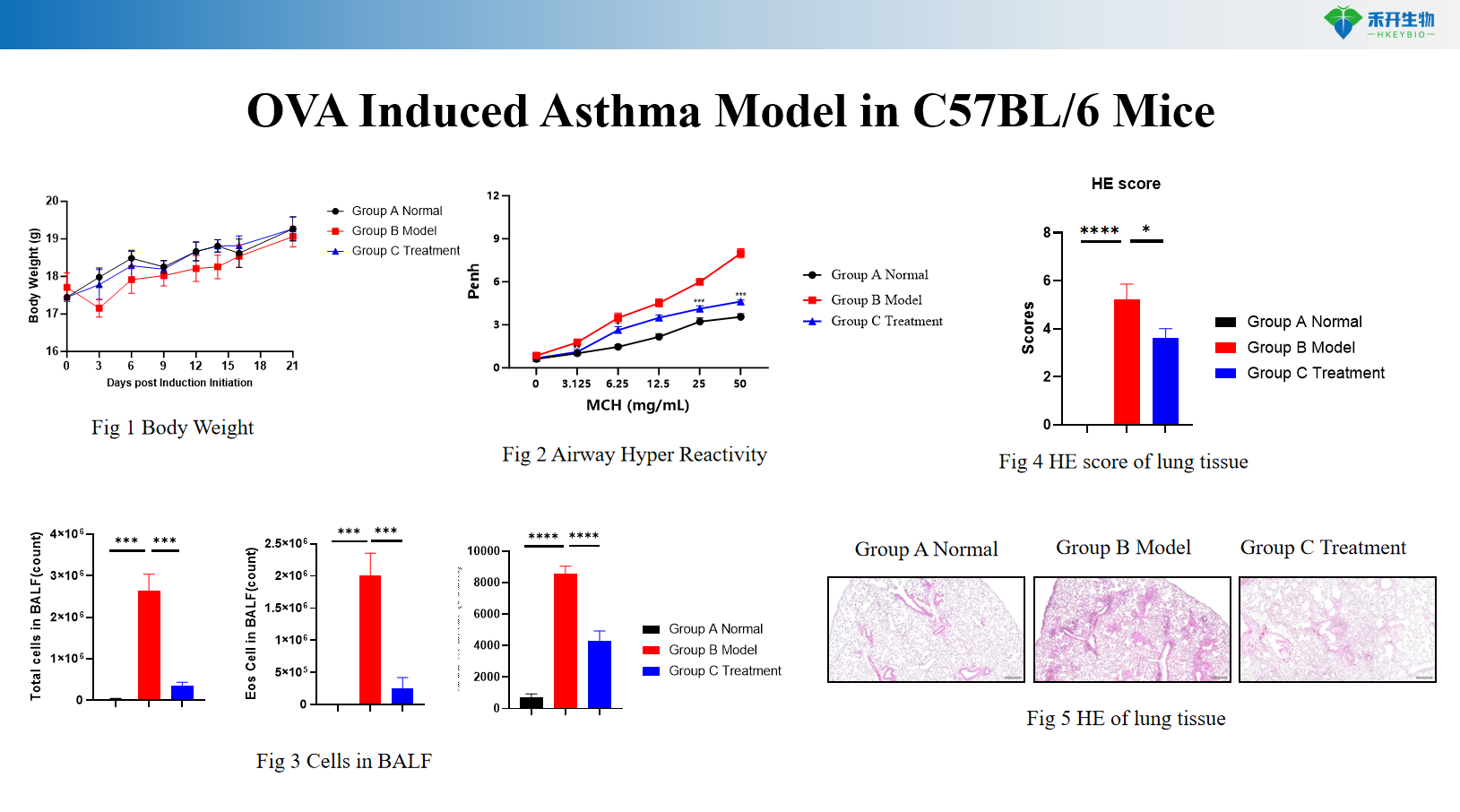
OVA-indusert astmamodell i C57BL/6-mus
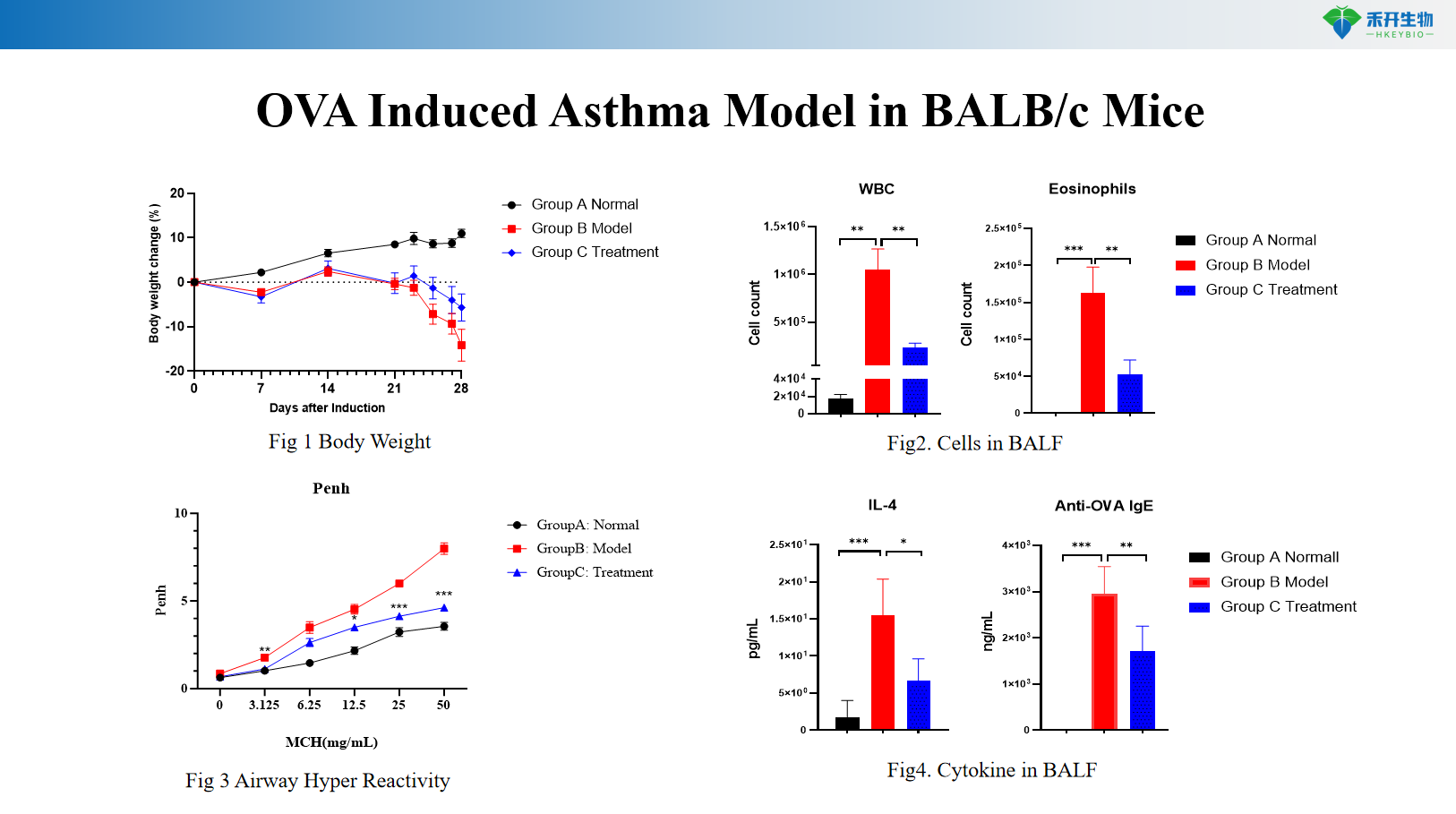
OVA-indusert astmamodell i BALB/c-mus
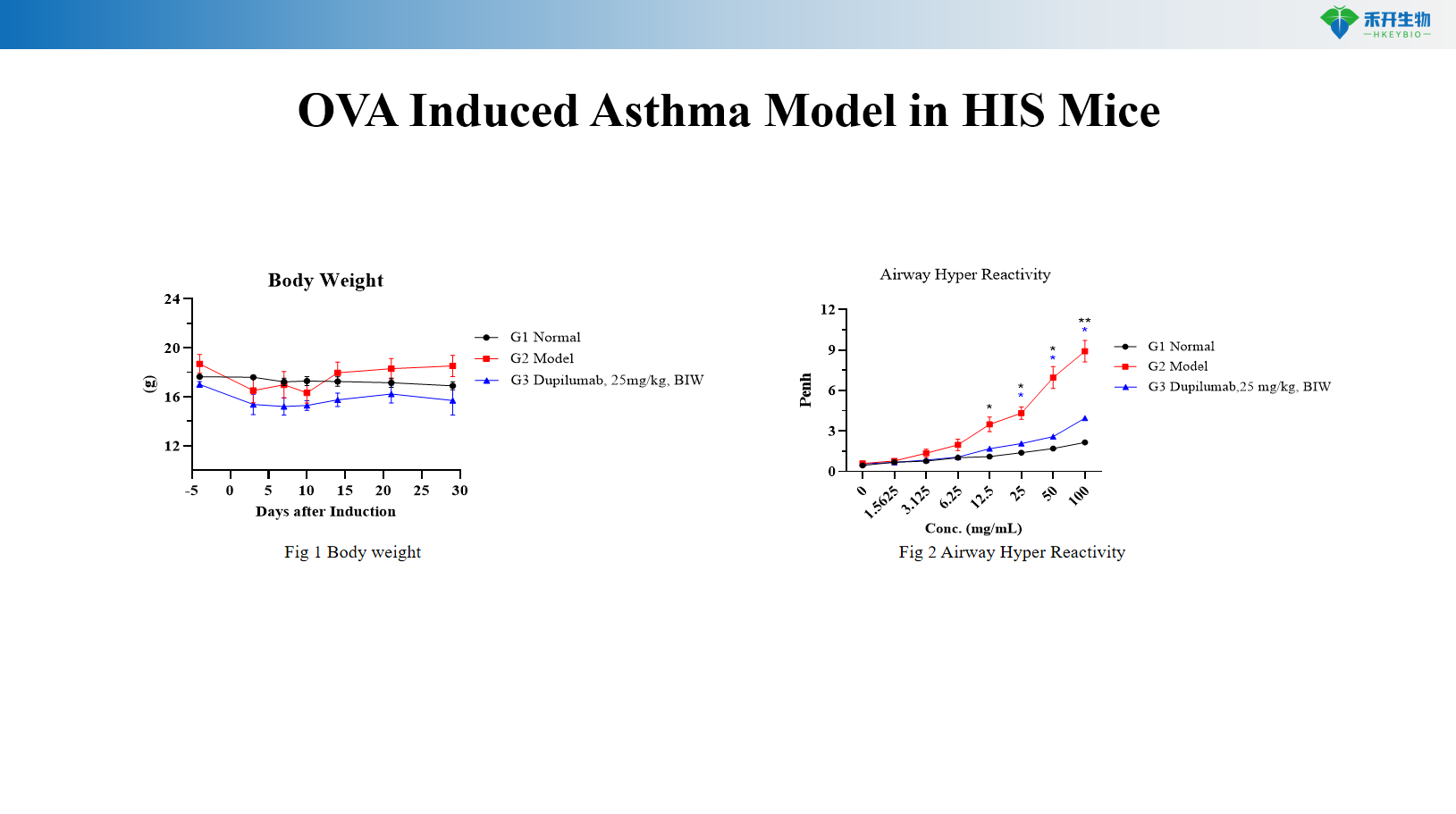
OVA-indusert astmamodell i HIS mus
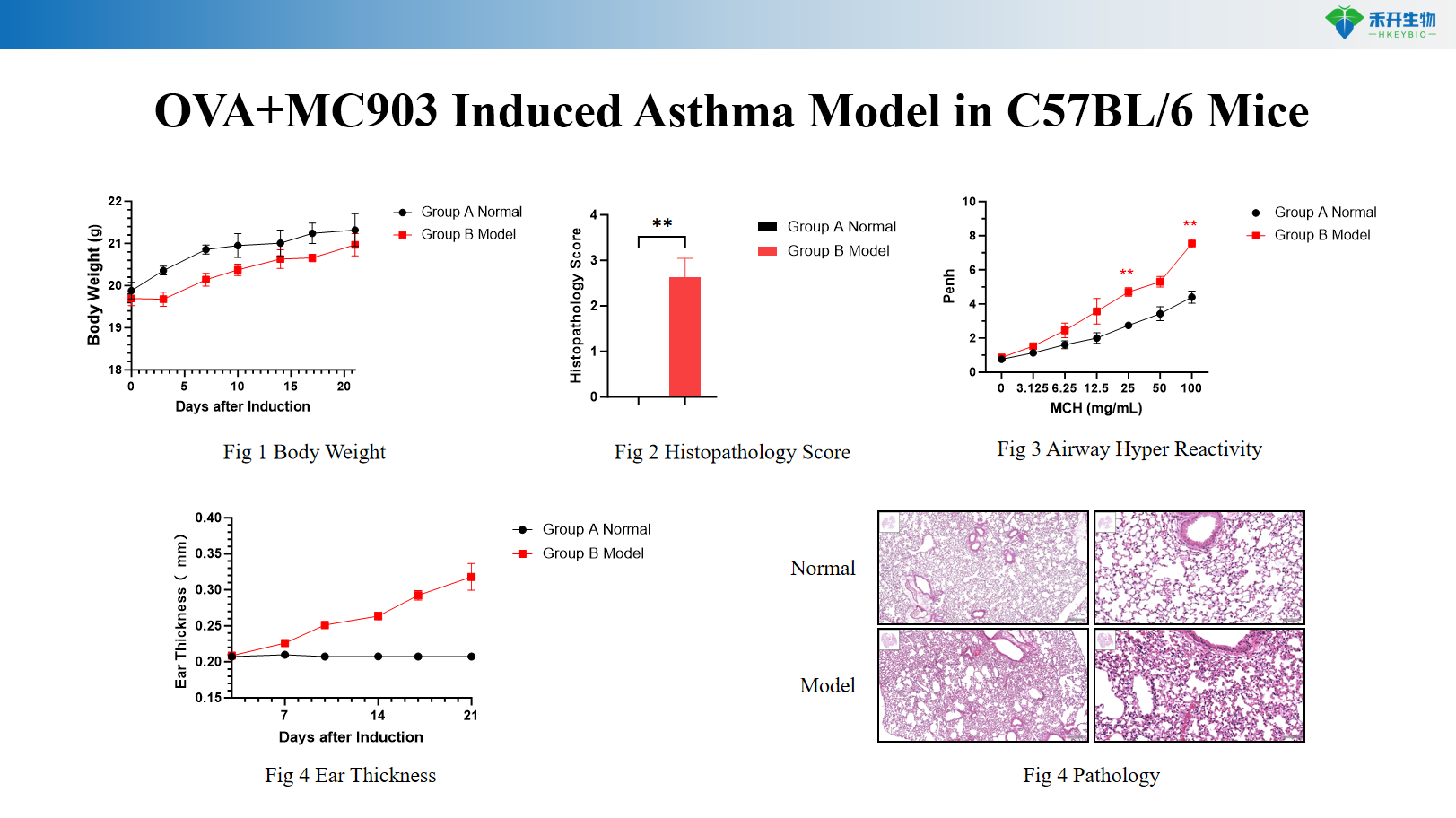
OVA+MC903-indusert astmamodell i C57BL/6-mus
OVA+LPS-indusert nøytrofil astmamodell i C57BL/6-mus
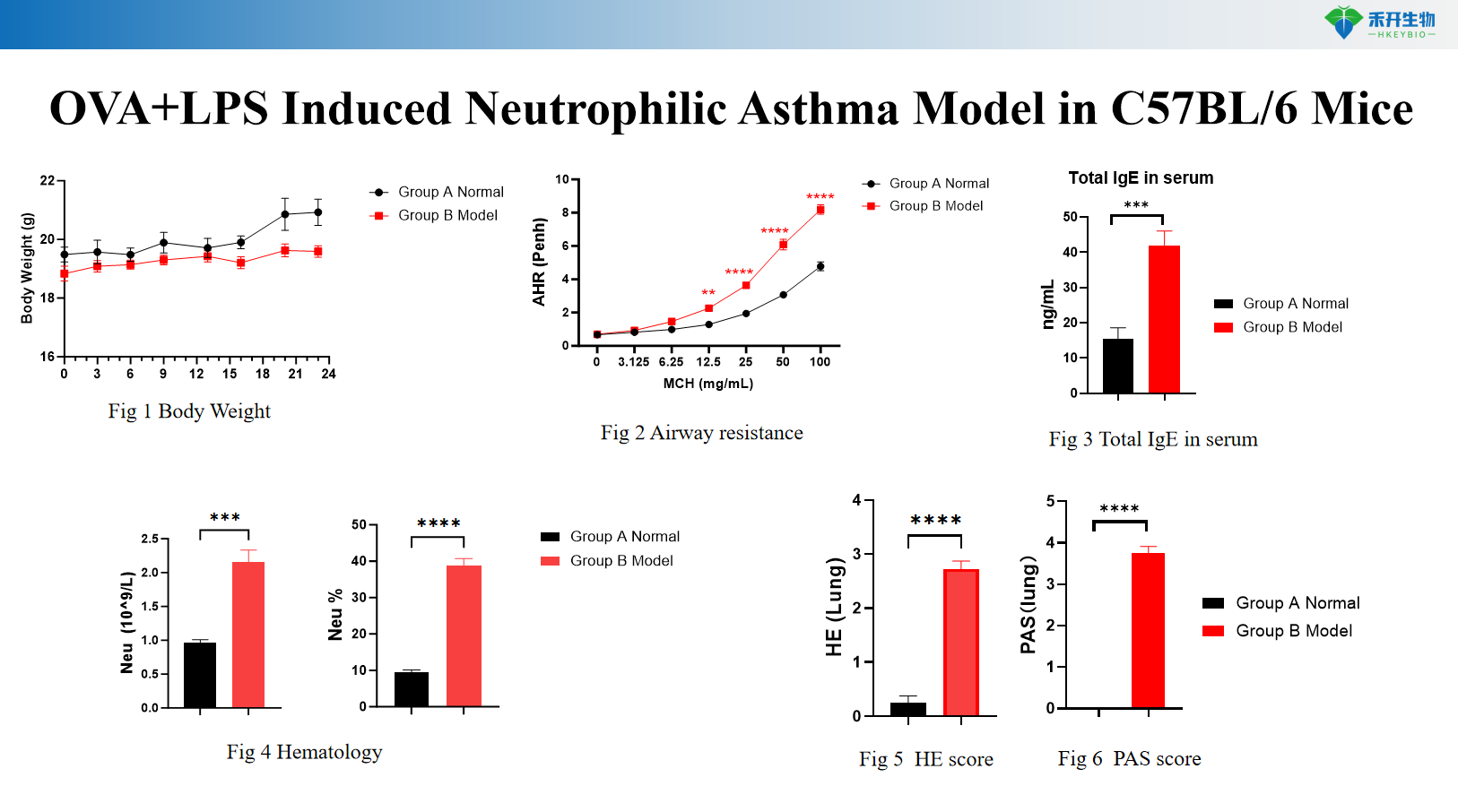
HDM-indusert astmamodell i C57BL/6-mus
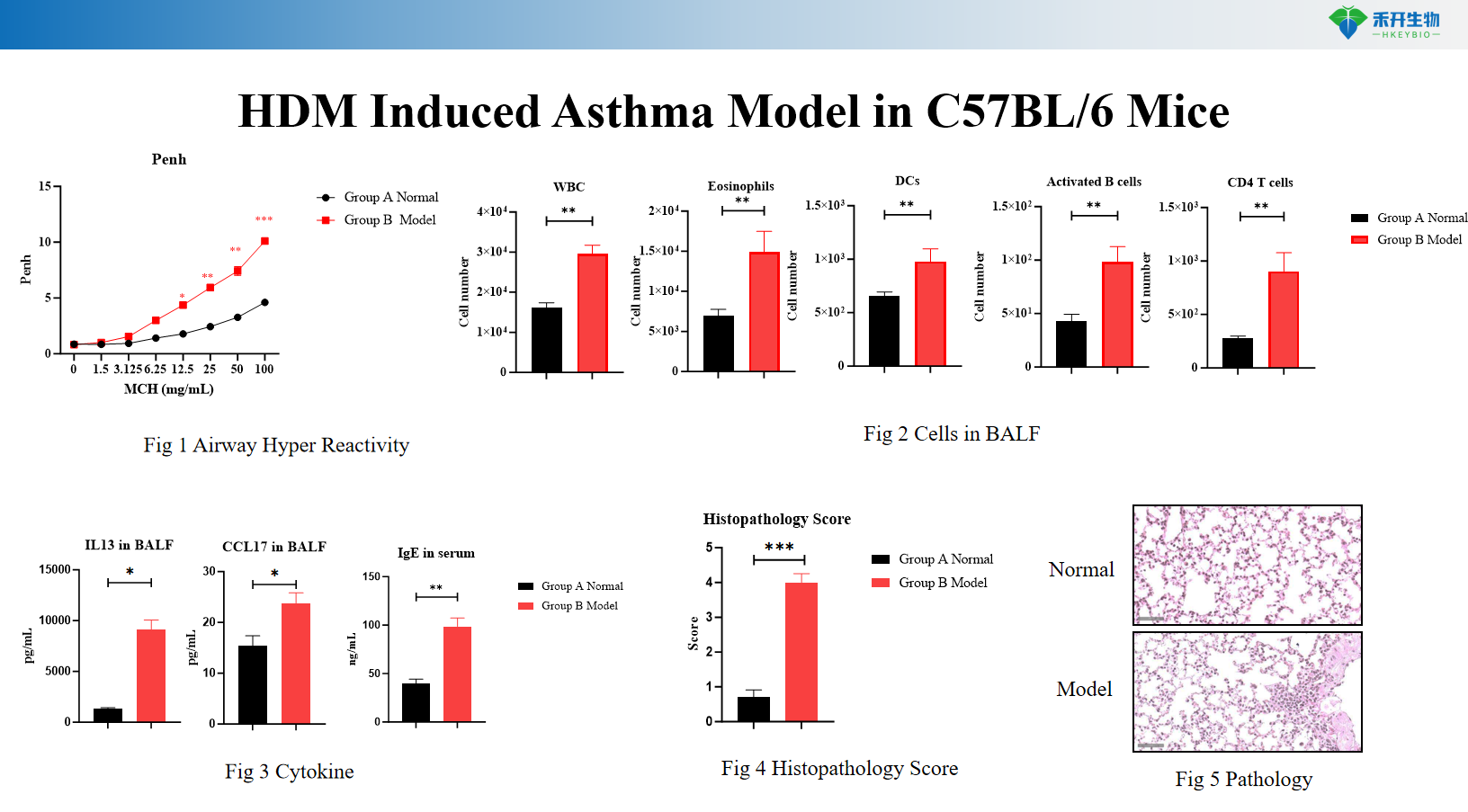
HDM-indusert astmamodell i IL4/IL4R-mus
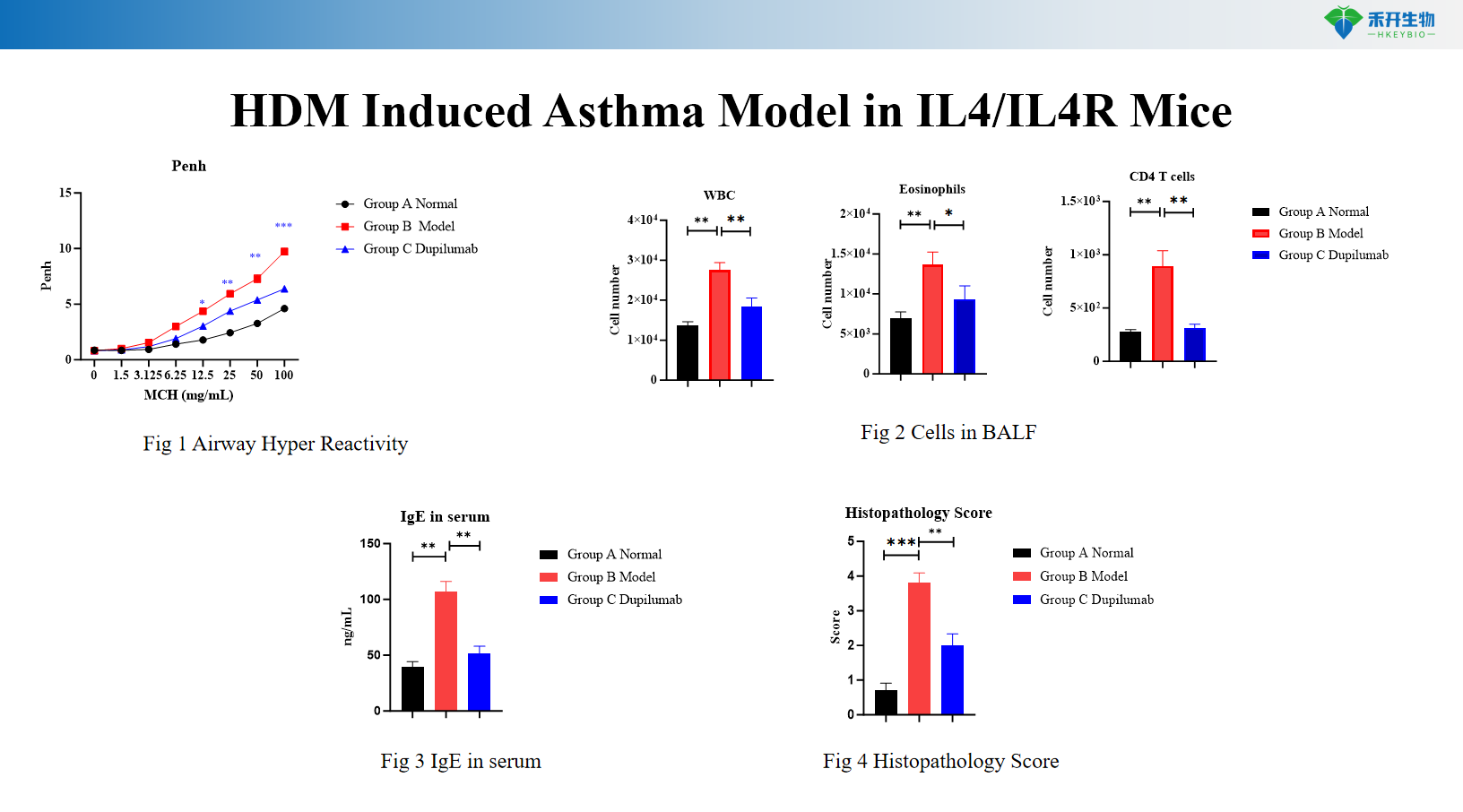
HDM+LPS-indusert astmamodell i C57BL/6-mus
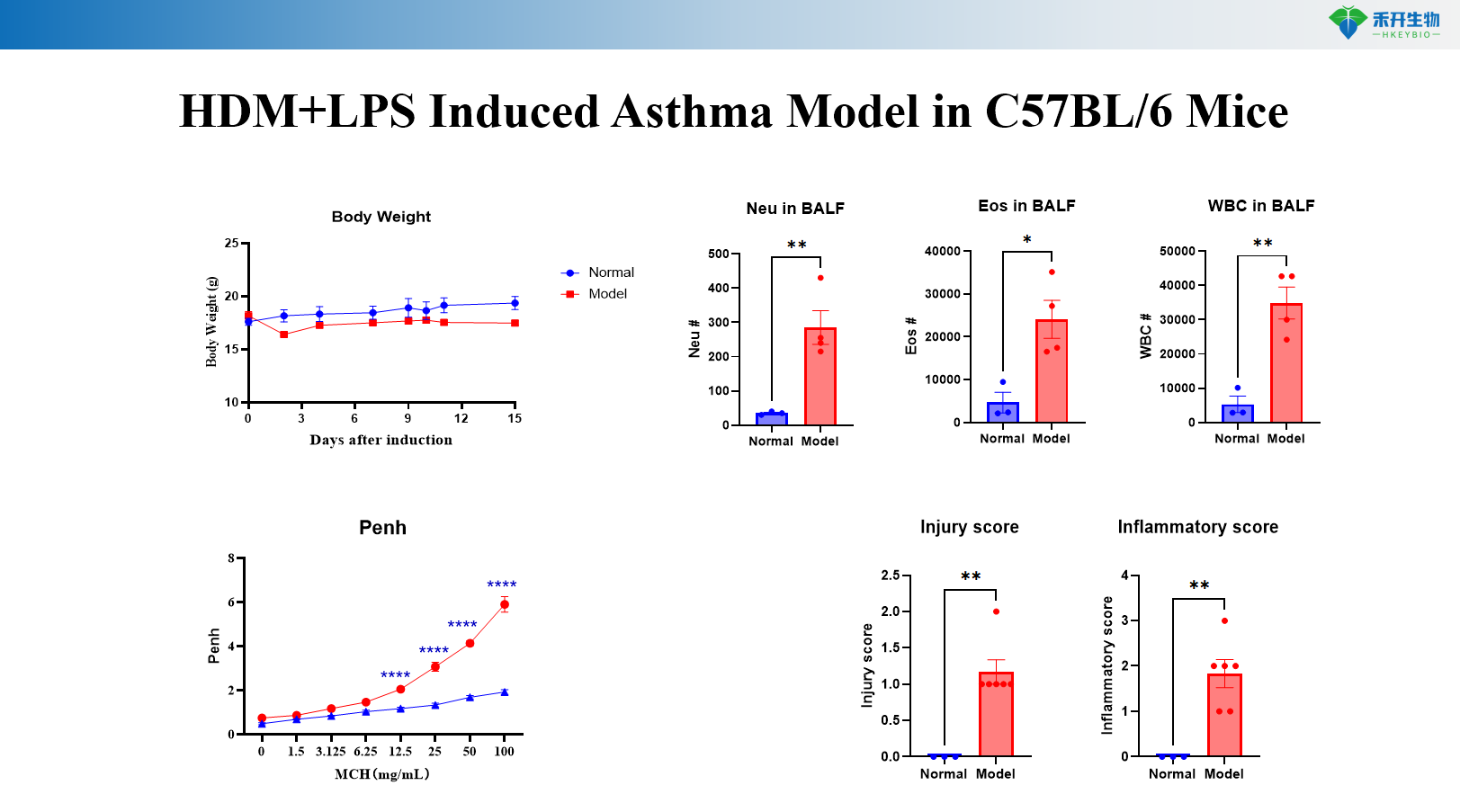
HDM+MC903-indusert astmamodell i C57BL/6-mus

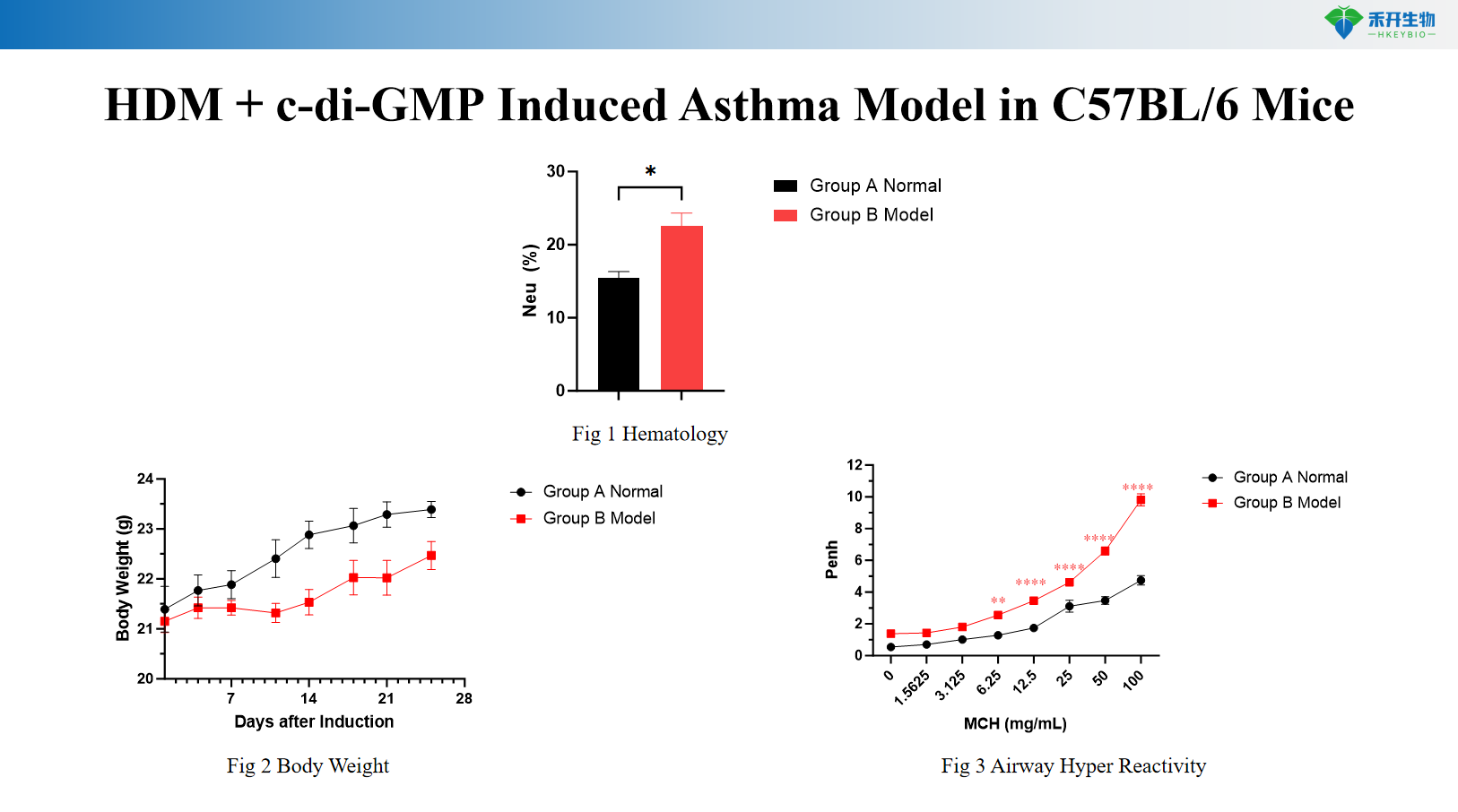
HDM + c-di-GMP-indusert astmamodell i C57BL/6-mus
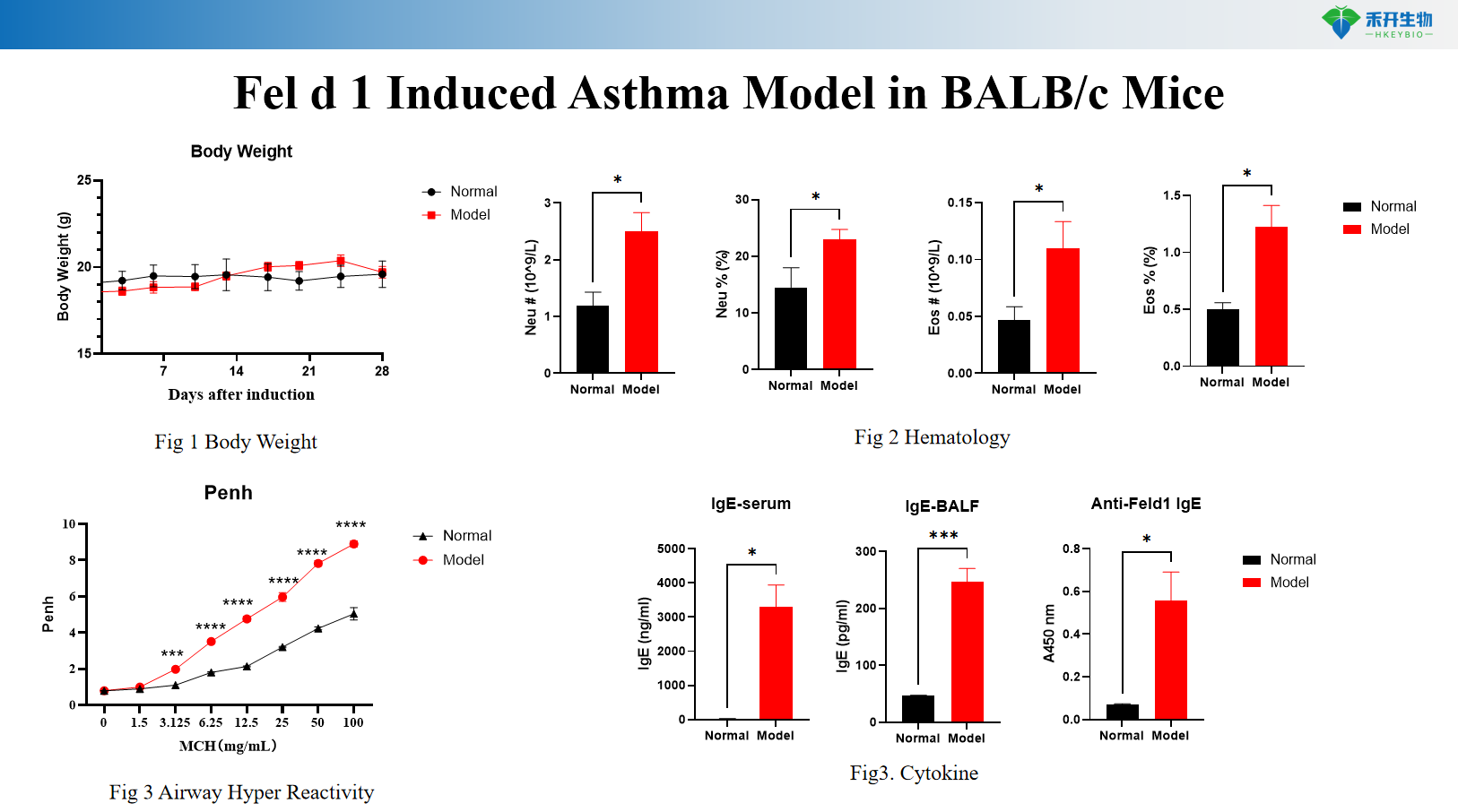
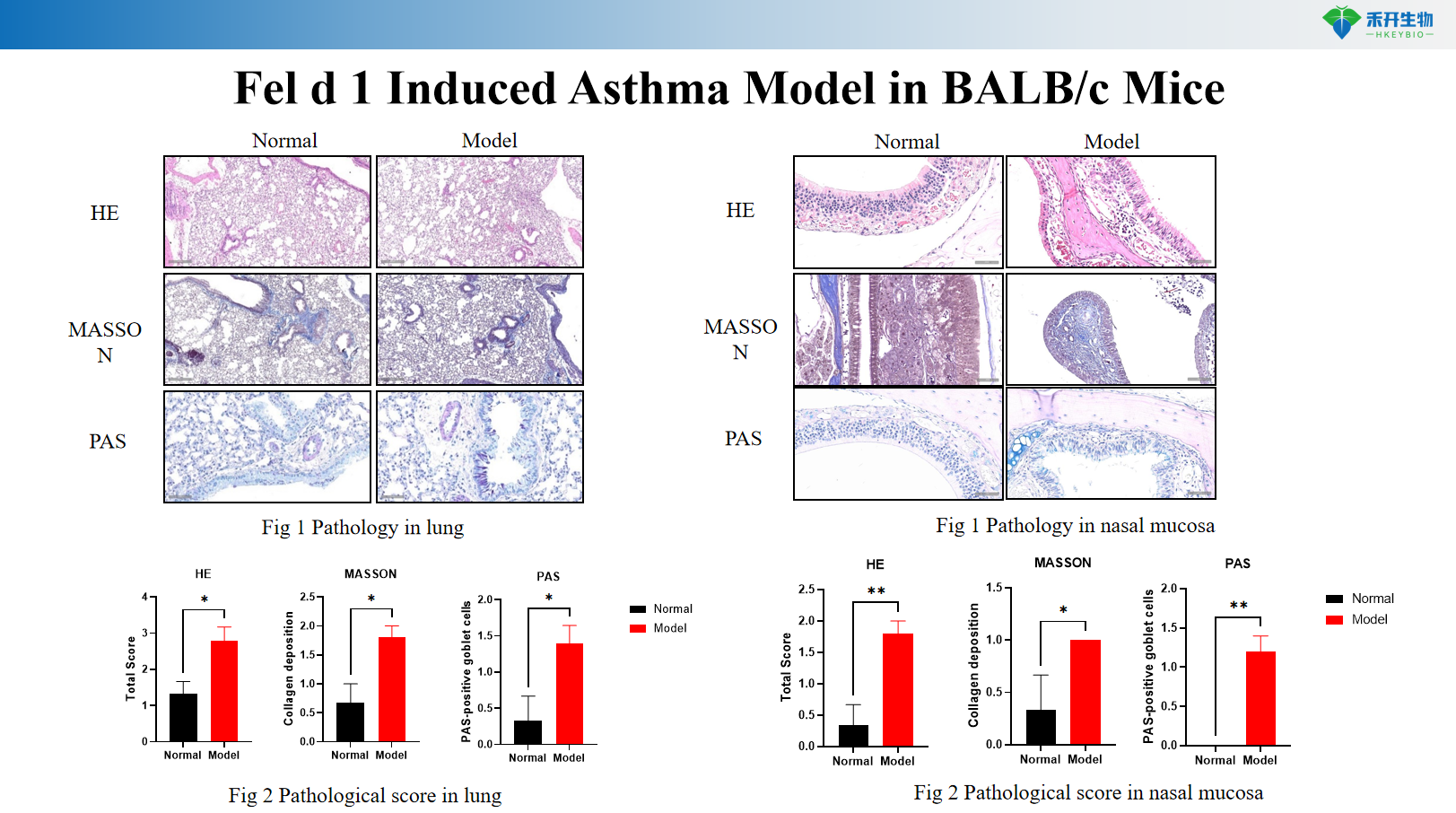
Fel d 1-indusert astmamodell i BALB/c-mus
• Effekttesting av biologiske legemidler (anti-IL-4Ra, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33)
• Evaluering av småmolekylære inhibitorer (JAK-hemmere, PDE4-hemmere, CRTH2-antagonister)
• Målvalidering for Th2, Th17 og epitelavledede cytokinveier
• Biomarkørfunn (IgE, cytokinsignaturer, eosinofile/nøytrofile markører)
• IND-aktiverende farmakologi og toksikologistudier
Parameter |
Spesifikasjoner |
Arter/Stamme |
C57BL/6, BALB/c, HIS humanisert, IL4/IL4R transgen |
Induksjonsmetode |
OVA ± alun ± MC903 ± LPS; HDM ± LPS ± MC903 ± c‑di‑GMP; Fel d 1 + alun |
Studievarighet |
3–8 uker (sensibilisering + utfordringsfaser) |
Viktige endepunkter |
Kroppsvekt, AHR (invasiv/ikke-invasiv), BALF-cytologi (eosinofiler, nøytrofiler, makrofager), totalt serum-IgE og allergen-spesifikk IgE, cytokinnivåer (IL-4, IL-5, IL-13, IL-17, γ-patologi), P-lunge, IFNAS, lunge-patologi, IFNAS) scoring, hematologi (valgfritt) |
| Positiv kontroll | Deksametason eller anti-IL-4Ra-antistoff tilgjengelig som referanseforbindelser |
Datapakke |
Rådata, analyserapporter, BALF-celletall, ELISA-resultater, histologiske lysbilder, lungefunksjonsdata, bioinformatikk (valgfritt) |
Spørsmål: Hvordan velger jeg riktig AD-modell for legemiddelkandidaten min?
A: For eosinofil (Th2-høy) astma anbefales OVA- eller HDM-modeller i BALB/c eller C57BL/6. For nøytrofil eller blandet granulocytisk astma er OVA+LPS- eller HDM+c-di-GMP-modeller i C57BL/6 passende. HIS humaniserte mus er ideelle for å teste menneskespesifikke biologiske stoffer. IL4/IL4R transgene mus er egnet for Th2 pathway-studier. Vårt vitenskapelige team kan veilede modellvalg basert på ditt spesifikke mål.
Spørsmål: Hva er forskjellen mellom OVA- og HDM-induserte modeller?
A: OVA er et modellallergen som krever adjuvans for sensibilisering, og produserer robuste Th2-responser. HDM er et klinisk relevant humant allergen som inneholder proteaser som aktiverer både medfødt og adaptiv immunitet, som i større grad etterligner human allergisk astmapatogenese.
Spørsmål: Kan disse modellene brukes til IND-aktiverende studier?
A: Ja. Studier kan utføres i samsvar med GLP-prinsipper for regulatoriske innleveringer (FDA, EMA).
Spørsmål: Tilbyr du tilpassede studieprotokoller (f.eks. ulike sensibiliserings-/utfordringsplaner, kombinasjonsterapier)?
A: Absolutt. Vårt vitenskapelige team skreddersyr induksjonsprotokoller, behandlingsplaner og endepunktsanalyser til din spesifikke legemiddelkandidat.
Spørsmål: Hva er den typiske tidslinjen for en piloteffektstudie?
A: De fleste astmamodeller fullføres innen 4–6 uker, inkludert sensibilisering, utfordring, behandling og endepunktsanalyse.
