| Disponibilità: | |
|---|---|
| Quantità: | |











Clinicamente rilevante – Panoramica dell’uveite autoimmune umana con infiammazione mediata da Th1/Th17, danno retinico e rottura della barriera emato-retinica.
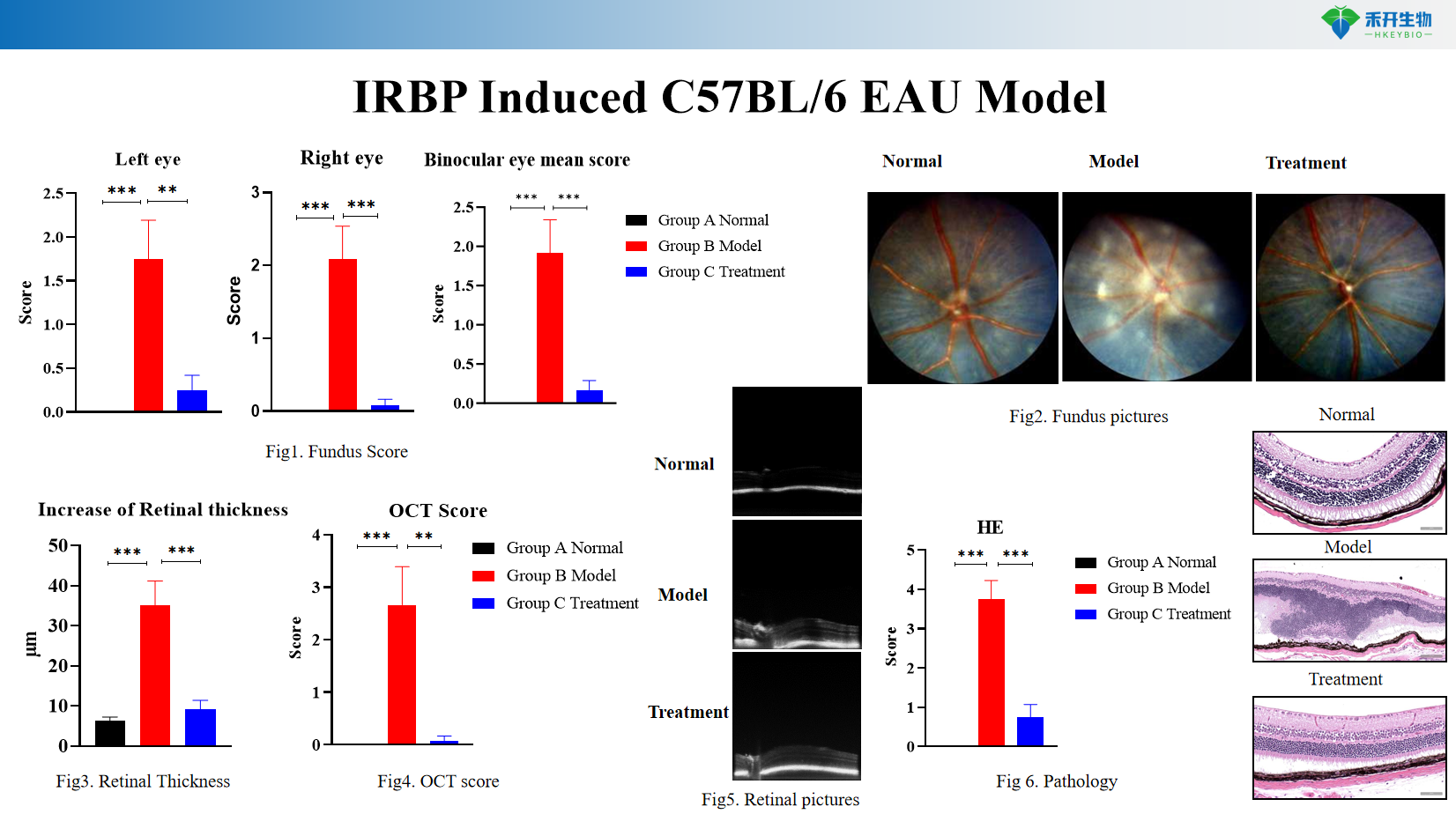
Endpoint di imaging avanzati : fotografia e punteggio del fondo oculare, tomografia a coerenza ottica (OCT) per la misurazione dello spessore della retina.
Patologia completa – Istopatologia (colorazione HE) dell'infiltrato infiammatorio e del danno strutturale della retina.
Guidato meccanicamente – L’IRBP attiva le cellule presentanti l’antigene, guidando la differenziazione Th1 e Th17 e la produzione di citochine infiammatorie (IFN-γ, IL-17, TNF-α).
IND Ready Packet – La ricerca può essere condotta in conformità con i principi GLP.
Modello IRBP Inducibile C57BL/6 EAU
• Testare l'efficacia degli immunomodulatori (corticosteroidi, metotrexato, micofenolato mofetile) nel trattamento dell'uveite autoimmune
• Valutare i farmaci biologici mirati alla via Th1/Th17 (anti-IL-17, anti-IL-23, anti-IFN-γ)
• Convalida del target delle risposte autoimmuni mediate dalle cellule T oculari
• Scoperta di biomarcatori (citochine infiammatorie, marcatori di danno retinico)
• Studi farmacologici e tossicologici a sostegno dell'IND
portata |
Specifica |
Specie/ceppo |
Mouse C57BL/6 |
metodo di induzione |
Immunizzare per via sottocutanea con peptidi IRBP emulsionati in CFA (p. es., IRBP1-20, 200-300 μg), integrati con Mycobacterium tuberculosis e più tossina della pertosse intraperitoneale (0,5-1 μg) al momento dell'immunizzazione |
tempo di studio |
21–35 giorni dopo l’immunizzazione (picco della malattia ~14–21 giorni) |
punto finale critico |
Fotografia del fondo oculare e punteggio clinico (grado 0-4 del disco ottico, vasculite, infiltrati), tomografia a coerenza ottica (OCT) per la misurazione dello spessore retinico, punteggio OCT, istopatologia (colorazione HE retinale per rilevare infiltrato infiammatorio e danno strutturale), opzionale: citometria a flusso delle cellule immunitarie retiniche/linfonodali (cellule T CD4+, sottogruppi Th1/Th17), analisi delle citochine (IFN-γ, IL-17, tumore fattore di necrosi-α) |
pacchetto |
Dati grezzi, referti di analisi, immagini del fondo oculare, dati OCT, sezioni istologiche, bioinformatica (opzionale) Dati grezzi, referti di analisi, punteggi clinici, sezioni istologiche, analisi del siero (IL-6, CRP), opzionale: anticorpi anti-CII, imaging micro-CT |
D: In che modo l'IRBP induce l'EAU?
Risposta: L'IRBP è un antigene retinico. L'immunizzazione con peptidi IRBP negli adiuvanti attiva le cellule presentanti l'antigene, che presentano l'antigene alle cellule T naive, guidando la loro differenziazione in cellule effettrici patogene Th1 e Th17. Queste cellule si infiltrano nell’occhio, rilasciano citochine infiammatorie (IFN-γ, IL-17, TNF-α) e causano infiammazione e danni alla retina.
D: Quali sono le principali somiglianze con l'uveite autoimmune umana?
R: Questo modello presenta infiammazione mediata dalle cellule T (Th1/Th17), rottura della barriera emato-retinica, infiltrazione di cellule infiammatorie, danno strutturale della retina e segni clinici visibili sul fondoscopio e sull'OCT, che sono strettamente correlati all'uveite umana non infettiva.
D: Questo modello può essere utilizzato per gli studi di supporto IND?
Risposta: sì. Gli studi possono essere condotti secondo i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diversi peptidi IRBP, dosi, tempi di trattamento)?
Risposta: certo. Il nostro team scientifico adatta i regimi di immunizzazione, i piani di trattamento e le analisi degli endpoint al tuo specifico farmaco candidato.
