| Beschikbaarheid: | |
|---|---|
| Aantal: | |











Klinisch relevant – Overzicht van menselijke auto-immuunuveïtis met door Th1/Th17 gemedieerde ontsteking, schade aan het netvlies en verstoring van de bloed-retinale barrière.
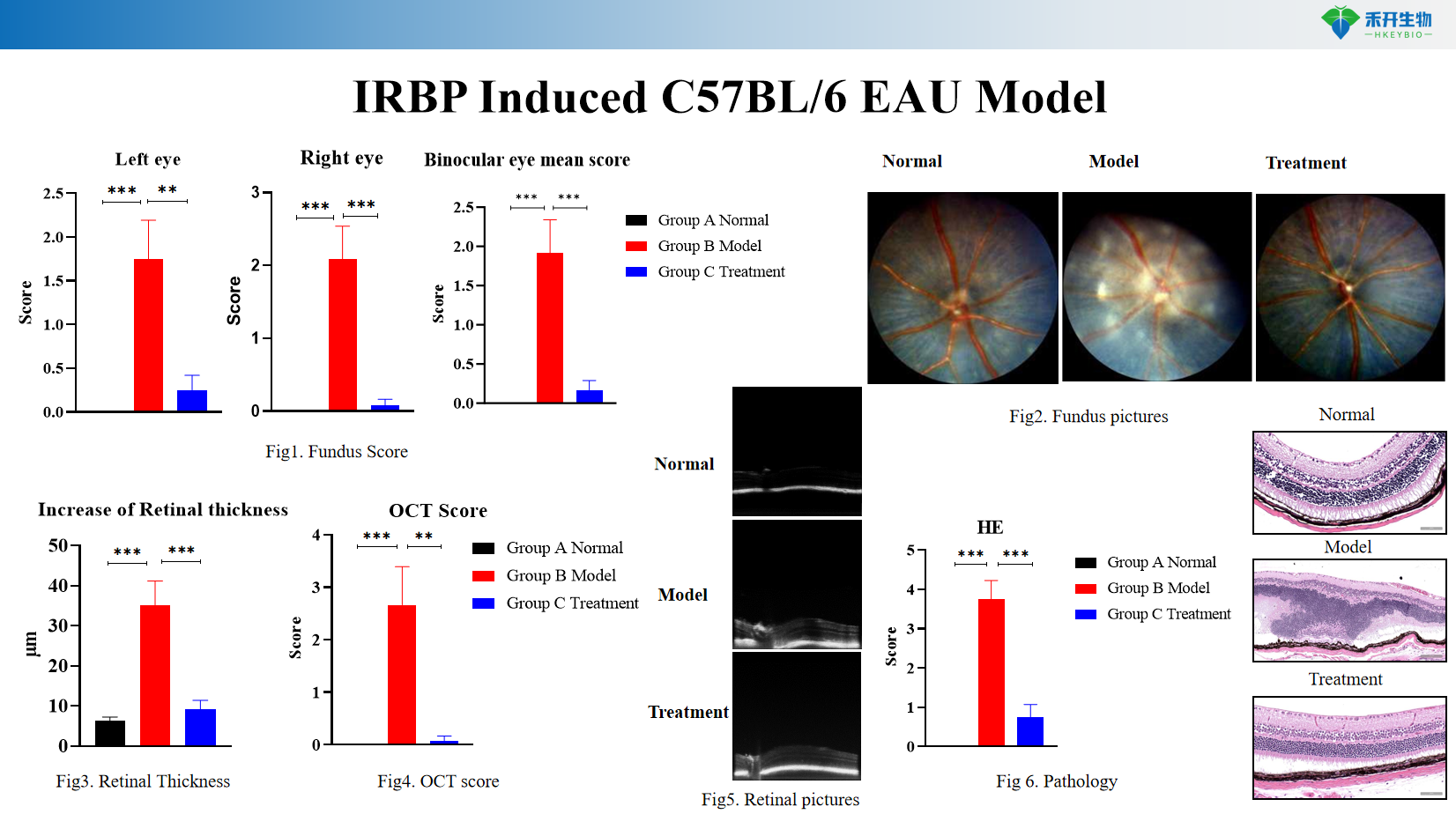
Geavanceerde eindpunten voor beeldvorming – fundusfotografie en scoring, optische coherentietomografie (OCT) voor het meten van de dikte van het netvlies.
Uitgebreide pathologie – Histopathologie (HE-kleuring) van inflammatoir infiltraat en structurele schade aan het netvlies.
Mechanistisch aangedreven – IRBP activeert antigeenpresenterende cellen, waardoor Th1- en Th17-differentiatie en de productie van inflammatoire cytokines (IFN-γ, IL-17, TNF-α) worden gestimuleerd.
IND Ready Packet – Onderzoek kan worden uitgevoerd volgens de GLP-principes.
IRBP Induceerbaar C57BL/6 EAU-model
• Het testen van de werkzaamheid van immunomodulatoren (corticosteroïden, methotrexaat, mycofenolaatmofetil) bij de behandeling van auto-immuun uveïtis
• Evalueer biologische geneesmiddelen die zich richten op de Th1/Th17-route (anti-IL-17, anti-IL-23, anti-IFN-γ)
• Doelvalidatie van oculaire T-cel-gemedieerde auto-immuunreacties
• Ontdekking van biomarkers (inflammatoire cytokines, markers voor schade aan het netvlies)
• Farmacologische en toxicologische onderzoeken ter ondersteuning van de IND
domein |
Specificatie |
Soort/stam |
C57BL/6 muis |
inductie methode |
Subcutaan immuniseren met IRBP-peptiden geëmulgeerd in CFA (bijv. IRBP1-20, 200-300 μg), aangevuld met Mycobacterium tuberculosis, en plus intraperitoneaal pertussistoxine (0,5-1 μg) op het moment van immunisatie |
studie tijd |
21–35 dagen na immunisatie (piek van de ziekte ~14–21 dagen) |
kritisch eindpunt |
Fundusfotografie en klinische scoring (graad 0-4 van optische schijf, vasculitis, infiltraten), optische coherentietomografie (OCT) voor meting van de dikte van het netvlies, OCT-score, histopathologie (HE-kleuring van het netvlies om inflammatoir infiltraat en structurele schade te detecteren), optioneel: flowcytometrie van immuuncellen van het netvlies/lymfeklier (CD4+ T-cellen, Th1/Th17-subsets), cytokineanalyse (IFN-γ, IL-17, tumornecrosefactor-α) |
pakket |
Ruwe data, analyserapporten, fundusbeelden, OCT-data, histologische coupes, bio-informatica (optioneel) Ruwe data, analyserapporten, klinische scores, histologische coupes, serumanalyse (IL-6, CRP), optioneel: anti-CII-antilichamen, micro-CT-beeldvorming |
Vraag: Hoe induceert IRBP EAU?
Antwoord: IRBP is een retinaal antigeen. Immunisatie met IRBP-peptiden in adjuvantia activeert antigeenpresenterende cellen, die antigeen presenteren aan naïeve T-cellen, waardoor hun differentiatie in pathogene Th1- en Th17-effectorcellen wordt gestimuleerd. Deze cellen infiltreren het oog, geven ontstekingscytokinen vrij (IFN-γ, IL-17, TNF-α) en veroorzaken ontstekingen en schade aan het netvlies.
Vraag: Wat zijn de belangrijkste overeenkomsten met menselijke auto-immuunuveïtis?
A: Dit model vertoont T-cel-gemedieerde ontsteking (Th1/Th17), verstoring van de bloed-retinale barrière, infiltratie van inflammatoire cellen, structurele schade aan het netvlies en klinische symptomen zichtbaar op funduscoop en OCT, die nauw verwant zijn aan menselijke niet-infectieuze uveïtis.
Vraag: Kan dit model worden gebruikt voor IND-ondersteuningsonderzoeken?
Antwoord: Ja. Studies kunnen worden uitgevoerd volgens de GLP-principes voor indieningen bij de regelgevende instanties (FDA, EMA).
Vraag: Bieden jullie op maat gemaakte onderzoeksprotocollen aan (bijvoorbeeld verschillende IRBP-peptiden, doses, behandeltijden)?
Antwoord: Natuurlijk. Ons wetenschappelijk team stemt immunisatieregimes, behandelplannen en eindpuntanalyses af op uw specifieke kandidaat-geneesmiddel.
