| Verfügbarkeit: | |
|---|---|
| Menge: | |











Klinisch relevant – Überblick über die menschliche Autoimmun-Uveitis mit Th1/Th17-vermittelter Entzündung, Netzhautschädigung und Störung der Blut-Netzhaut-Schranke.
Erweiterte Bildgebungsendpunkte – Fundusfotografie und -bewertung, optische Kohärenztomographie (OCT) zur Messung der Netzhautdicke.
Umfassende Pathologie – Histopathologie (HE-Färbung) von entzündlichem Infiltrat und Netzhautstrukturschäden.
Mechanistisch gesteuert – IRBP aktiviert Antigen-präsentierende Zellen und treibt die Th1- und Th17-Differenzierung sowie die Produktion von entzündlichen Zytokinen (IFN-γ, IL-17, TNF-α) voran.
IND Ready Packet – Forschung kann gemäß den GLP-Grundsätzen durchgeführt werden.
IRBP-induzierbares C57BL/6 EAU-Modell
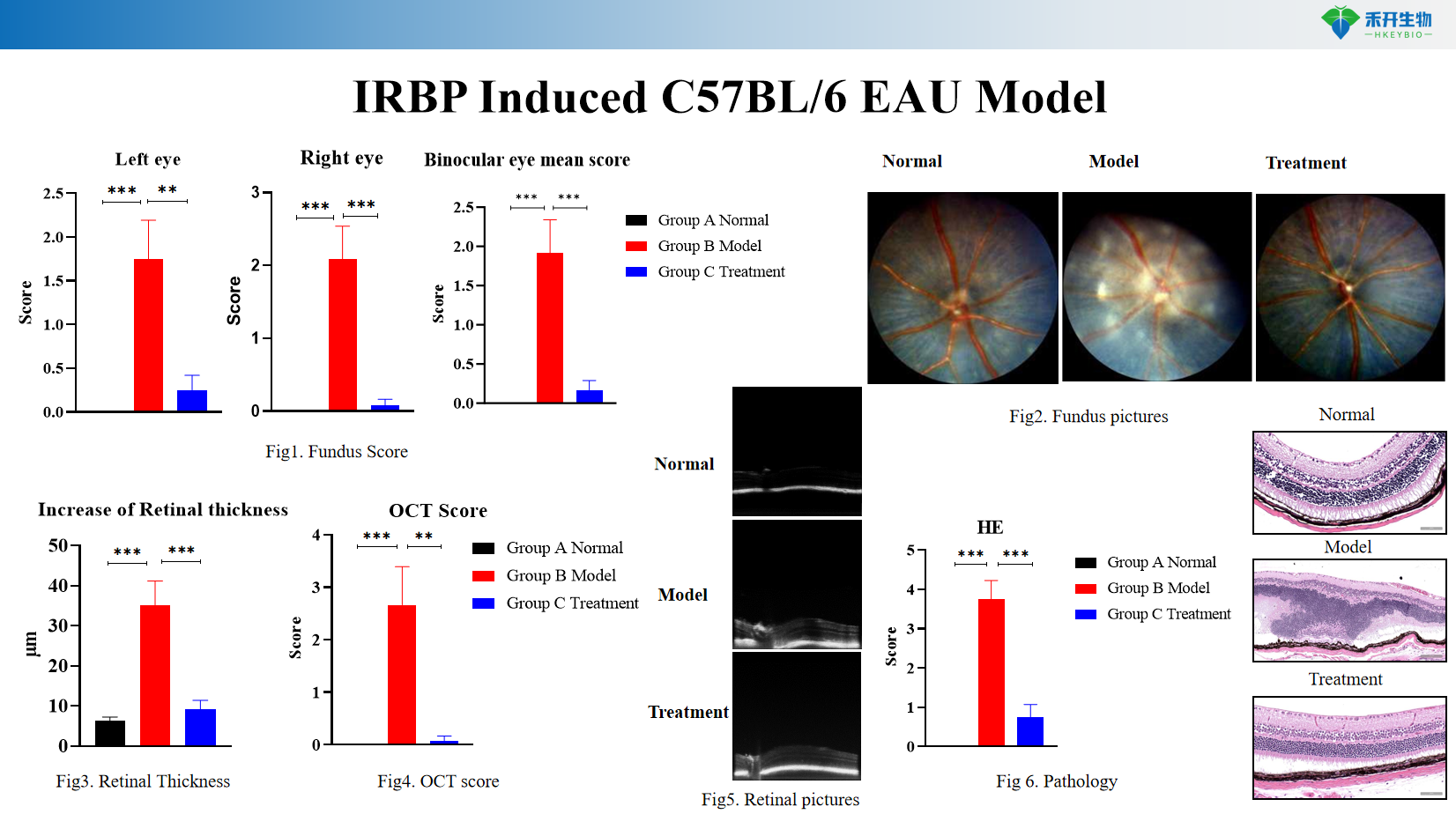
• Prüfung der Wirksamkeit von Immunmodulatoren (Kortikosteroide, Methotrexat, Mycophenolatmofetil) bei der Behandlung von Autoimmun-Uveitis
• Bewertung von Biologika, die auf den Th1/Th17-Signalweg abzielen (Anti-IL-17, Anti-IL-23, Anti-IFN-γ)
• Zielvalidierung okulärer T-Zell-vermittelter Autoimmunreaktionen
• Entdeckung von Biomarkern (entzündliche Zytokine, Marker für Netzhautschäden)
• Pharmakologische und toxikologische Studien zur Unterstützung von IND
Umfang |
Spezifikation |
Art/Stamm |
C57BL/6-Maus |
Induktionsmethode |
Immunisieren Sie subkutan mit in CFA emulgierten IRBP-Peptiden (z. B. IRBP1-20, 200–300 μg), ergänzt mit Mycobacterium tuberculosis und plus intraperitonealem Pertussis-Toxin (0,5–1 μg) zum Zeitpunkt der Immunisierung |
Lernzeit |
21–35 Tage nach der Immunisierung (Höhepunkt der Erkrankung ~14–21 Tage) |
kritischer Endpunkt |
Fundusfotografie und klinische Bewertung (Grad 0–4 der Sehnervenpapille, Vaskulitis, Infiltrate), optische Kohärenztomographie (OCT) zur Messung der Netzhautdicke, OCT-Bewertung, Histopathologie (retinale HE-Färbung zur Erkennung entzündlicher Infiltrate und struktureller Schäden), optional: Durchflusszytometrie von Netzhaut-/Lymphknoten-Immunzellen (CD4+ T-Zellen, Th1/Th17-Untergruppen), Zytokinanalyse (IFN-γ, IL-17, Tumornekrosefaktor-α) |
Paket |
Rohdaten, Analyseberichte, Fundusbilder, OCT-Daten, histologische Schnitte, Bioinformatik (optional) Rohdaten, Analyseberichte, klinische Scores, histologische Schnitte, Serumanalyse (IL-6, CRP), optional: Anti-CII-Antikörper, Mikro-CT-Bildgebung |
F: Wie induziert IRBP EAU?
Antwort: IRBP ist ein retinales Antigen. Die Immunisierung mit IRBP-Peptiden in Adjuvantien aktiviert Antigen-präsentierende Zellen, die naiven T-Zellen Antigene präsentieren und so deren Differenzierung in pathogene Th1- und Th17-Effektorzellen vorantreiben. Diese Zellen dringen in das Auge ein, setzen entzündliche Zytokine (IFN-γ, IL-17, TNF-α) frei und verursachen eine Entzündung und Schädigung der Netzhaut.
F: Was sind die wichtigsten Ähnlichkeiten zur menschlichen Autoimmun-Uveitis?
A: Dieses Modell weist eine T-Zell-vermittelte Entzündung (Th1/Th17), eine Störung der Blut-Netzhaut-Schranke, eine Infiltration entzündlicher Zellen, eine Schädigung der Netzhautstruktur und klinische Anzeichen auf, die auf dem Funduskop und im OCT sichtbar sind und in engem Zusammenhang mit einer nichtinfektiösen Uveitis beim Menschen stehen.
F: Kann dieses Modell für IND-Unterstützungsstudien verwendet werden?
Antwort: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. verschiedene IRBP-Peptide, Dosen, Behandlungszeiten)?
Antwort: Natürlich. Unser wissenschaftliches Team passt Impfschemata, Behandlungspläne und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
