| Verfügbarkeit: | |
|---|---|
| Menge: | |











Ergänzender Mechanismus – Das MSU-Modell simuliert eine durch Kristalle verursachte Entzündung (durch Gicht verursacht); Das LPS-Modell simuliert eine durch bakterielles Endotoxin verursachte Entzündung.
Quantifizierbare Endpunkte – Neutrophilenzahl in der Peritonealspülflüssigkeit (MSU-Modell), IL-1β- und IL-6-Spiegel in der Peritonealspülflüssigkeit und im Blut (LPS-Modell).
Schnell und reproduzierbar – Beide Modelle lösen innerhalb von Stunden eine akute Entzündung aus und ermöglichen so ein schnelles Screening entzündungshemmender Verbindungen.
Translationaler Wert – ideal zum Testen von entzündungshemmenden Arzneimitteln (NSAIDs, Kortikosteroiden), IL-1-Inhibitoren (Anakinra, Canakinumab) und TLR4-Antagonisten.
IND Ready Packet – Forschung kann gemäß den GLP-Grundsätzen durchgeführt werden.
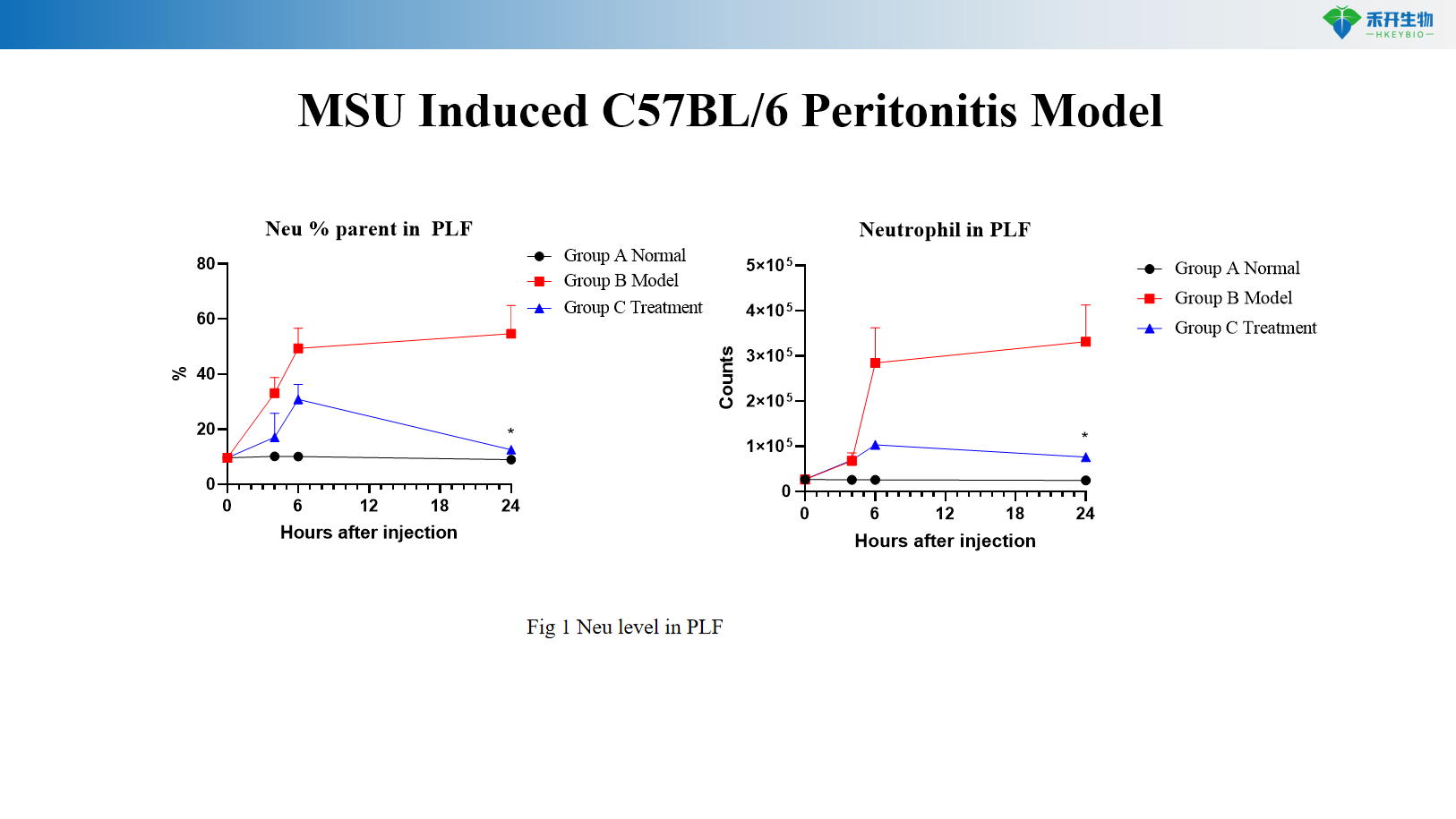
MSU-induziertes C57BL/6-Peritonitis-Modell
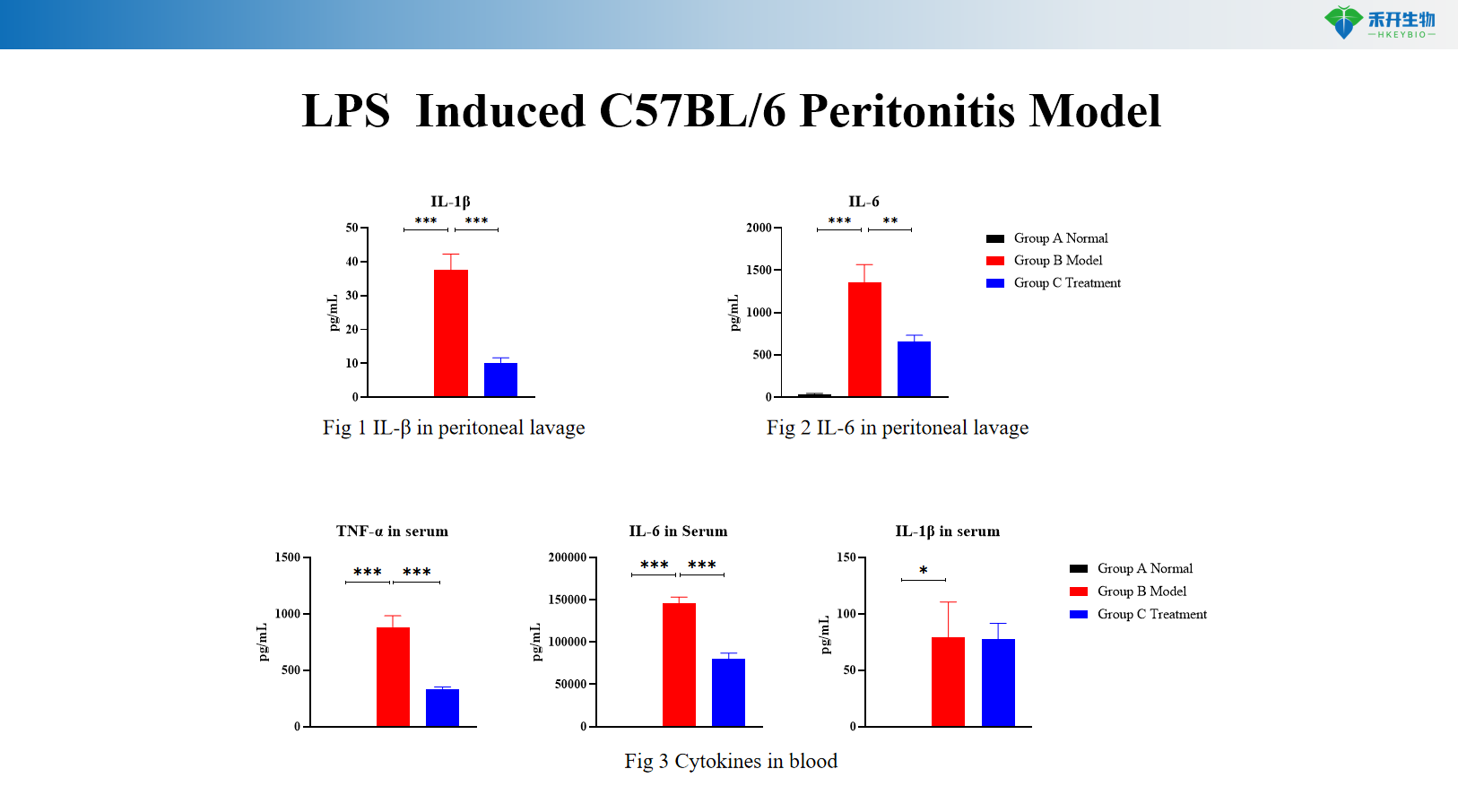
LPS-induziertes C57BL/6-Peritonitis-Modell
• Wirksamkeitsprüfung von entzündungshemmenden Medikamenten (NSAIDs, Kortikosteroide, COX-2-Hemmer)
• Bewertung von IL-1-Inhibitoren (Anakinra, Canakinumab), NLRP3-Inflammasom-Inhibitoren und TLR4-Antagonisten
• Zielvalidierung der Neutrophilenrekrutierung und der Zytokinwege
• Entdeckung von Biomarkern (Neutrophilenmarker, Zytokinprofile)
• Pharmakologische und toxikologische Studien zur Unterstützung von IND
Umfang |
MSU-induziertes Peritonitis-Modell |
LPS-induziertes Peritonitis-Modell |
Art/Stamm |
C57BL/6-Maus |
C57BL/6-Maus |
Induktionsmethode |
Intraperitoneale Injektion von MSU-Kristallen (1–3 mg/Maus) | Intraperitoneale Injektion von LPS (5–20 mg/kg) |
Lernzeit |
4-24 Stunden nach der Induktion | 2–24 Stunden nach der Induktion |
kritischer Endpunkt |
Neutrophilenzahl in der Peritonealspülflüssigkeit (Durchflusszytometrie oder Zytospin) |
IL-1β- und IL-6-Spiegel in Peritonealspülflüssigkeit und Blut (ELISA) |
| Positivkontrolle | Als entzündungshemmende Referenzverbindungen können Dexamethason oder Indomethacin verwendet werden | |
| Paket | Rohdaten, Analysebericht, Zellzahl, ELISA-Ergebnisse, Bioinformatik (optional) Rohdaten, Analysebericht, Zellzahl, ELISA-Ergebnisse, Bioinformatik (optional) | |
F: Was ist der Unterschied zwischen MSU- und LPS-Peritonitismodellen?
A: MSU-Kristalle aktivieren das NLRP3-Inflammasom und führen zu einer IL-1β-vermittelten neutrophilen Entzündung, ähnlich einer kristallinduzierten Peritonitis (z. B. Gicht). LPS aktiviert die TLR4-Signalübertragung und löst eine breite proinflammatorische Zytokinreaktion (IL-1β, IL-6, TNF-α) aus, ähnlich einer durch bakterielles Endotoxin verursachten Peritonitis.
F: Welches Modell eignet sich besser zum Testen von NLRP3-Inhibitoren?
A: Das Modell der MSU-induzierten Peritonitis basiert ausschließlich auf der Aktivierung des NLRP3-Inflammasoms und IL-1β und eignet sich daher ideal für die Bewertung von NLRP3-Inhibitoren und auf IL-1 ausgerichteten Therapien. Das LPS-Modell aktiviert mehrere Wege und eignet sich für ein umfassenderes entzündungshemmendes Screening.
F: Können diese Modelle für IND-Unterstützungsstudien verwendet werden?
Antwort: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche MSU-Dosen, LPS-Konzentrationen, Behandlungszeiten)?
Antwort: Natürlich. Unser wissenschaftliches Team erstellt maßgeschneiderte Induktionsprotokolle, Behandlungspläne (präventiv oder therapeutisch) und Endpunktanalysen für Ihren spezifischen Medikamentenkandidaten.
F: Wie sieht der typische Zeitplan für eine Pilot-Wirksamkeitsstudie aus?
A: Beide Modelle sind akut und die Studien werden in der Regel innerhalb von 24 Stunden nach der Induktion abgeschlossen, was ein schnelles Screening entzündungshemmender Verbindungen ermöglicht.
