| Verfügbarkeit: | |
|---|---|
| Menge: | |











Breites Modellportfolio – Allergen- (OVA, HDM, Fel d 1), Adjuvans-kombinierte (LPS, c-di-GMP) und TSLP-gesteuerte (MC903) Modelle, die eosinophile, neutrophile und gemischte granulozytäre Asthma-Endotypen abdecken.
Mehrere Stämme – C57BL/6-, BALB/c-, HIS-humanisierte und transgene IL4/IL4R-Mäuse verfügbar.
Umfassende Endpunkte – Körpergewicht, AHR (Penh, Resistenz), BALF-Zellzahlen (Eosinophile, Neutrophile, Makrophagen), Serum-Gesamt-IgE und allergenspezifisches IgE, Zytokin-Profilierung (IL-4, IL-5, IL-13, IL-17), Lungenhistopathologie (HE, Masson, PAS), Hämatologie.
Translationswert – Ideal zum Testen von Biologika (Anti-IL-4Rα, Anti-IL-5, Anti-IL-13, Anti-TSLP, Anti-IL-33), JAK-Inhibitoren, Kortikosteroiden und Bronchodilatatoren.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen durchgeführt werden.
OVA-induziertes Asthmamodell bei C57BL/6-Mäusen
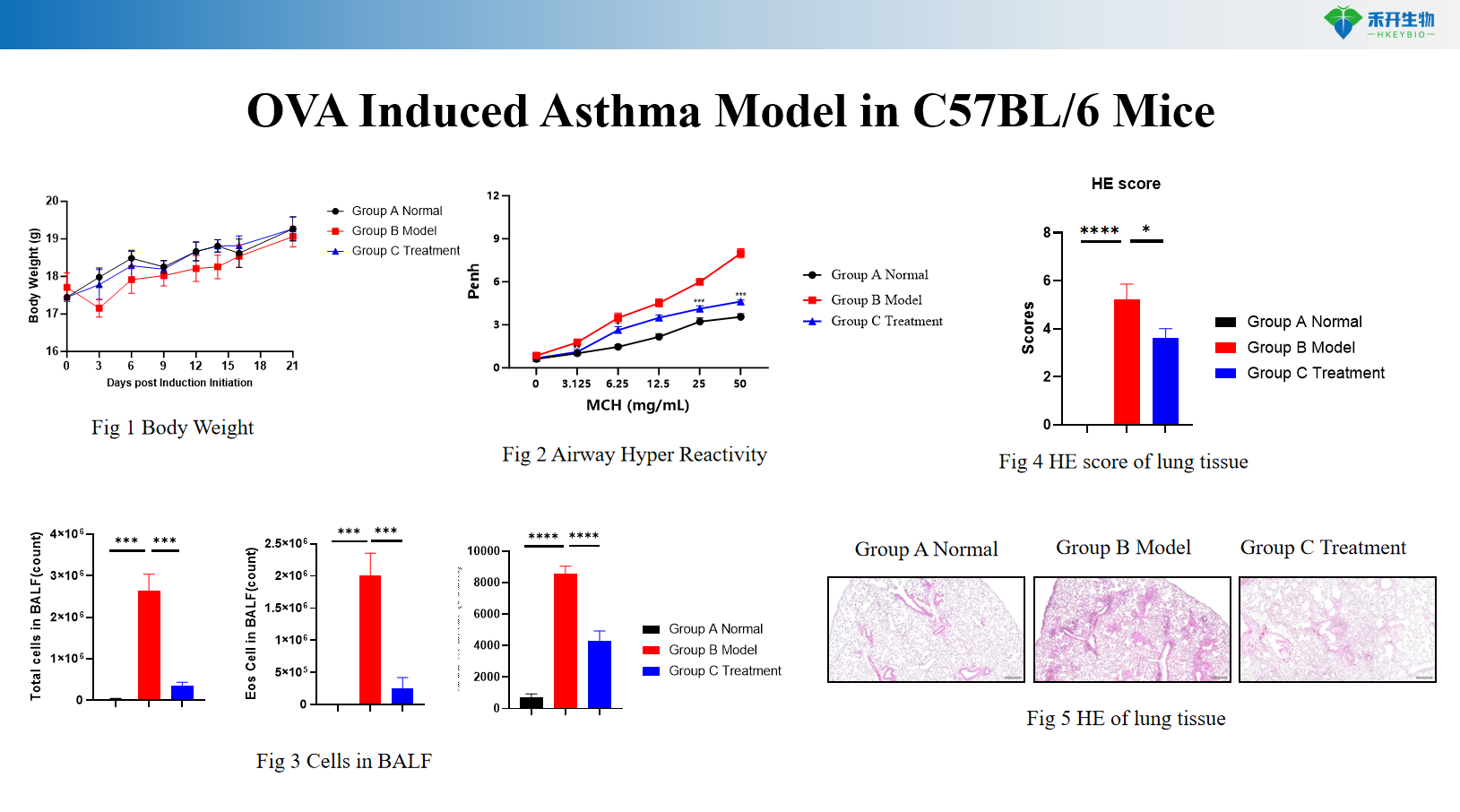
OVA-induziertes Asthmamodell bei BALB/c-Mäusen
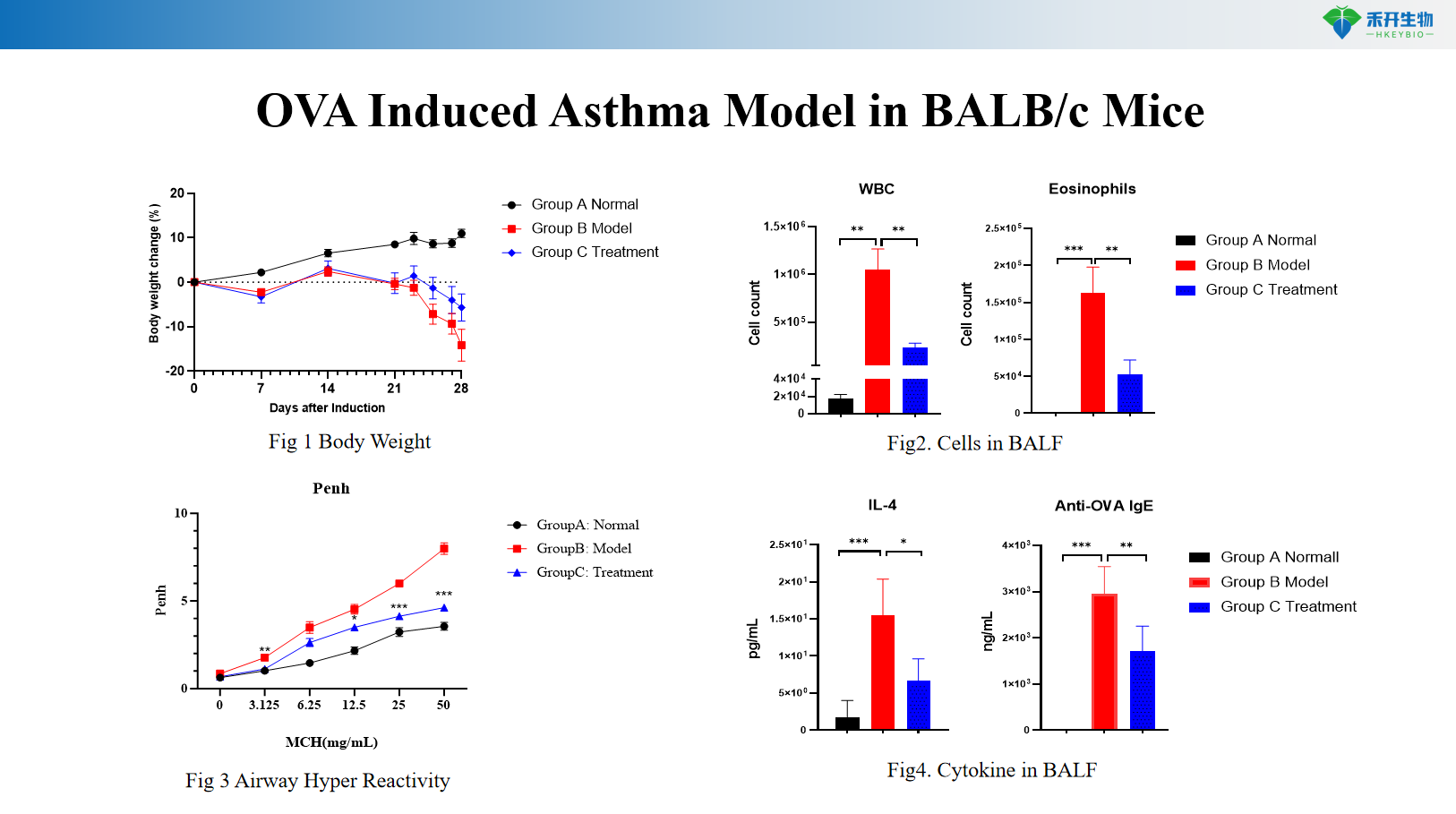
OVA-induziertes Asthmamodell bei HIS-Mäusen
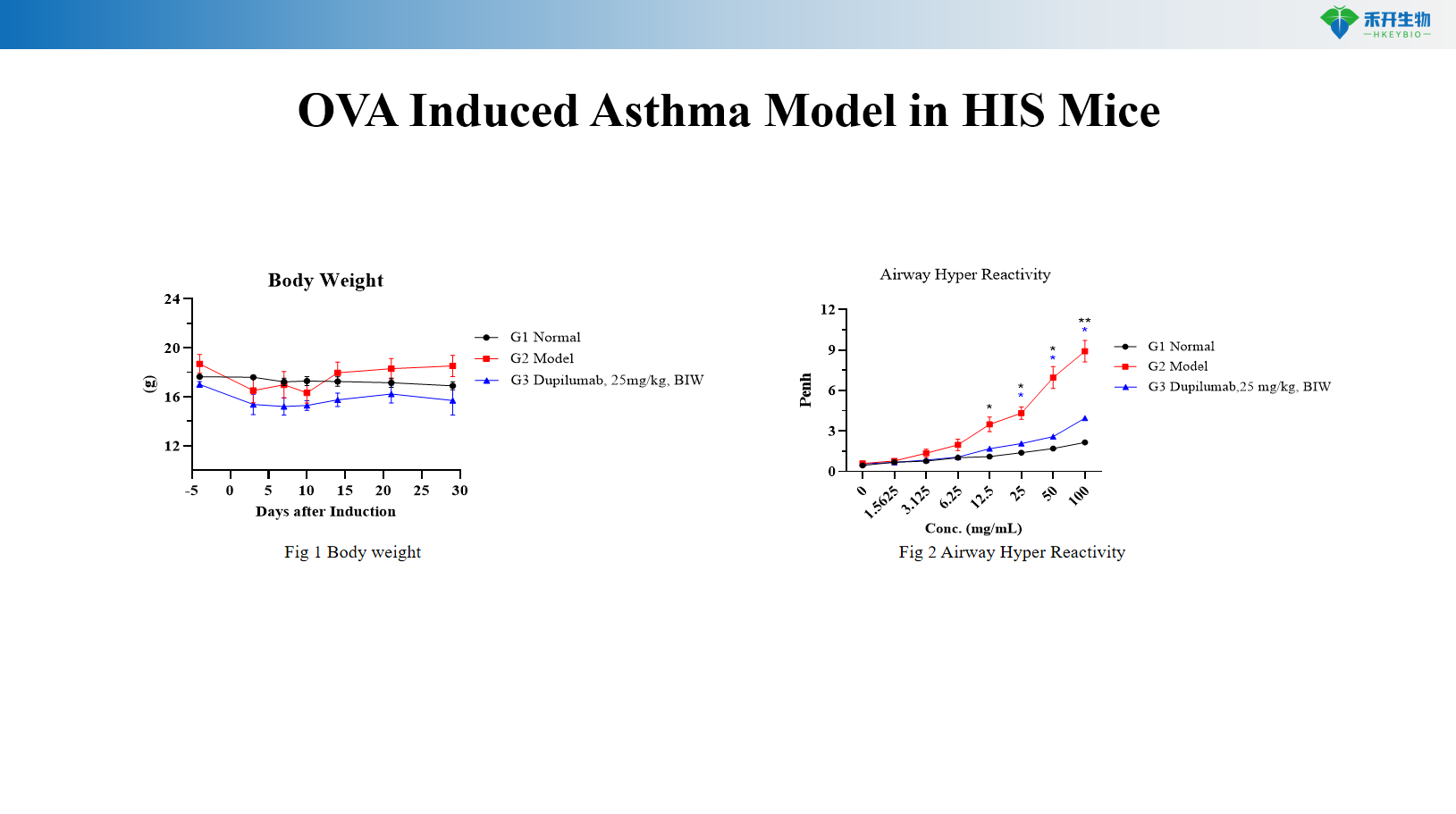
OVA+MC903-induziertes Asthmamodell bei C57BL/6-Mäusen
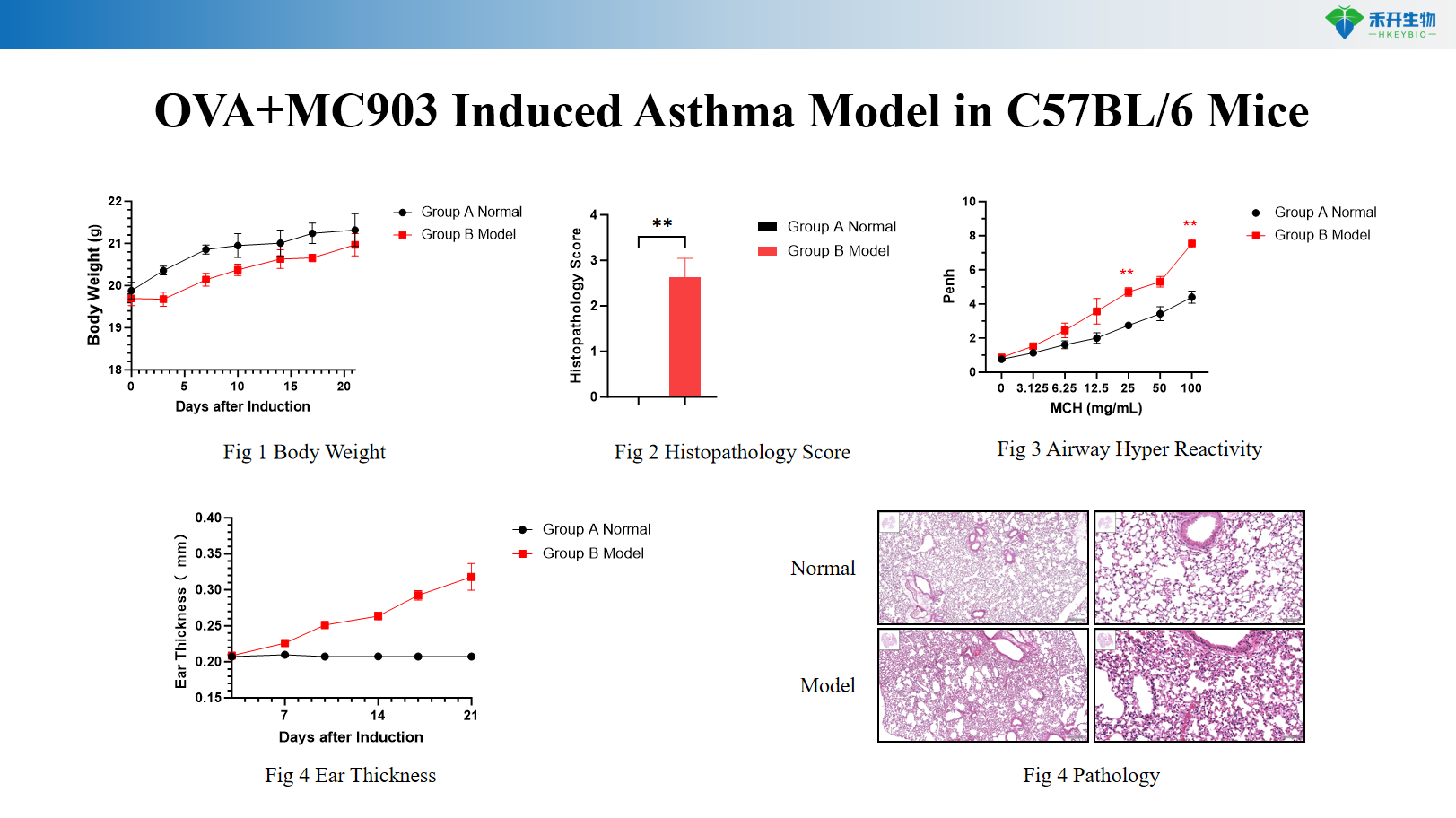
OVA+LPS-induziertes neutrophiles Asthmamodell bei C57BL/6-Mäusen
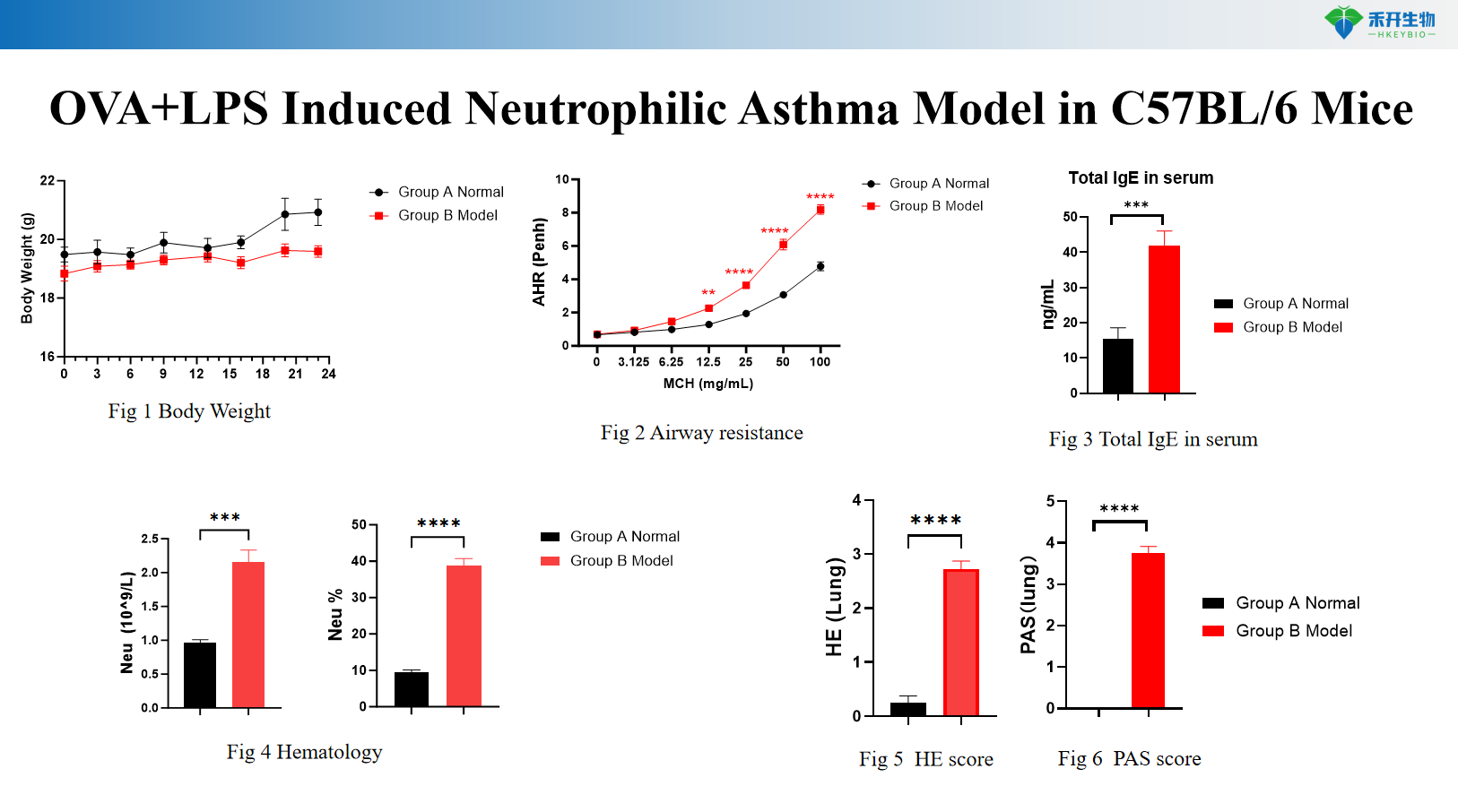
HDM-induziertes Asthmamodell bei C57BL/6-Mäusen
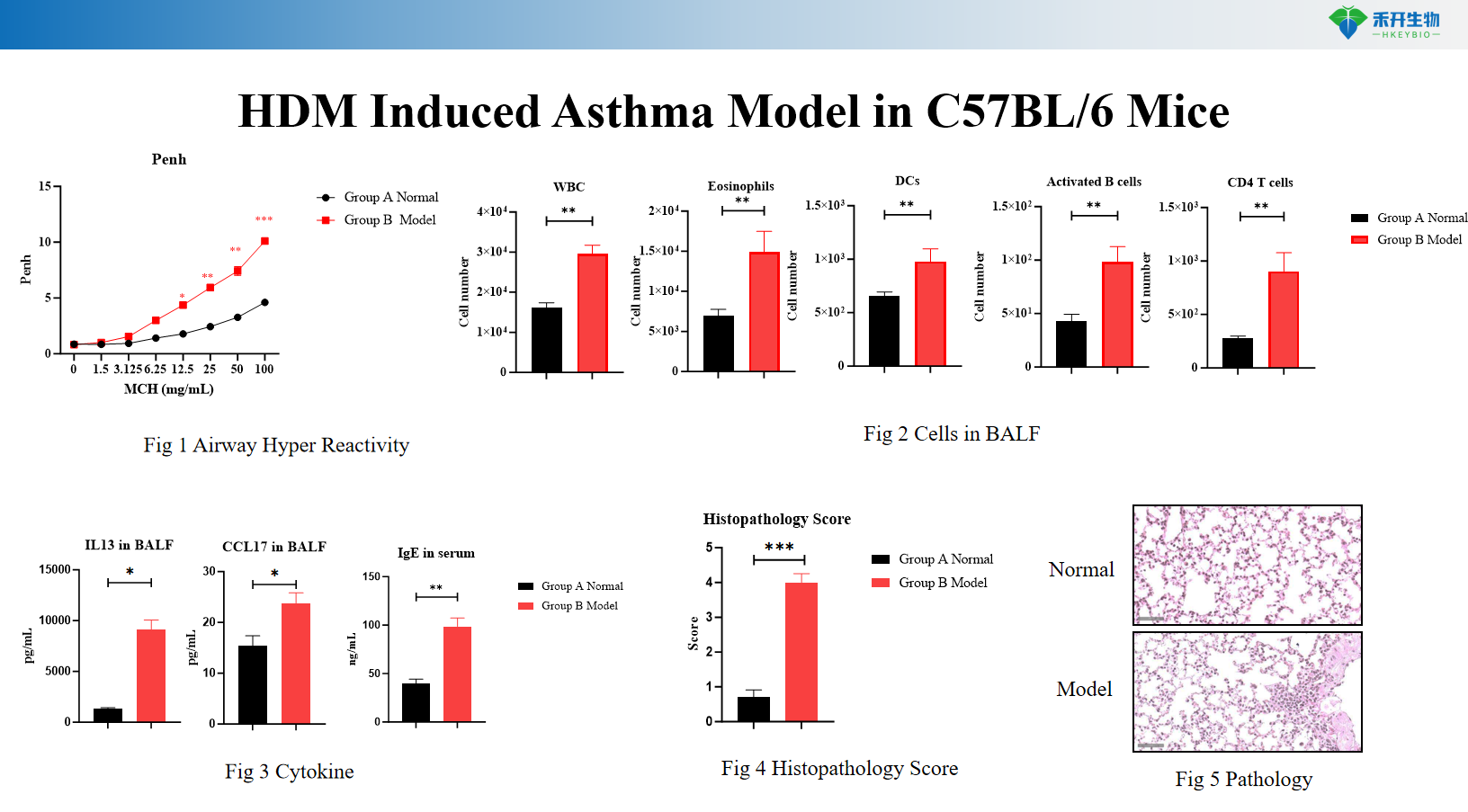
HDM-induziertes Asthmamodell bei IL4/IL4R-Mäusen
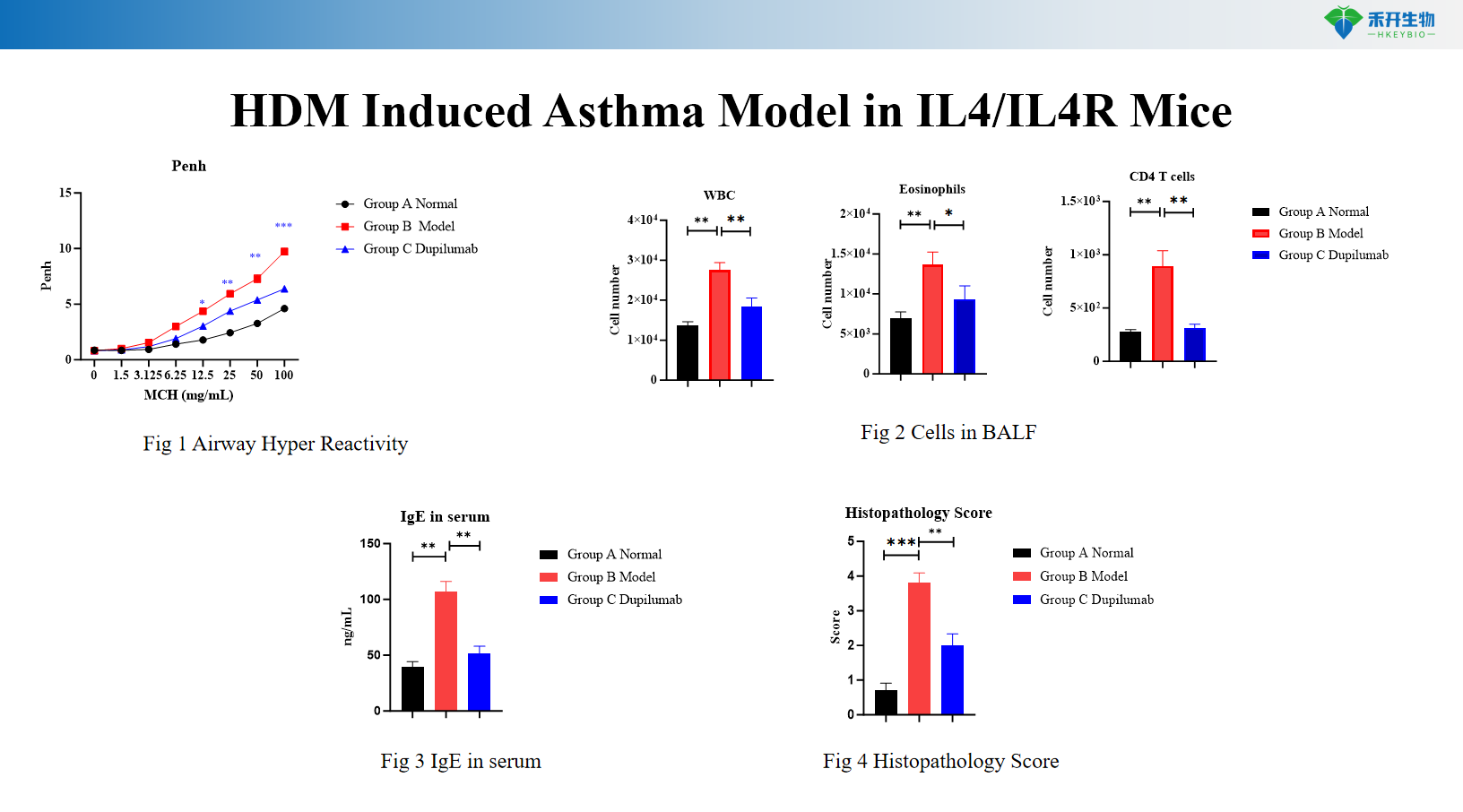
HDM+LPS-induziertes Asthmamodell bei C57BL/6-Mäusen
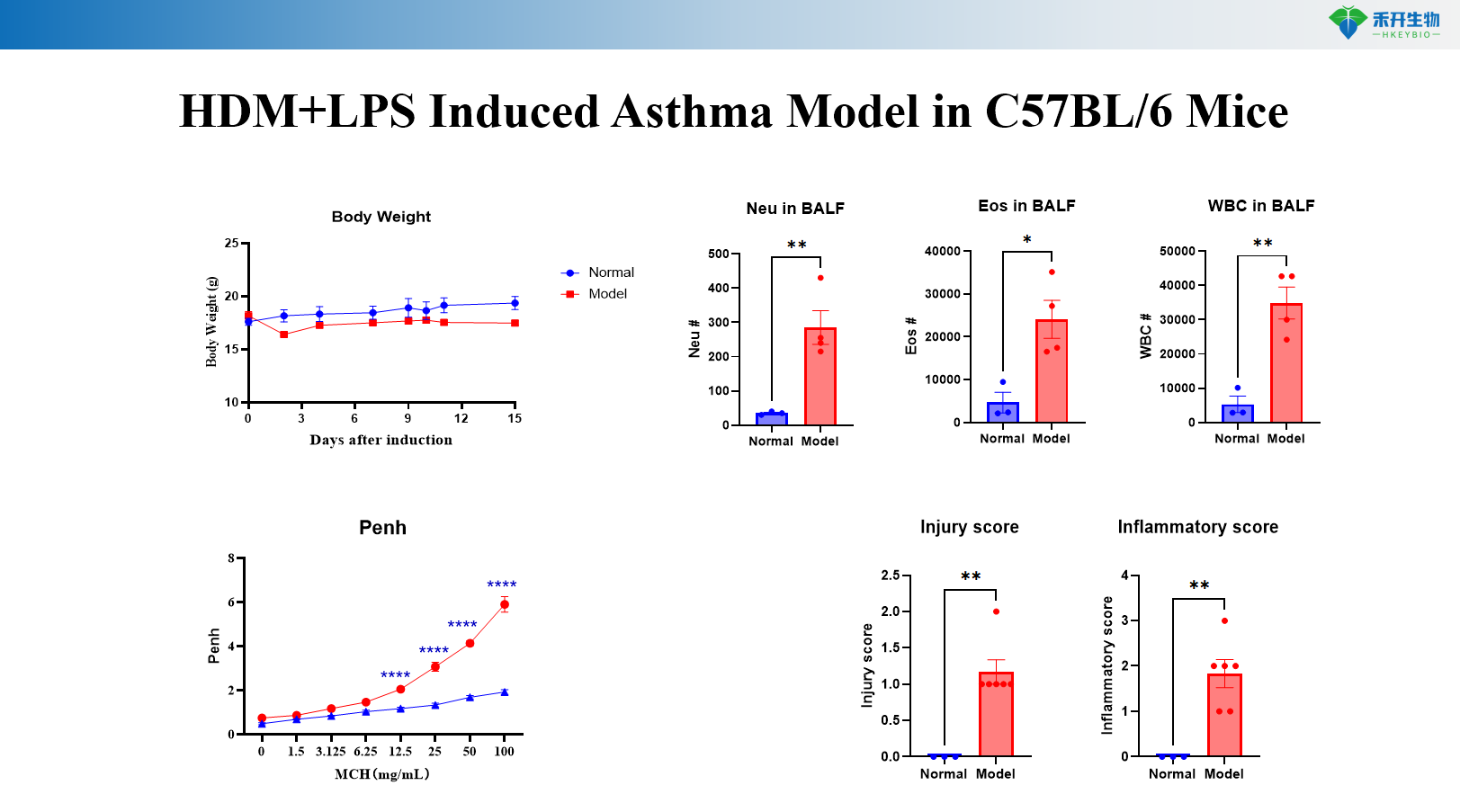
HDM+MC903-induziertes Asthmamodell bei C57BL/6-Mäusen

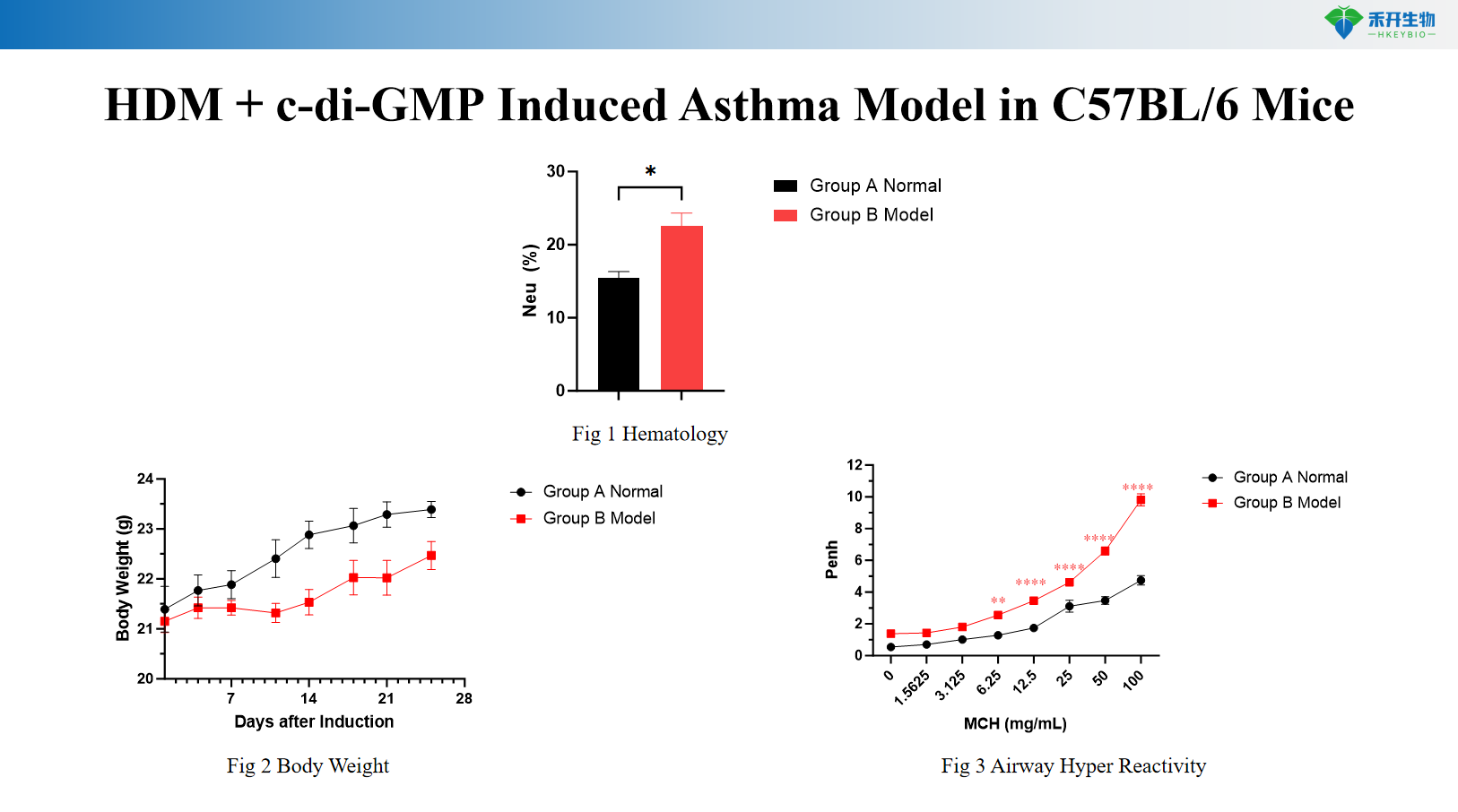
HDM + c-di-GMP-induziertes Asthmamodell bei C57BL/6-Mäusen
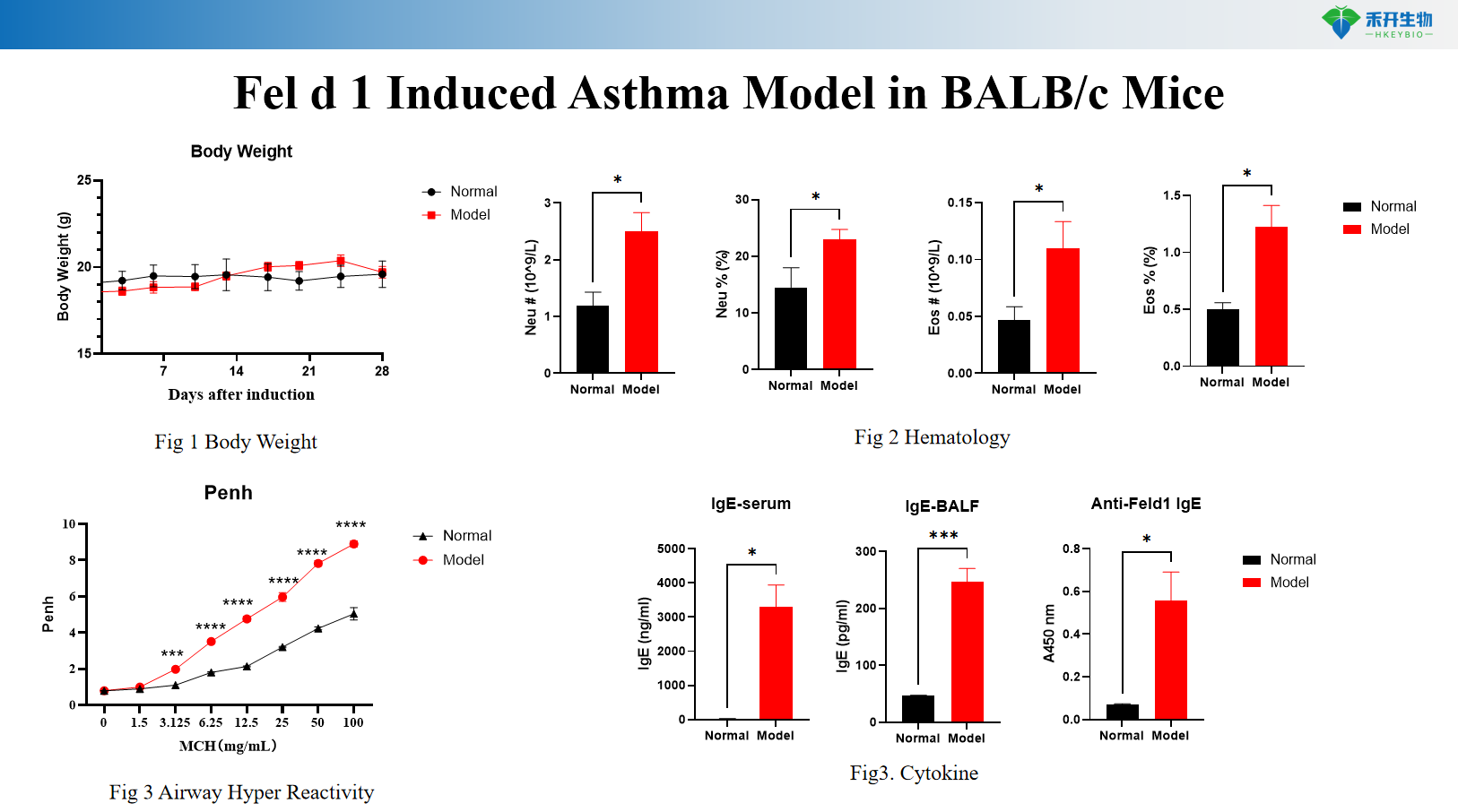
Fel d 1-induziertes Asthmamodell bei BALB/c-Mäusen
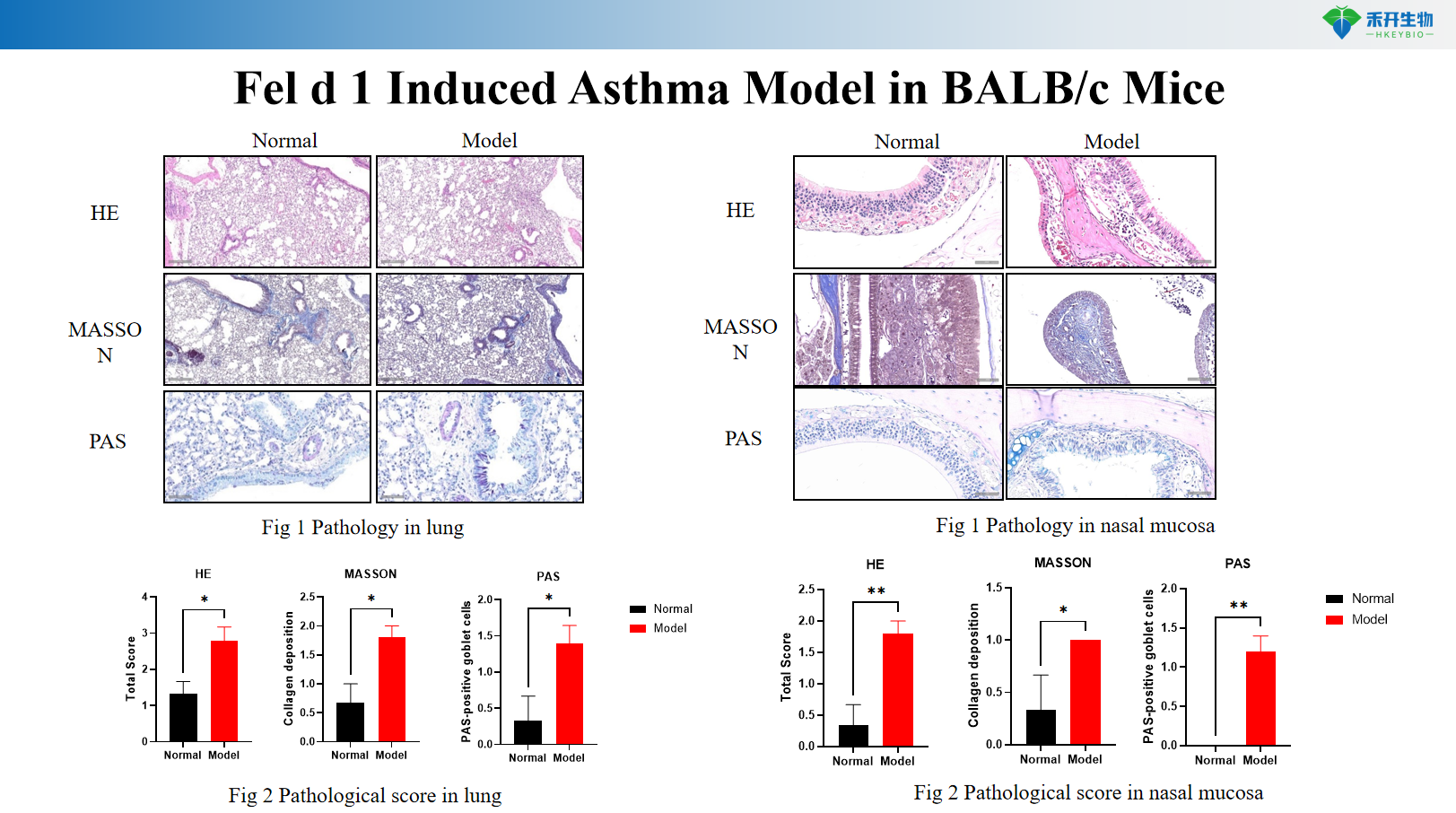
• Wirksamkeitsprüfung von Biologika (Anti-IL-4Rα, Anti-IL-5, Anti-IL-13, Anti-TSLP, Anti-IL-33)
• Bewertung niedermolekularer Inhibitoren (JAK-Inhibitoren, PDE4-Inhibitoren, CRTH2-Antagonisten)
• Zielvalidierung für Th2-, Th17- und epitheliale Zytokinwege
• Biomarker-Entdeckung (IgE, Zytokinsignaturen, Eosinophilen-/Neutrophilen-Marker)
• IND-ermöglichende Pharmakologie- und Toxikologiestudien
Parameter |
Spezifikation |
Art/Stamm |
C57BL/6, BALB/c, HIS humanisiert, IL4/IL4R transgen |
Induktionsmethode |
OVA ± Alaun ± MC903 ± LPS; HDM ± LPS ± MC903 ± c-di-GMP; Fel d 1 + Alaun |
Studiendauer |
3–8 Wochen (Sensibilisierungs- und Provokationsphasen) |
Wichtige Endpunkte |
Körpergewicht, AHR (invasiv/nicht-invasiv), BALF-Zytologie (Eosinophile, Neutrophile, Makrophagen), Serum-Gesamt-IgE und allergenspezifisches IgE, Zytokinspiegel (IL-4, IL-5, IL-13, IL-17, IFN-γ), Lungenhistopathologie (HE, Masson, PAS) mit Bewertung, Hämatologie (optional) |
| Positivkontrolle | Dexamethason oder Anti-IL-4Rα-Antikörper sind als Referenzverbindungen verfügbar |
Datenpaket |
Rohdaten, Analyseberichte, BALF-Zellzahlen, ELISA-Ergebnisse, Histologie-Objektträger, Lungenfunktionsdaten, Bioinformatik (optional) |
F: Wie wähle ich das richtige AD-Modell für meinen Medikamentenkandidaten aus?
A: Für eosinophiles (Th2-hohes) Asthma werden OVA- oder HDM-Modelle in BALB/c oder C57BL/6 empfohlen. Für neutrophiles oder gemischtes granulozytäres Asthma sind OVA+LPS- oder HDM+c-di-GMP-Modelle in C57BL/6 geeignet. HIS-humanisierte Mäuse eignen sich ideal zum Testen humanspezifischer Biologika. Transgene IL4/IL4R-Mäuse eignen sich für Th2-Signalwegstudien. Unser wissenschaftliches Team kann die Modellauswahl basierend auf Ihrem spezifischen Ziel steuern.
F: Was ist der Unterschied zwischen OVA- und HDM-induzierten Modellen?
A: OVA ist ein Modellallergen, das zur Sensibilisierung ein Adjuvans benötigt und starke Th2-Reaktionen hervorruft. HDM ist ein klinisch relevantes menschliches Allergen, das Proteasen enthält, die sowohl die angeborene als auch die adaptive Immunität aktivieren und so die Pathogenese des menschlichen allergischen Asthmas besser nachahmen.
F: Können diese Modelle für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. verschiedene Sensibilisierungs-/Provokationspläne, Kombinationstherapien)?
A: Absolut. Unser wissenschaftliches Team passt Einführungsprotokolle, Behandlungspläne und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
F: Wie sieht der typische Zeitplan für eine Pilot-Wirksamkeitsstudie aus?
A: Die meisten Asthmamodelle sind innerhalb von 4–6 Wochen abgeschlossen, einschließlich Sensibilisierung, Belastung, Behandlung und Endpunktanalyse.
