| Verfügbarkeit: | |
|---|---|
| Menge: | |











Klinisch relevant – LPS-induzierter ALI ähnelt stark dem menschlichen ALI/ARDS mit akuter Entzündung, Leukozyteninfiltration und Lungenödem.
Umfassende Endpunkte – BALF-Zellzahlen (Lymphozyten, Neutrophile, Makrophagen), Zytokinprofilierung (MCP-1, IL-6, IL-10), Lungenhistopathologie (HE, IHC), Lungenödembewertung (Nass-/Trockenverhältnis).
Mechanismusgesteuert – LPS aktiviert die TLR4-Signalübertragung, löst den NF-κB-Signalweg und eine starke Entzündungsreaktion aus und spiegelt eine durch gramnegative Sepsis verursachte Lungenschädigung wider.
Translationaler Wert – Ideal zum Testen entzündungshemmender Medikamente, Zytokininhibitoren, Neutrophilen-Elastase-Inhibitoren und zellbasierter Therapien.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen durchgeführt werden.
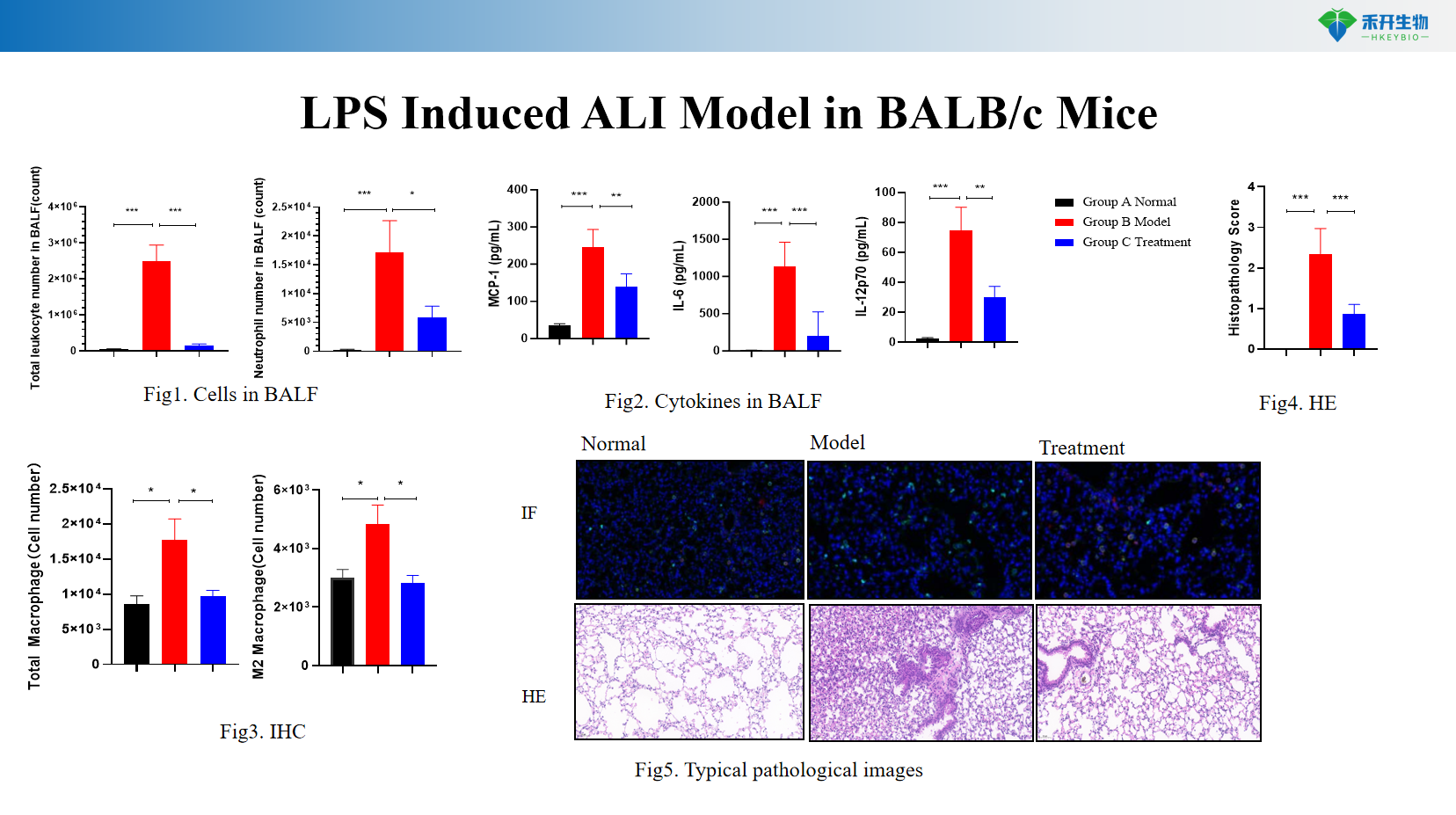
LPS-induziertes ALI-Modell in BALB/c-Mäusen
• Wirksamkeitstests von entzündungshemmenden Medikamenten (Kortikosteroide, NSAIDs), Zytokininhibitoren (Anti-IL-6, Anti-TNF-α) und Neutrophilen-Elastase-Inhibitoren
• Evaluierung der Therapie mit mesenchymalen Stammzellen (MSC) und Behandlungen auf Basis extrazellulärer Vesikel
• Zielvalidierung für TLR4-Signalisierung, NF-κB-Signalweg und Entzündungskaskaden
• Biomarker-Entdeckung (BALF-Zellprofile, Zytokinsignaturen, Lungenverletzungsmarker)
• IND-ermöglichende Pharmakologie- und Toxikologiestudien
Parameter |
Spezifikation |
Art/Stamm |
BALB/c-Maus |
Induktionsmethode |
Intratracheale, intranasale oder intraperitoneale Verabreichung von Lipopolysaccharid (LPS, 5–10 mg/kg) |
Studiendauer |
Akut: 6–48 Stunden nach der LPS-Verabreichung |
Wichtige Endpunkte |
BALF-Zellzahlen (gesamt und differenziell: Neutrophile, Makrophagen, Lymphozyten), BALF-Zytokinspiegel (MCP-1, IL-6, IL-10 durch ELISA), Lungenhistopathologie (HE-Färbung mit Lungenverletzungs-Score), Immunhistochemie (IHC) für Entzündungsmarker, Verhältnis von Feucht-/Trockengewicht der Lunge (Lungenödem), optional: MPO-Aktivität, Marker für oxidativen Stress |
Datenpaket |
Rohdaten, Analyseberichte, BALF-Zellzahlen, ELISA-Ergebnisse, Histologie-Objektträger (HE, IHC), Bioinformatik (optional) |
F: Wie löst LPS bei Mäusen eine akute Lungenschädigung aus?
A: LPS bindet an TLR4 auf Immunzellen, aktiviert die NF-κB- und MAPK-Signalwege und führt zu einer starken Entzündungsreaktion mit Zytokinfreisetzung (IL-6, TNF-α, MCP-1), Neutrophilenrekrutierung in der Lunge, erhöhter Gefäßpermeabilität und Alveolarschäden, was der durch gramnegative Sepsis induzierten ALI sehr ähnlich ist.
F: Was sind die wichtigsten Ähnlichkeiten mit menschlichem ALI/ARDS?
A: Das Modell weist eine Neutrophileninfiltration, erhöhte proinflammatorische Zytokine, Lungenödeme und histopathologische Merkmale (Alveolarverdickung, Bildung hyaliner Membranen) auf, die mit denen des menschlichen ALI/ARDS identisch sind.
F: Kann dieses Modell für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche LPS-Dosen, Verabreichungswege, Zeitpunkte)?
A: Absolut. Unser wissenschaftliches Team passt LPS-Dosierungsschemata, Verabreichungswege und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
