| Verfügbarkeit: | |
|---|---|
| Menge: | |











Breites Modellportfolio – Hapten-, Zytokin-, Allergen- und Vitamin-D-Analogon-Modelle, die akute, chronische und Th2/Th17/Th22-dominante AD-Endotypen abdecken.
Mehrere Arten/Stämme – BALB/c (Th2-anfällig), C57BL/6 (Th1/Th17-anfällig) und SD-Ratte verfügbar.
Umfassende Endpunkte – Körpergewicht, Ohrdicke, Hautwert, Juckreizereignisse, Serum-IgE, Zytokinprofilierung (IL-4, IL-13, IL-17, IL-36), Histopathologie (HE, Toluidinblau), epidermale Dicke.
Translationaler Wert – Ideal zum Testen von JAK-Inhibitoren, Biologika (Anti-IL-4Rα, Anti-IL-13), PDE4-Inhibitoren und topischen Wirkstoffen.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen durchgeführt werden.
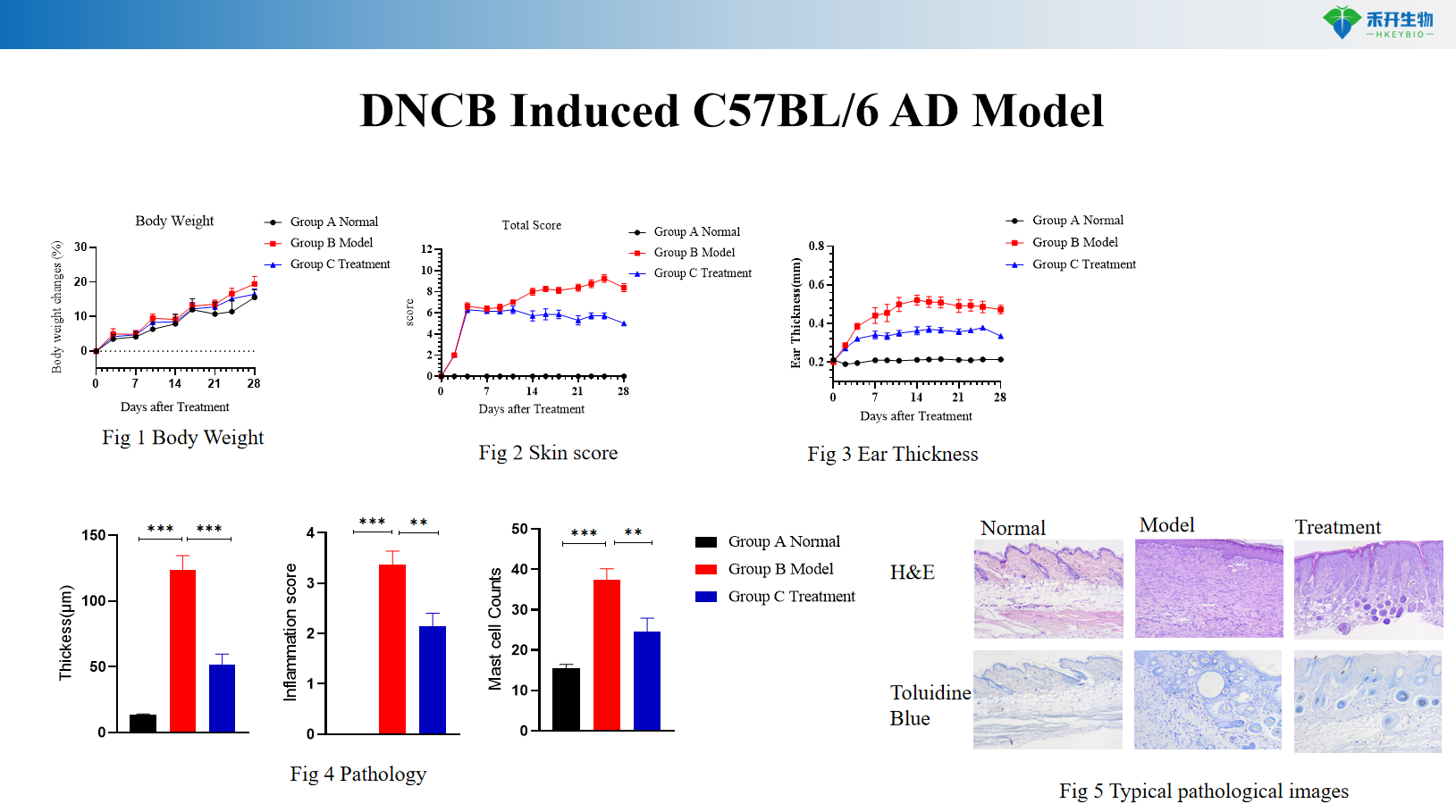
DNCB-induziertes C57BL/6 AD-Modell
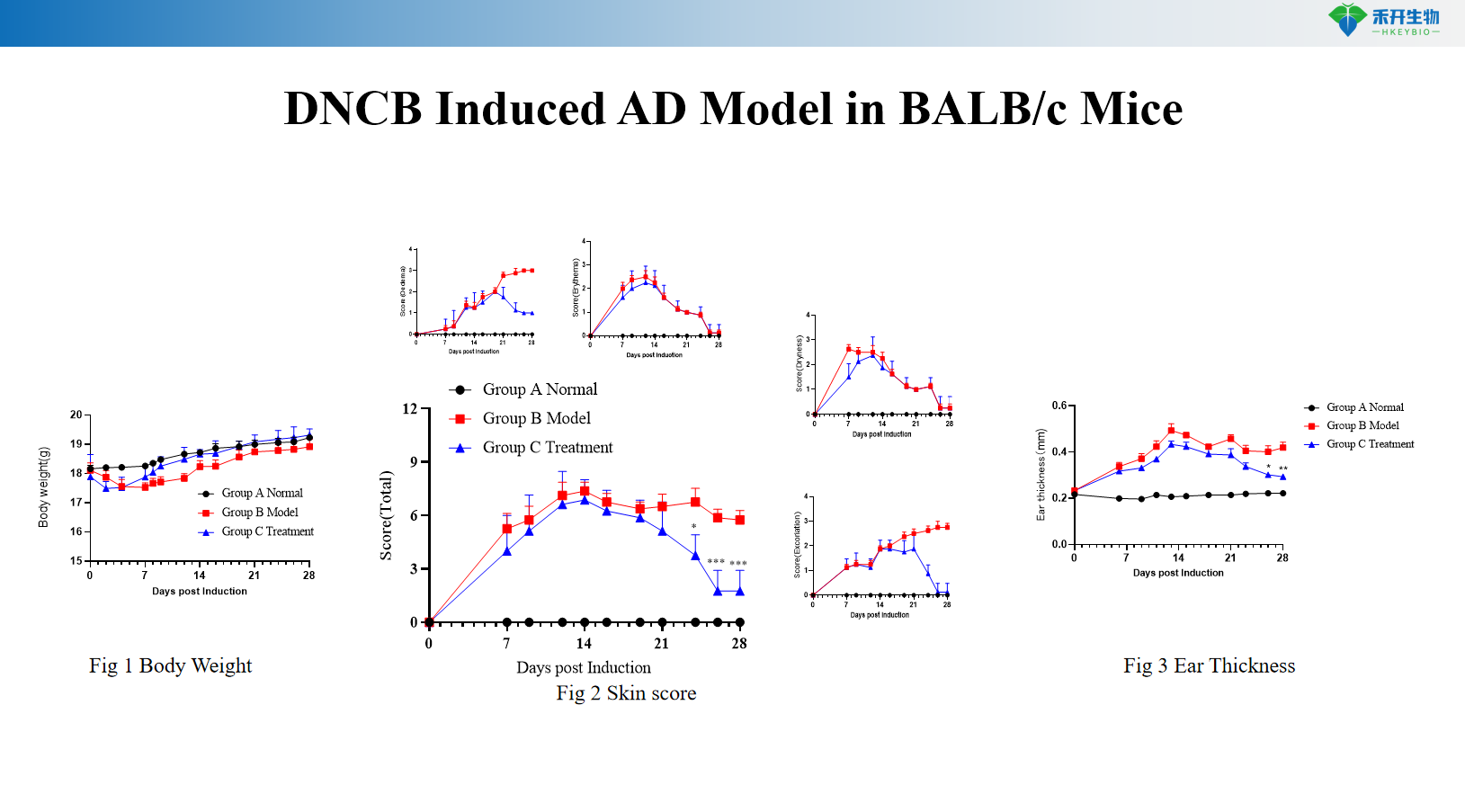
DNCB-induziertes AD-Modell in BALB/c-Mäusen
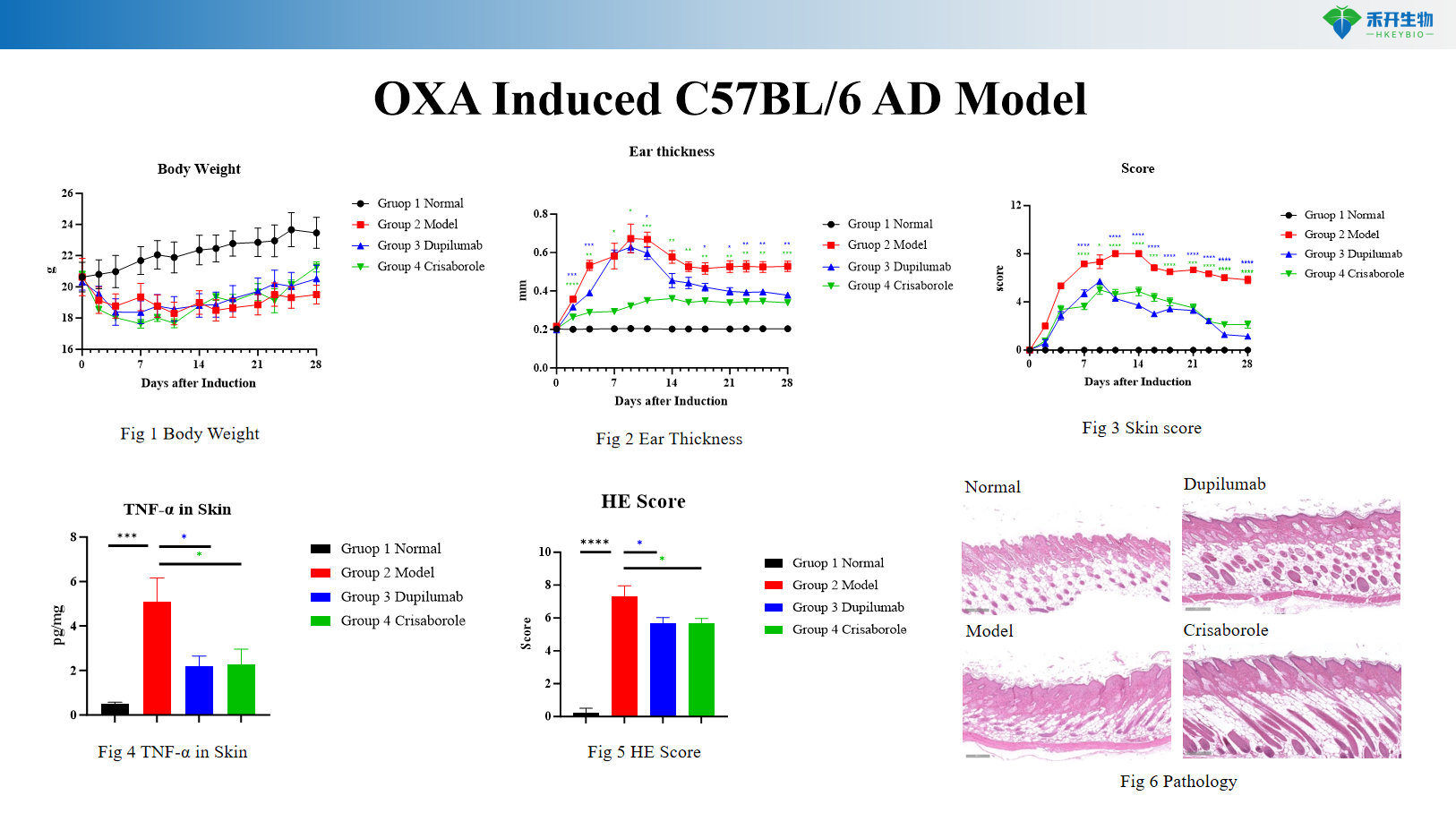
OXA-induziertes C57BL/6 AD-Modell
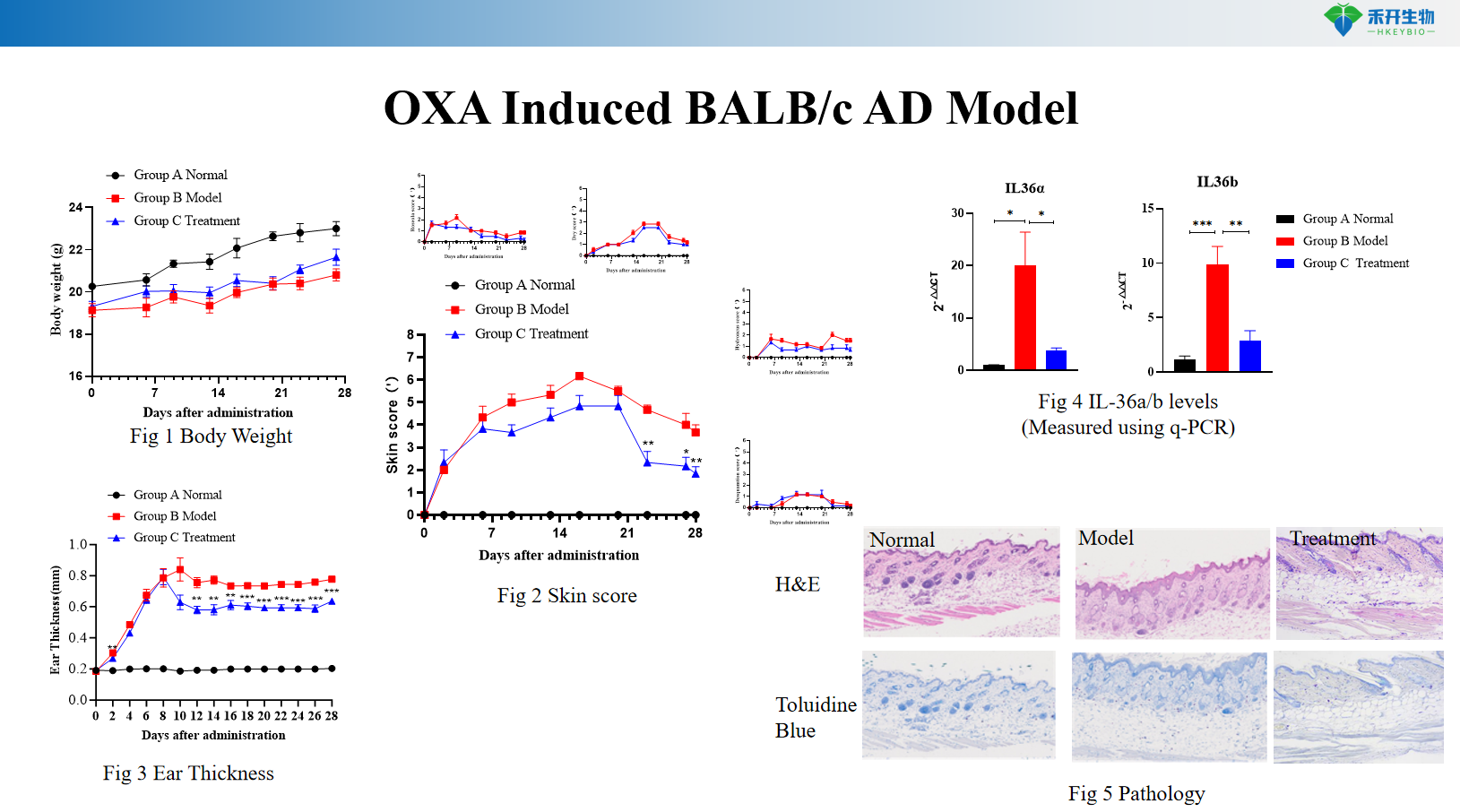
OXA-induziertes BALB/c AD-Modell
MC903-induziertes C57BL/6 AD-Modell

MC903 Induziertes BALB/c AD-Modell


MC903&OXA-induziertes AD-Modell in BALB/c

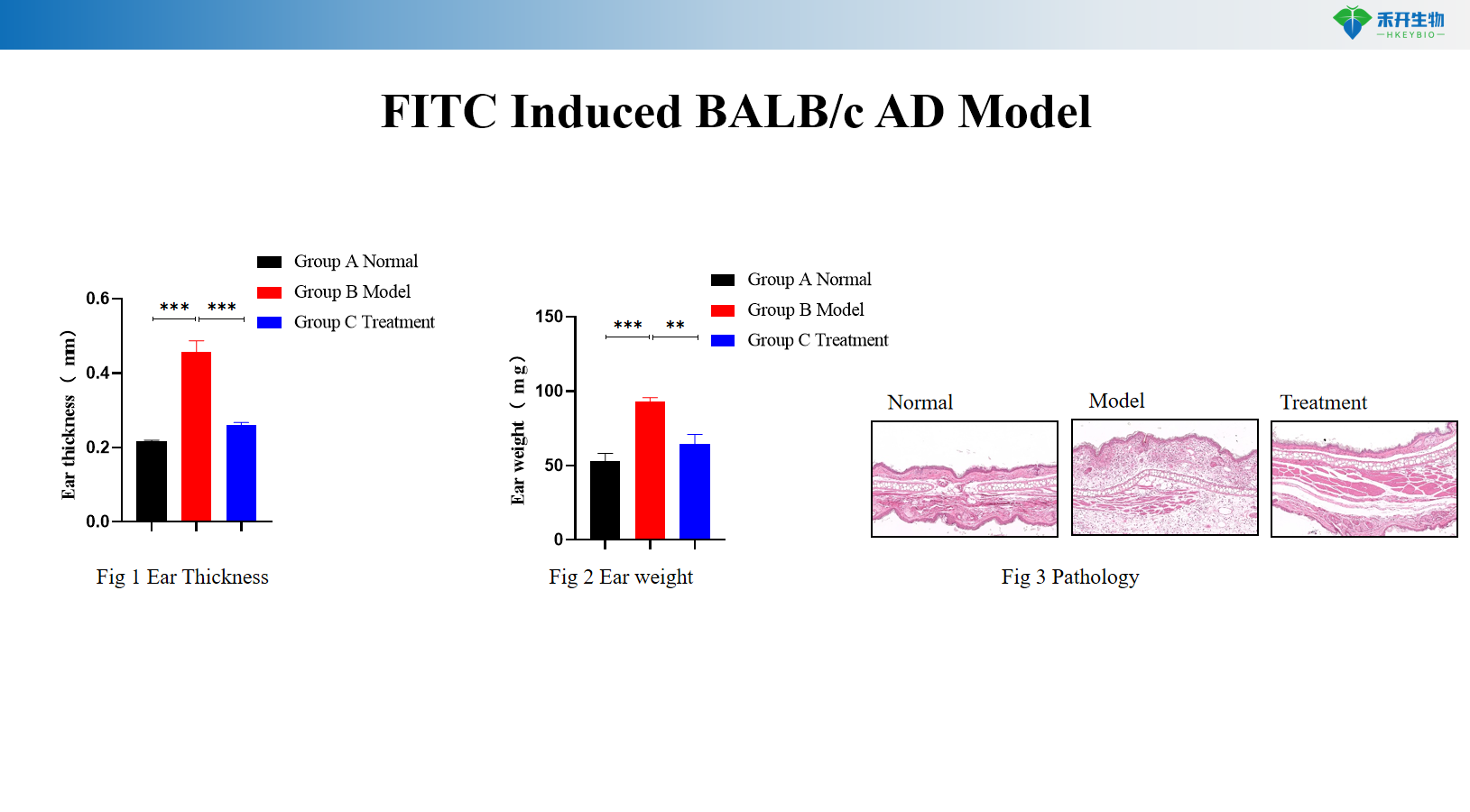
FITC-induziertes BALB/c AD-Modell
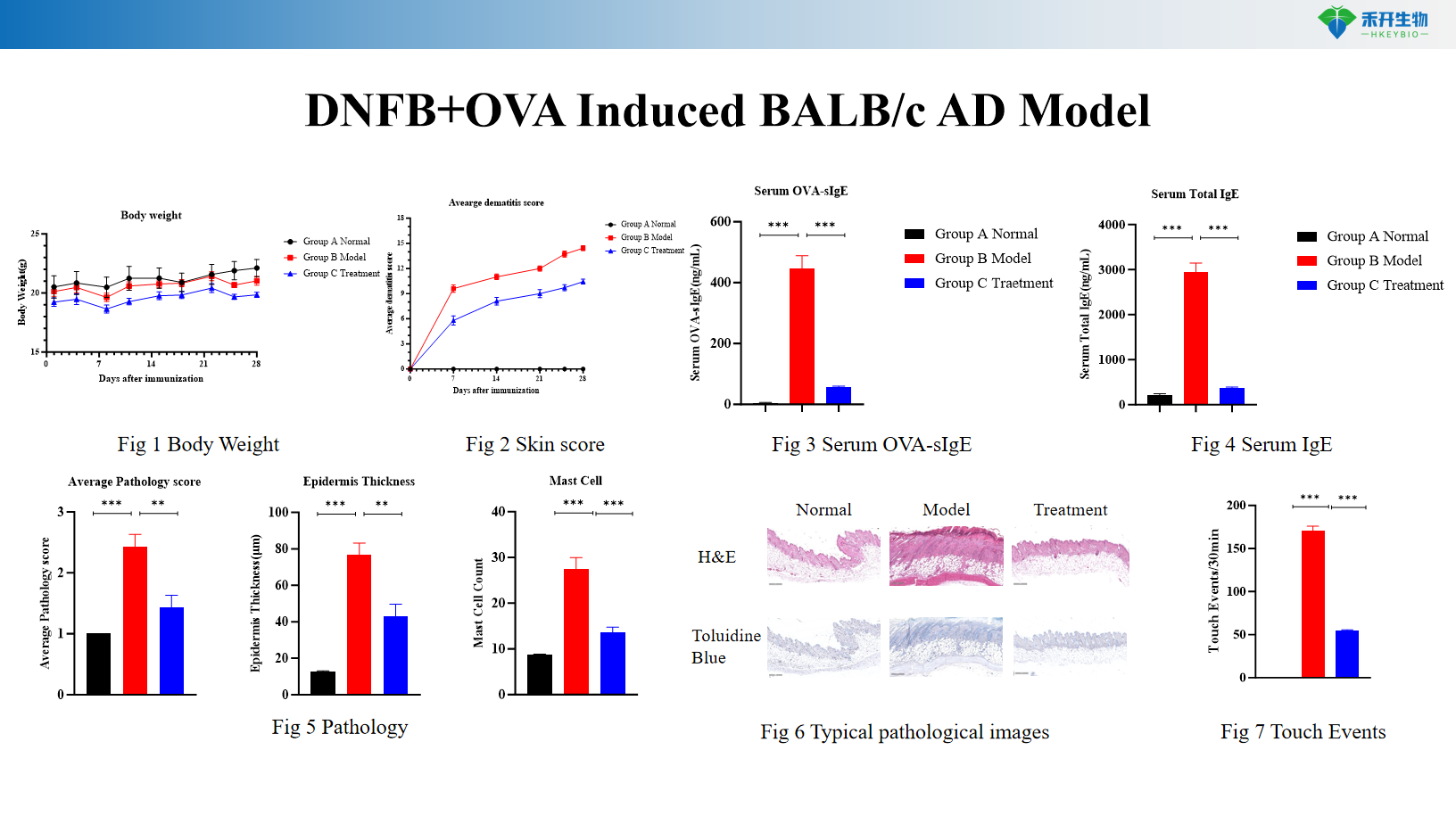
DNFB+OVA-induziertes BALB/c AD-Modell
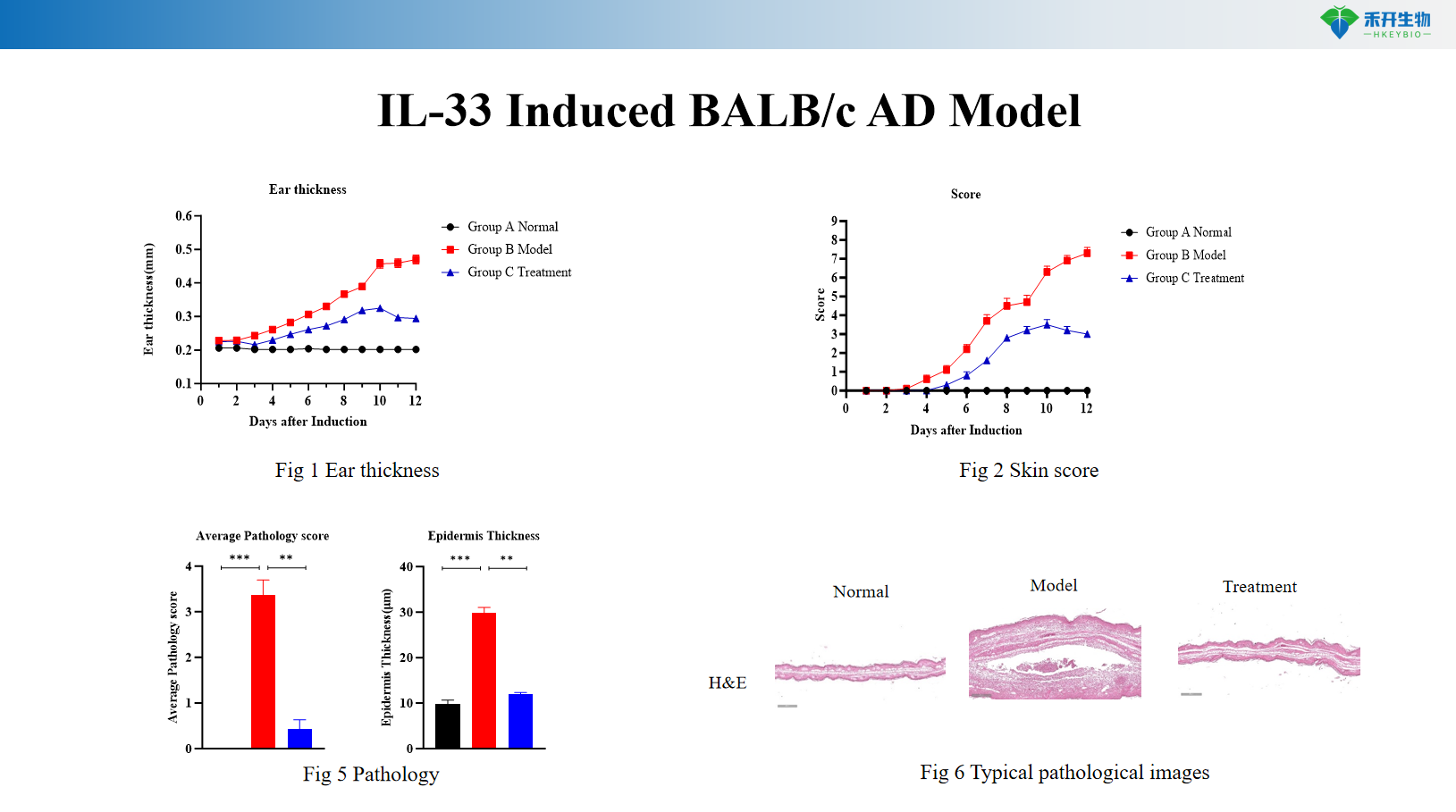
IL-33-induziertes BALB/c AD-Modell
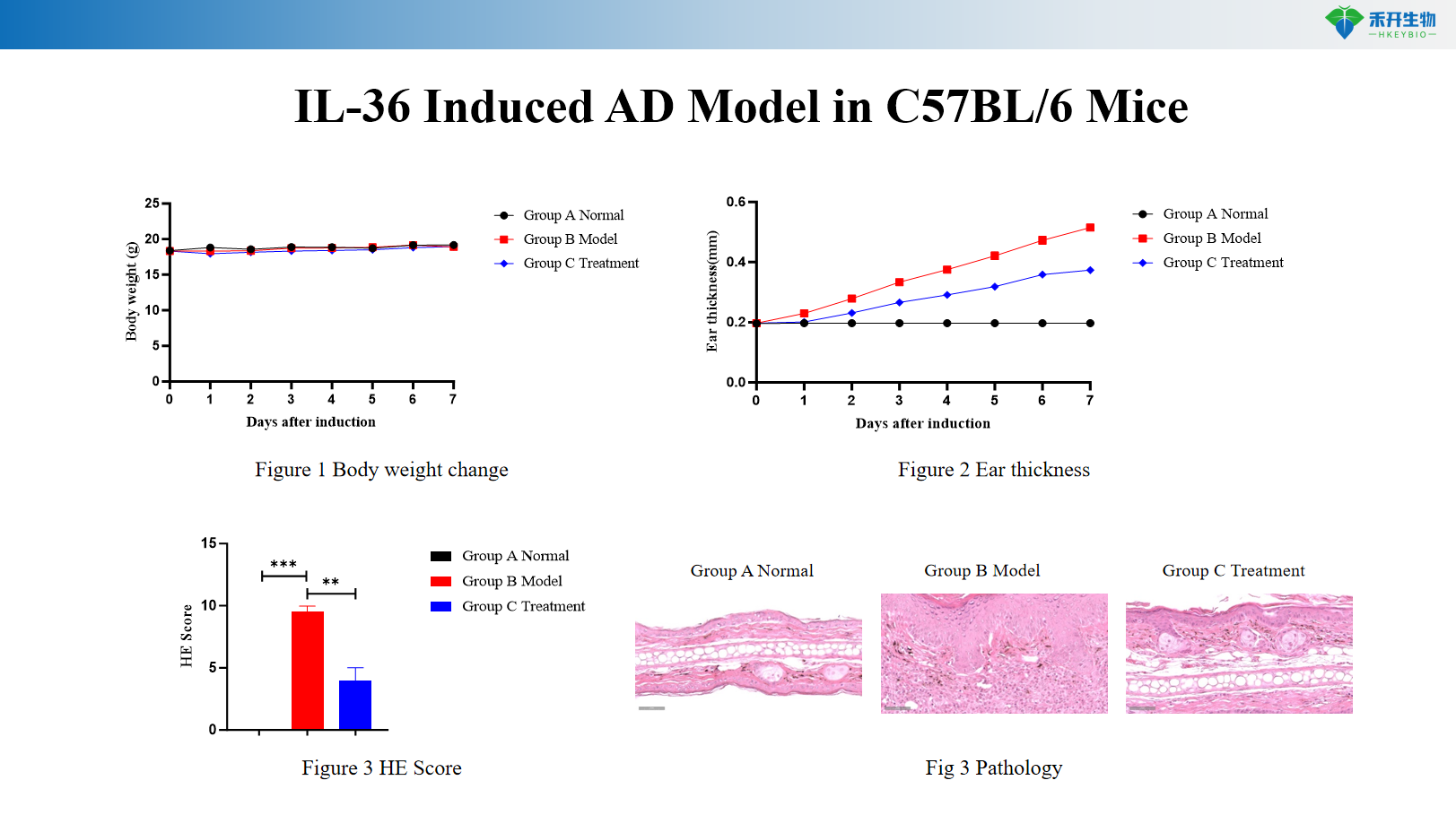
IL-36-induziertes AD-Modell in C57BL/6-Mäusen
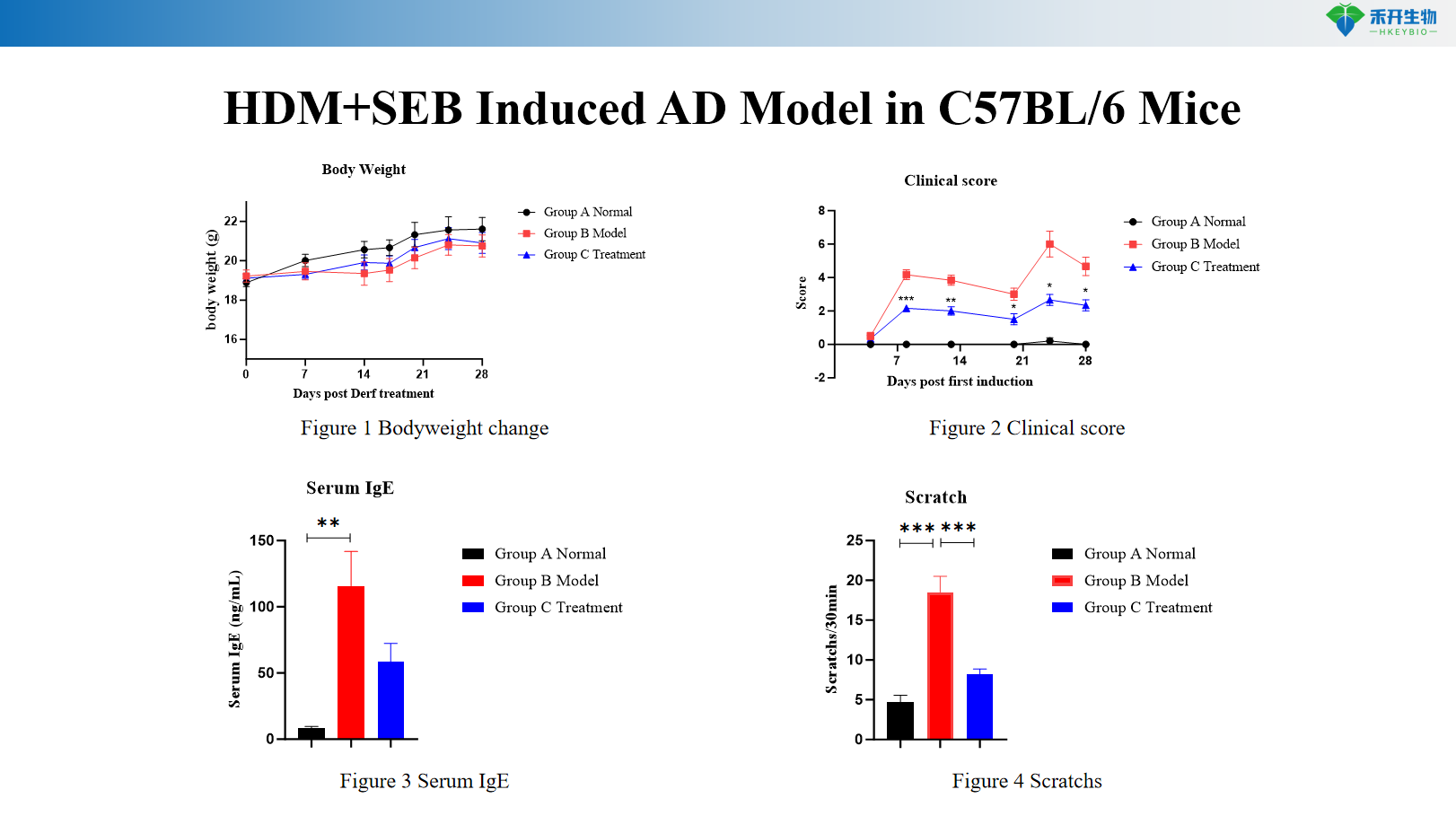
HDM+SEB-induziertes AD-Modell in C57BL/6-Mäusen
• Wirksamkeitsprüfung von topischen und systemischen AD-Therapien (JAK-Inhibitoren, PDE4-Inhibitoren, Biologika gegen IL-4/13, IL-31, IL-33, TSLP)
• Zielvalidierung für Th2-, Th17-, Th22- und Juckreizpfade
• Entdeckung von Biomarkern (IgE, Zytokinsignaturen, Hautbarriereproteine)
• Wirkmechanismusstudien (MOA).
• IND-ermöglichende Pharmakologie- und Toxikologiestudien
Parameter |
Spezifikation |
Art/Stamm |
Maus (BALB/c, C57BL/6); Ratte (SD) |
Induktionsmethode |
Haptene (DNCB, OXA, DNFB+OVA, FITC), Vitamin-D-Analogon (MC903), Zytokine (IL-33, IL-36), Allergene (HDM+SEB), Kombinationen (MC903+OXA) |
Studiendauer |
7–28 Tage (je nach Modell) |
Wichtige Endpunkte |
Körpergewicht, Ohrdicke, klinischer Hautwert, Juckreizereignisse (Kratzen), Serum-Gesamt-IgE und Antigen-spezifisches IgE, Zytokinspiegel (IL-4, IL-13, IL-17, IL-36, TNF-α), Histopathologie (H&E, Toluidinblau), Epidermisdicke, Immunzellinfiltration (FACS/IHC) |
Datenpaket |
Rohdaten, Analyseberichte, klinische Fotos, histologische Objektträger, Durchflusszytometriedateien, Bioinformatik (optional) |
F: Wie wähle ich das richtige AD-Modell für meinen Medikamentenkandidaten aus?
A: Berücksichtigen Sie den Wirkmechanismus Ihres Medikaments: Th2-gerichtete Biologika (z. B. Anti-IL-4Rα) werden am besten in Hapten- oder MC903-Modellen evaluiert; Th17-verwandte Verbindungen können für IL-36- oder HDM+SEB-Modelle geeignet sein. BALB/c-Mäuse zeigen stärkere Th2-Reaktionen, während C57BL/6 ausgewogenere Th1/Th17-Profile zeigen. Unser wissenschaftliches Team kann die Modellauswahl basierend auf Ihrem spezifischen Ziel unterstützen.
F: Können diese Modelle für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche Dosierungspläne, Kombinationstherapien)?
A: Absolut. Unser wissenschaftliches Team passt Einführungsprotokolle, Behandlungspläne und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
F: Wie sieht der typische Zeitplan für eine Pilot-Wirksamkeitsstudie aus?
A: Die meisten AD-Modelle sind innerhalb von 2–4 Wochen abgeschlossen, einschließlich der Sensibilisierungs-/Provokations- und Behandlungsphasen. Spezifische Zeitpläne hängen von der Modellauswahl und den Endpunkten ab.
