| Disponibilité : | |
|---|---|
| Quantité : | |











Large gamme de modèles – couvrant le SCR éosinophile (papaïne), le SRC induit par la protéase fongique (Aspergillus), le SCR associé aux superantigènes (SEB) et la rhinite allergique classique (OVA).
Plusieurs souches – C57BL/6 et BALB/c pour s'adapter à différents fonds génétiques et préférences Th1/Th2.
Critères d'évaluation composites : poids corporel, nombre de cellules de lavage nasal (éosinophiles, cellules totales), IgE sériques (IgE totales et spécifiques à l'OVA), comportement de grattage nasal, histopathologie de la muqueuse nasale (HE) et analyse des cytokines (IL-33, cytokines Th2).
Valeur translationnelle – Idéal pour tester les corticostéroïdes, les antihistaminiques, les produits biologiques (anti-IgE, anti-IL-5, anti-IL-4Rα) et les nouveaux immunomodulateurs.
IND Ready Packet – La recherche peut être menée conformément aux principes BPL.
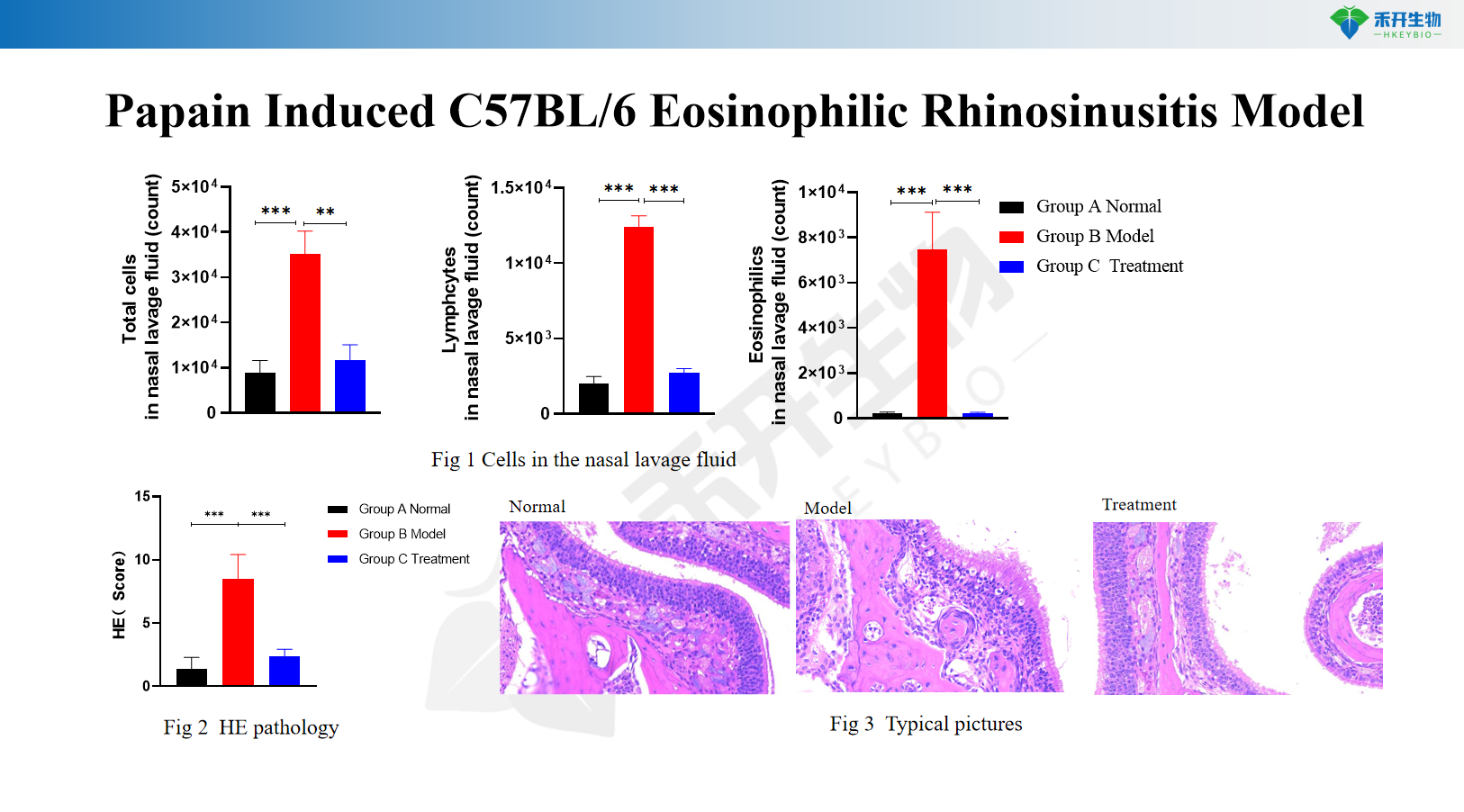
Modèle de sinusite à éosinophiles C57BL/6 induite par la papaïne
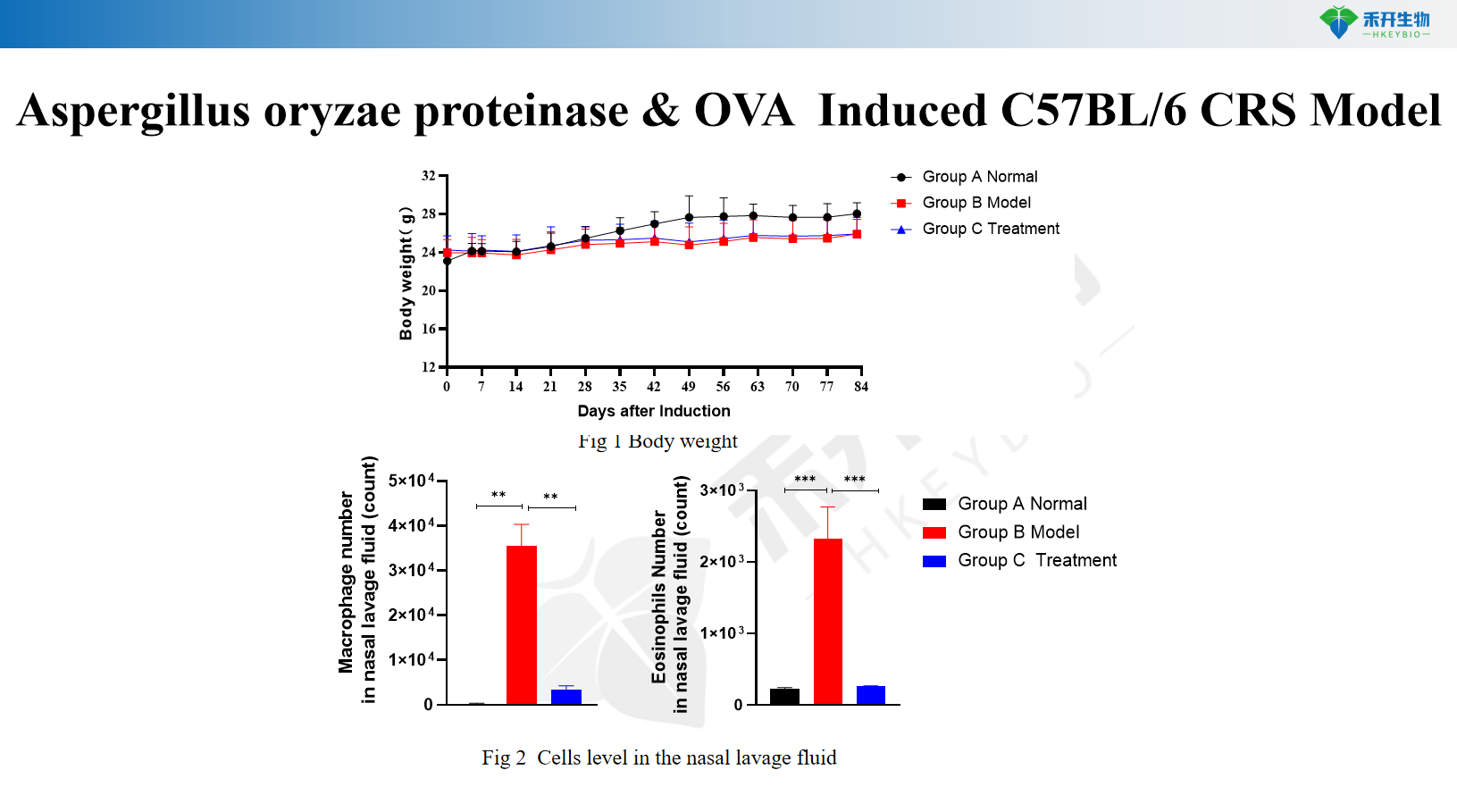
Modèle C57BL/6 CRS induit par la protéase d'Aspergillus oryzae et l'OVA
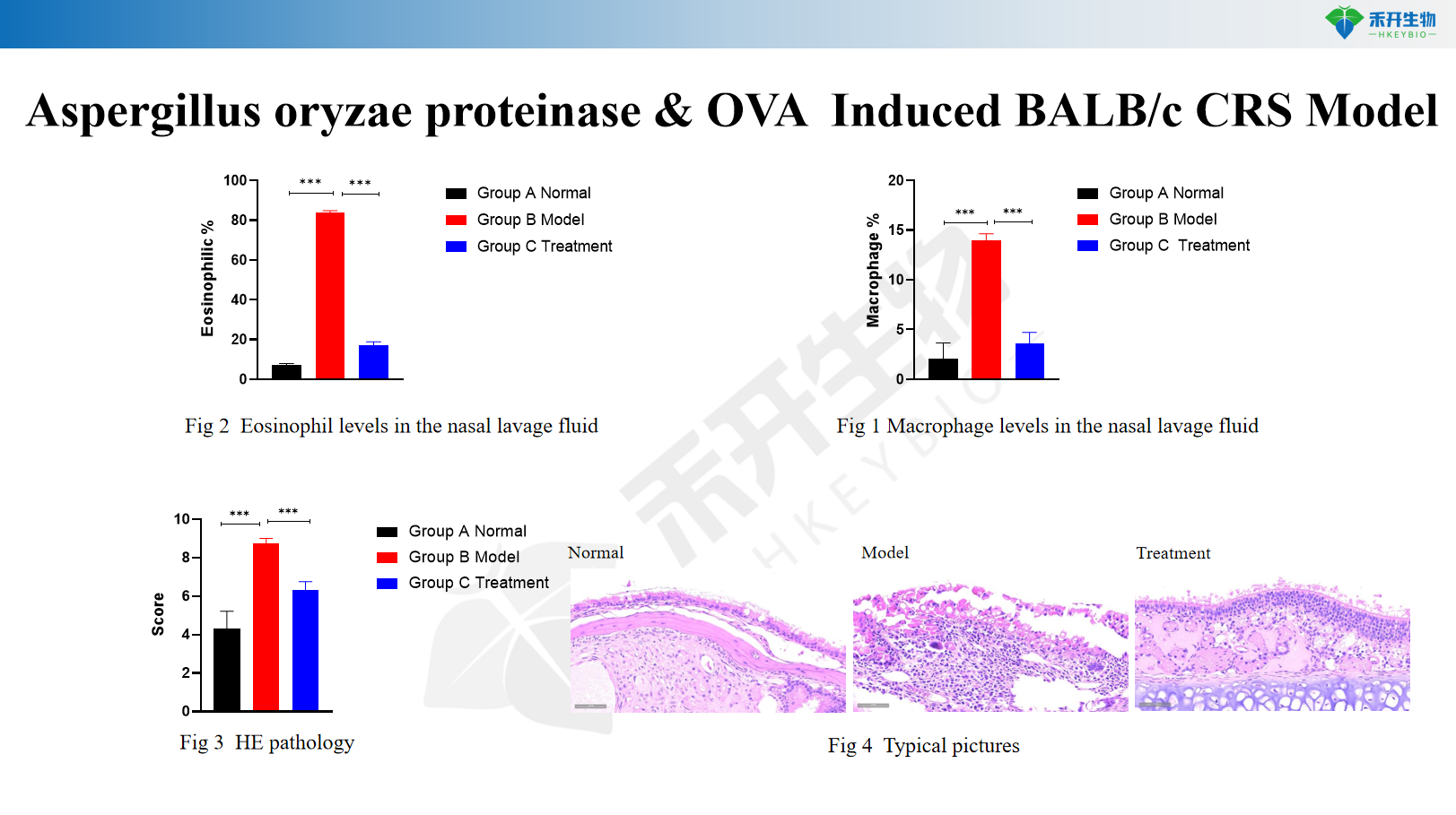
Modèle BALB/c CRS induit par la protéase d'Aspergillus oryzae et l'OVA
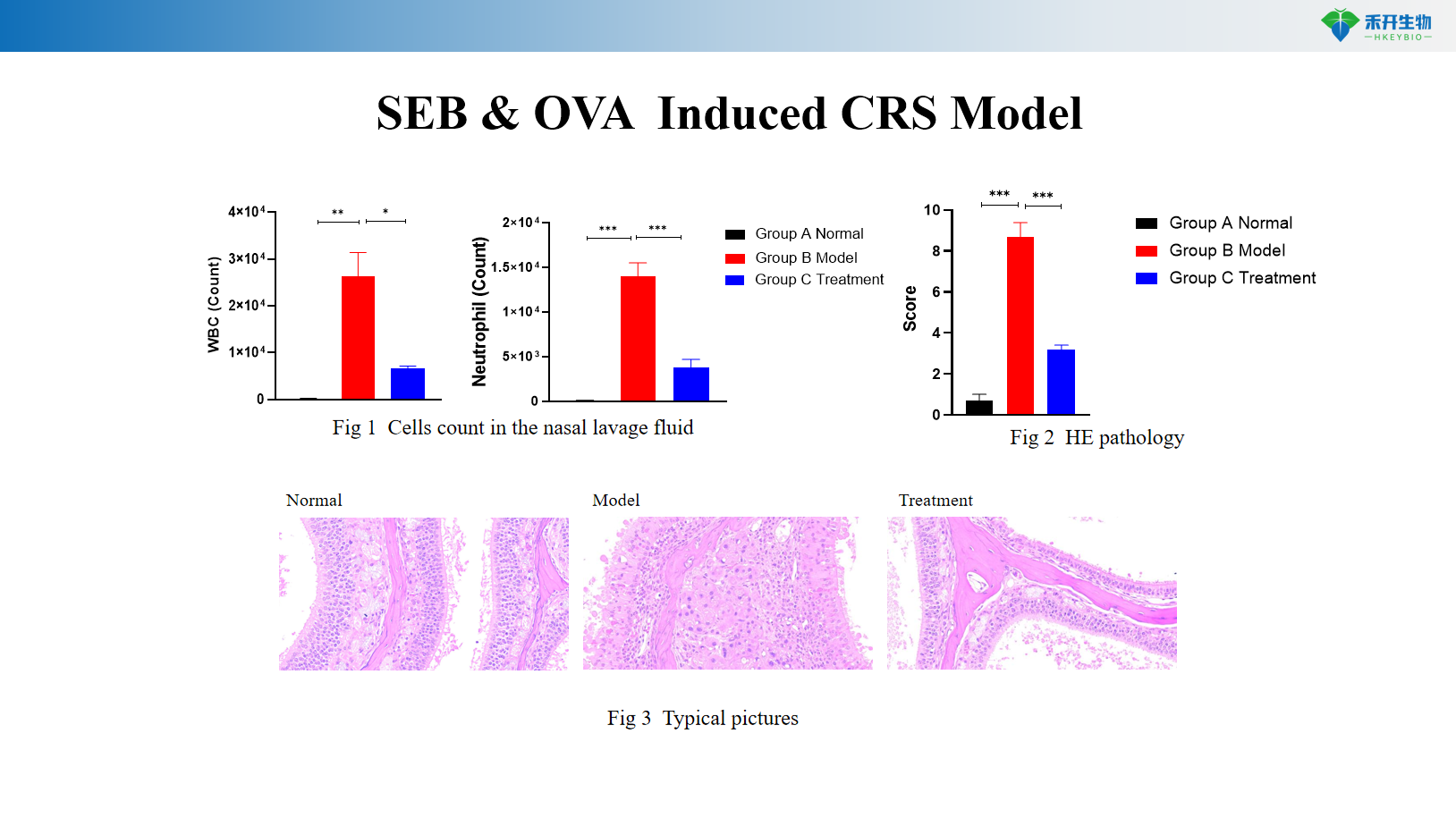
Modèle CRS induit par SEB et OVA
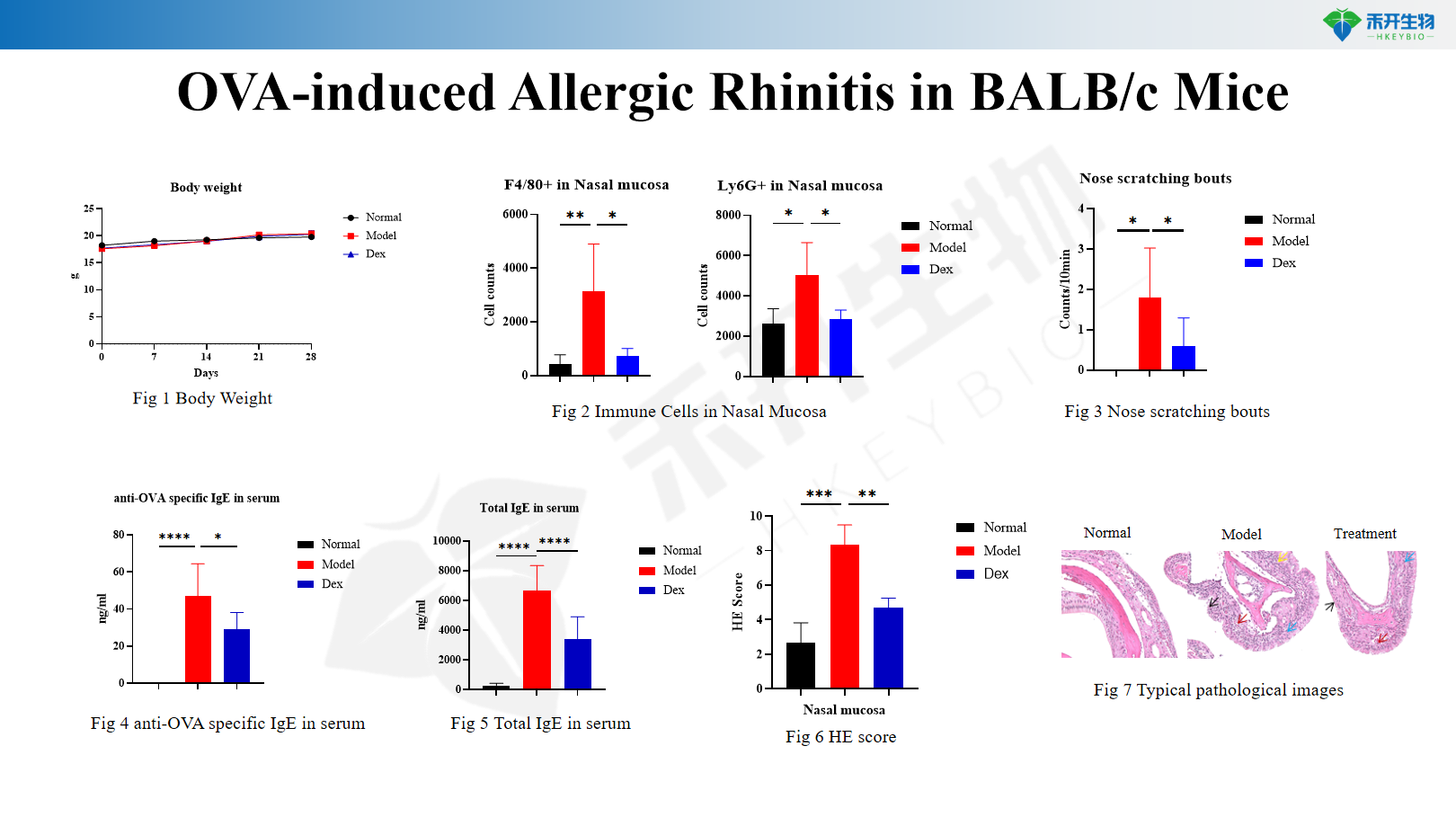
Rhinite allergique induite par l'OVA chez la souris BALB/c
• Tests d'efficacité des corticostéroïdes intranasaux et systémiques, des antihistaminiques et des décongestionnants
• Évaluer les produits biologiques ciblant la voie Th2 (anti-IL-4Rα, anti-IL-5, anti-IL-13, anti-IgE)
• Validation cible des cytokines d'origine épithéliale (TSLP, IL-33, IL-25) et des voies d'activation des protéases
• Découverte de biomarqueurs (IgE, peroxydase des éosinophiles, signature des cytokines)
• Études de pharmacologie et de toxicologie pour soutenir l'IND
portée |
Spécification |
Espèce/souche |
Souris (C57BL/6, BALB/c) |
méthode d'induction |
Papaïne (protéase); Aspergillus + OVA ; SEB + OVA ; OVA + alun |
temps d'étude |
3 à 6 semaines (phase de sensibilisation + challenge) |
point final critique |
Poids corporel, nombre de cellules de lavage nasal (total et différentiel), IgE totales sériques et IgE spécifiques à l'OVA, comportement de grattage du nez (rhinite allergique), histopathologie de la muqueuse nasale (score HE pour l'inflammation, l'infiltration des éosinophiles, l'hyperplasie des cellules caliciformes), taux de cytokines dans les tissus nasaux/liquide de lavage (IL-4, IL-5, IL-13, IL-33) |
paquet |
Données brutes, rapport d'analyse, cytologie de lavage nasal, résultats ELISA, coupes histologiques, données comportementales, bioinformatique (facultatif) |
Q : Comment puis-je choisir le bon modèle pour mon candidat-médicament ?
R : Pour les SCR éosinophiles, des modèles de papaïne ou de protéase aspergillus sont recommandés. Pour le CRS lié aux superantigènes, le modèle SEB+OVA convient. Pour la rhinite allergique typique, le modèle OVA est le choix standard. Les souris BALB/c présentent une réponse Th2 plus forte, tandis que C57BL/6 permet l'utilisation de lignées transgéniques. Notre équipe scientifique peut guider la sélection de modèles en fonction de vos objectifs spécifiques.
Q : Quel rôle l'activité de la protéase joue-t-elle dans le modèle CRS ?
R : Les protéases (papaïne, aspergillus) perturbent les jonctions serrées épithéliales, entraînant un dysfonctionnement de la barrière et la libération de cytokines épithéliales (IL-33, TSLP) responsables de l'inflammation de type 2 et de l'infiltration des éosinophiles, similaires à la physiopathologie du SRC humain.
Q : Ces modèles peuvent-ils être utilisés pour les études de support IND ?
Réponse : Oui. Les études peuvent être menées selon les principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différentes doses d'allergènes, programmes de sensibilisation) ?
Réponse : Bien sûr. Notre équipe scientifique adapte les protocoles d’induction, les plans de traitement et les analyses des paramètres à votre candidat médicament spécifique.
