| Verfügbarkeit: | |
|---|---|
| Menge: | |











Breites Modellportfolio – deckt eosinophiles CRS (Papain), Pilzprotease-induziertes CRS (Aspergillus), Superantigen-assoziiertes CRS (SEB) und klassische allergische Rhinitis (OVA) ab.
Mehrere Stämme – C57BL/6 und BALB/c, um unterschiedlichen genetischen Hintergründen und Th1/Th2-Präferenzen gerecht zu werden.
Zusammengesetzte Endpunkte – Körpergewicht, Anzahl der Nasenspülzellen (Eosinophile, Gesamtzellen), Serum-IgE (Gesamt-IgE und OVA-spezifisch), Nasenkratzverhalten, Histopathologie der Nasenschleimhaut (HE) und Zytokinanalyse (IL-33, Th2-Zytokine).
Translationaler Wert – Ideal zum Testen von Kortikosteroiden, Antihistaminika, Biologika (Anti-IgE, Anti-IL-5, Anti-IL-4Rα) und neuartigen Immunmodulatoren.
IND Ready Packet – Forschung kann gemäß den GLP-Grundsätzen durchgeführt werden.
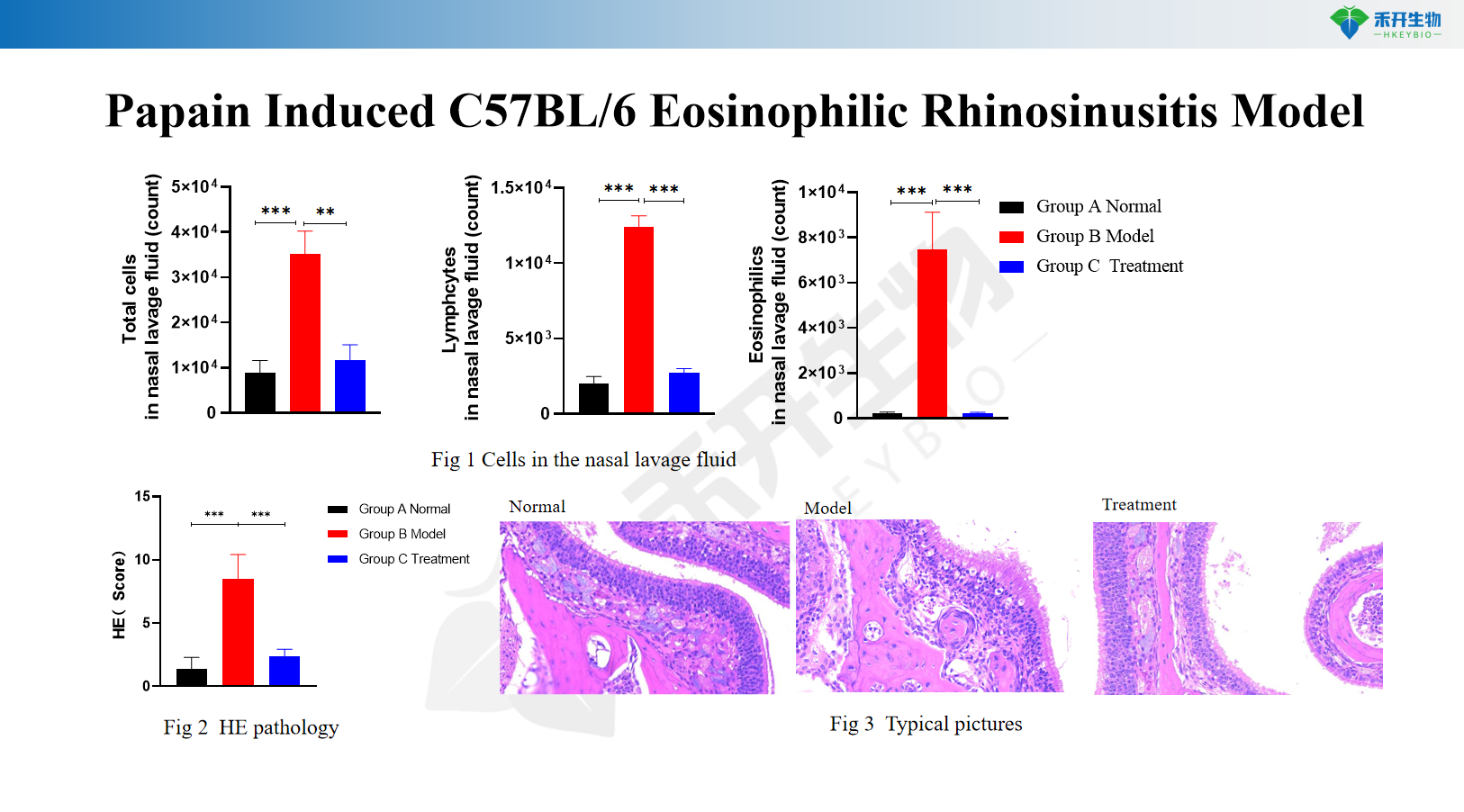
Papain-induziertes C57BL/6-Modell der eosinophilen Sinusitis
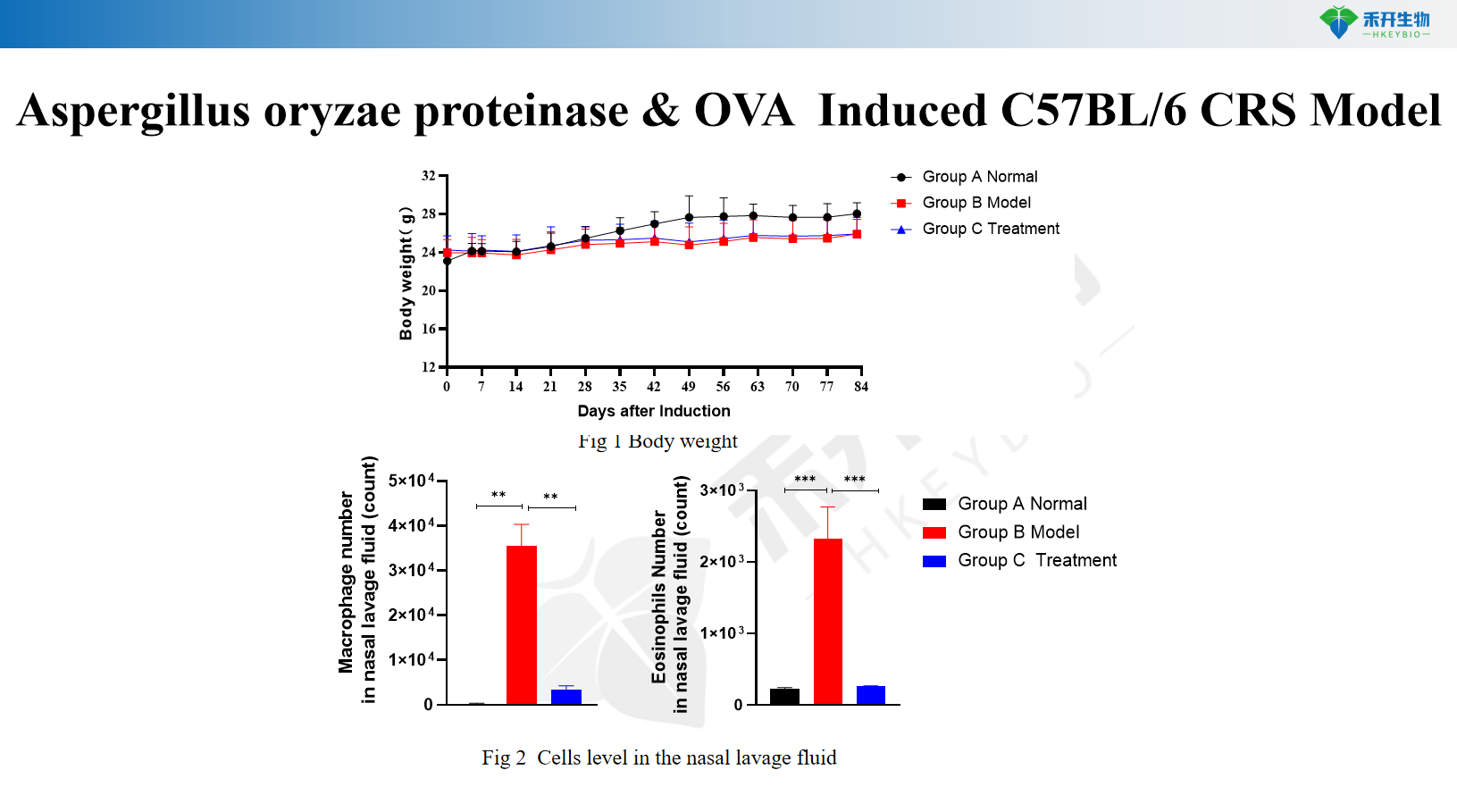
C57BL/6 CRS-Modell, induziert durch Aspergillus oryzae-Protease und OVA
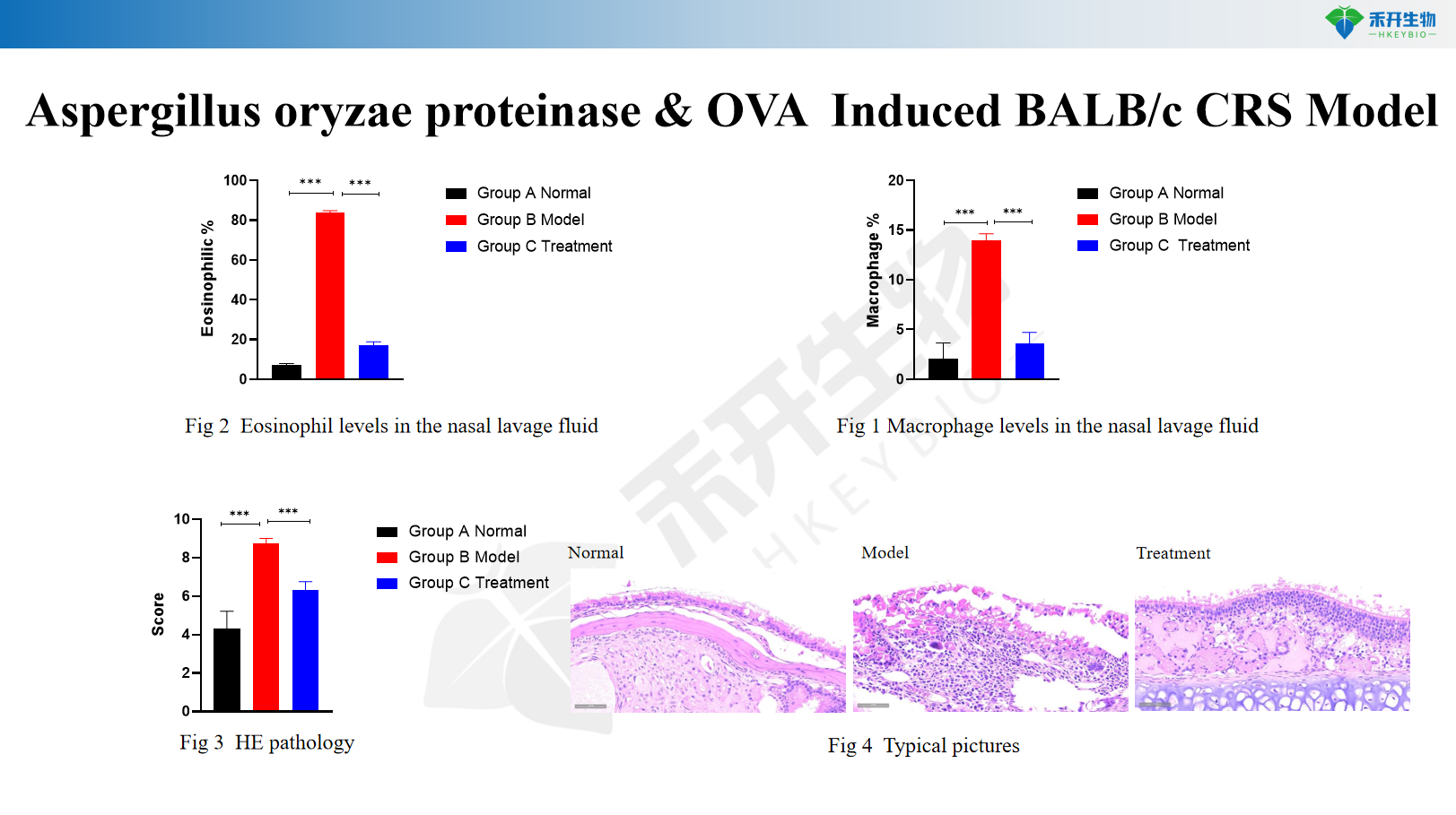
BALB/c CRS-Modell, induziert durch Aspergillus oryzae-Protease und OVA
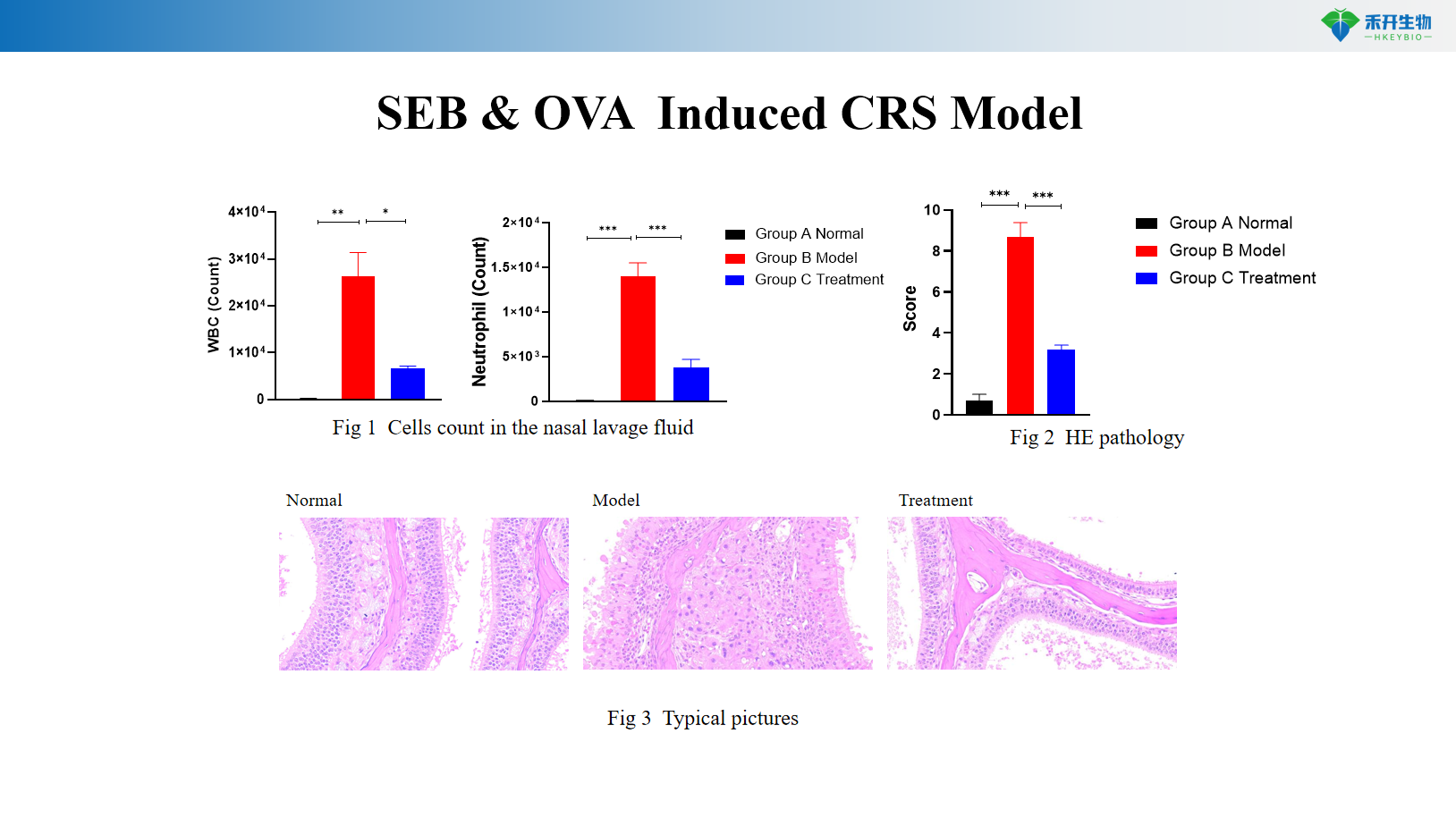
SEB- und OVA-induziertes CRS-Modell
OVA-induzierte allergische Rhinitis bei BALB/c-Mäusen
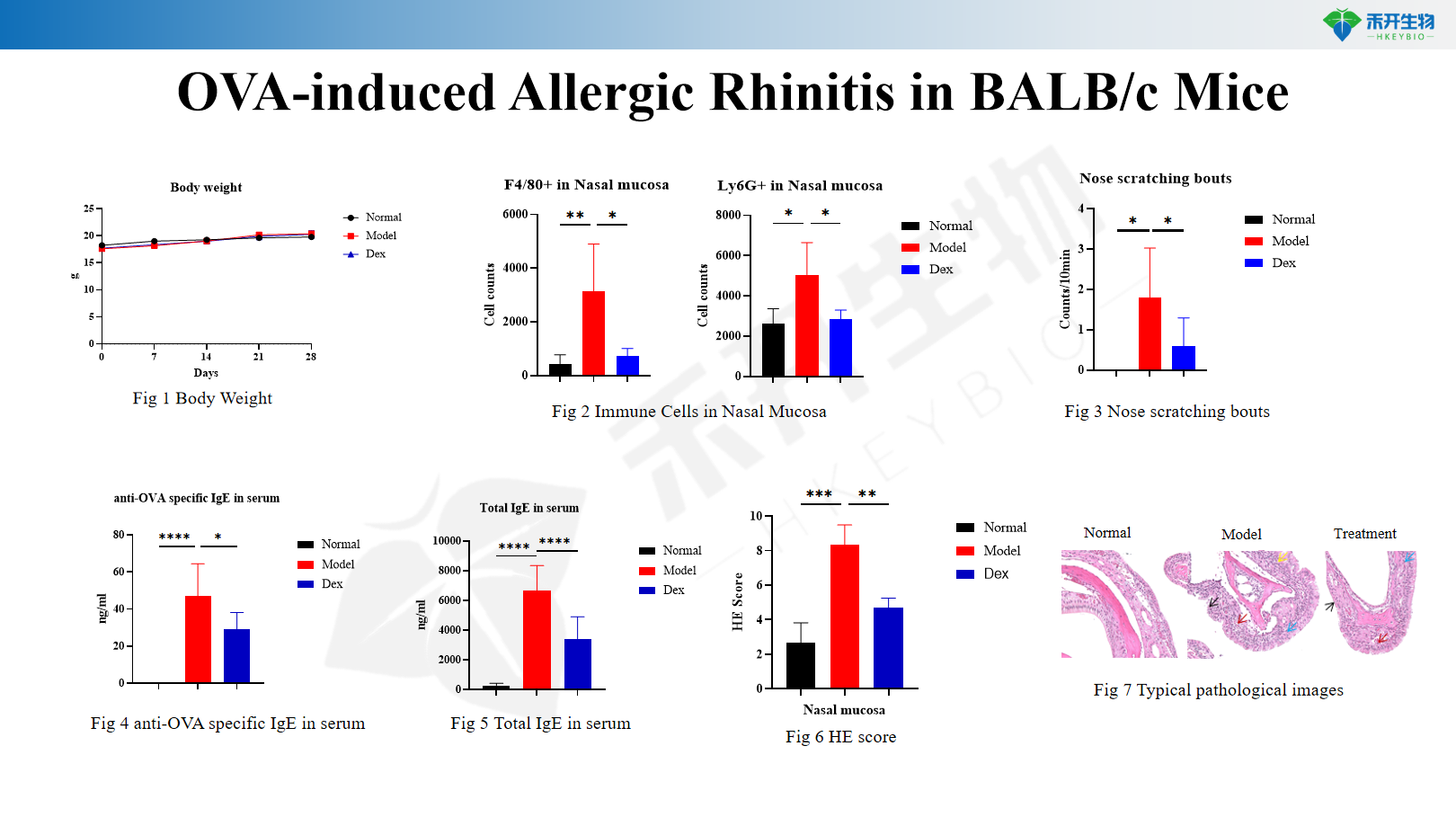
• Wirksamkeitstests von intranasalen und systemischen Kortikosteroiden, Antihistaminika und abschwellenden Mitteln
• Bewerten Sie Biologika, die auf den Th2-Signalweg abzielen (Anti-IL-4Rα, Anti-IL-5, Anti-IL-13, Anti-IgE).
• Zielvalidierung von epithelialen Zytokinen (TSLP, IL-33, IL-25) und Protease-Aktivierungswegen
• Entdeckung von Biomarkern (IgE, eosinophile Peroxidase, Zytokinsignatur)
• Pharmakologische und toxikologische Studien zur Unterstützung von IND
Umfang |
Spezifikation |
Art/Stamm |
Maus (C57BL/6, BALB/c) |
Induktionsmethode |
Papain (Protease); Aspergillus + OVA; SEB + OVA; OVA + Alaun |
Lernzeit |
3–6 Wochen (Sensibilisierungs- und Provokationsphase) |
kritischer Endpunkt |
Körpergewicht, Nasenspülzellzahl (gesamt und differenziell), Serum-Gesamt-IgE und OVA-spezifisches IgE, Nasenkratzverhalten (allergische Rhinitis), Histopathologie der Nasenschleimhaut (HE-Score für Entzündung, Eosinophileninfiltration, Becherzellhyperplasie), Zytokinspiegel im Nasengewebe/Spülflüssigkeit (IL-4, IL-5, IL-13, IL-33) |
Paket |
Rohdaten, Analysebericht, Nasenspülzytologie, ELISA-Ergebnisse, histologische Schnitte, Verhaltensdaten, Bioinformatik (optional) |
F: Wie wähle ich das richtige Modell für meinen Medikamentenkandidaten aus?
A: Für eosinophiles CRS werden Papain- oder Aspergillus-Protease-Modelle empfohlen. Für Superantigen-bezogenes CRS ist das SEB+OVA-Modell geeignet. Bei typischer allergischer Rhinitis ist das OVA-Modell die Standardwahl. BALB/c-Mäuse zeigen eine stärkere Th2-Antwort, wohingegen C57BL/6 die Verwendung transgener Linien ermöglicht. Unser wissenschaftliches Team kann die Modellauswahl basierend auf Ihren spezifischen Zielen steuern.
F: Welche Rolle spielt die Proteaseaktivität im CRS-Modell?
A: Proteasen (Papain, Aspergillus) stören epitheliale Tight Junctions, was zu einer Barrierefunktionsstörung und der Freisetzung von epithelialen Zytokinen (IL-33, TSLP) führt, die Typ-2-Entzündungen und die Infiltration von Eosinophilen vorantreiben, ähnlich der menschlichen CRS-Pathophysiologie.
F: Können diese Modelle für IND-Unterstützungsstudien verwendet werden?
Antwort: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche Allergendosis, Sensibilisierungspläne)?
Antwort: Natürlich. Unser wissenschaftliches Team erstellt maßgeschneiderte Induktionsprotokolle, Behandlungspläne und Endpunktanalysen für Ihren spezifischen Medikamentenkandidaten.
