| Disponibilité : | |
|---|---|
| Quantité : | |











Cliniquement pertinent - Deux modèles capturent les caractéristiques clés de l'EoE humaine : l'infiltration des éosinophiles, l'inflammation Th2 et le dysfonctionnement épithélial.
Diversité mécanistique : le modèle IL-33 reflète la réponse Th2 induite par l'alarme ; Le modèle OXA représente une inflammation allergique induite par l’haptène.
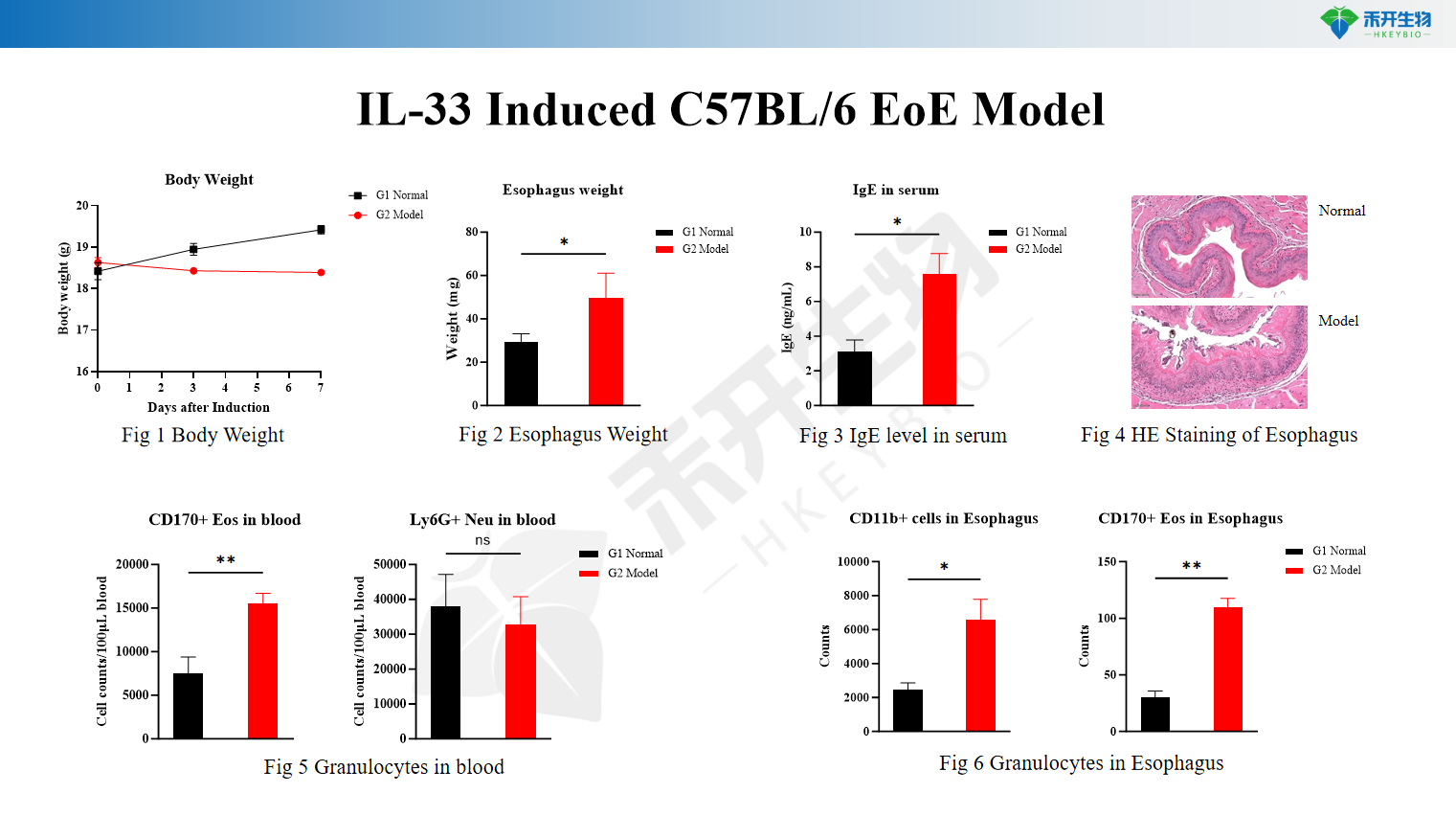
Critères d'évaluation quantifiables - poids corporel, poids de l'œsophage, IgE sérique, nombre d'éosinophiles dans le sang et l'œsophage, score histopathologique (HE), analyse des granulocytes.
Valeur translationnelle – Idéal pour tester les anti-IL-5, anti-IL-13, anti-IL-33, les inhibiteurs de JAK et les thérapies d’épargne stéroïdienne.
IND Ready Packet – La recherche peut être menée conformément aux principes BPL.
L'IL-33 induit le modèle C57BL/6 EoE
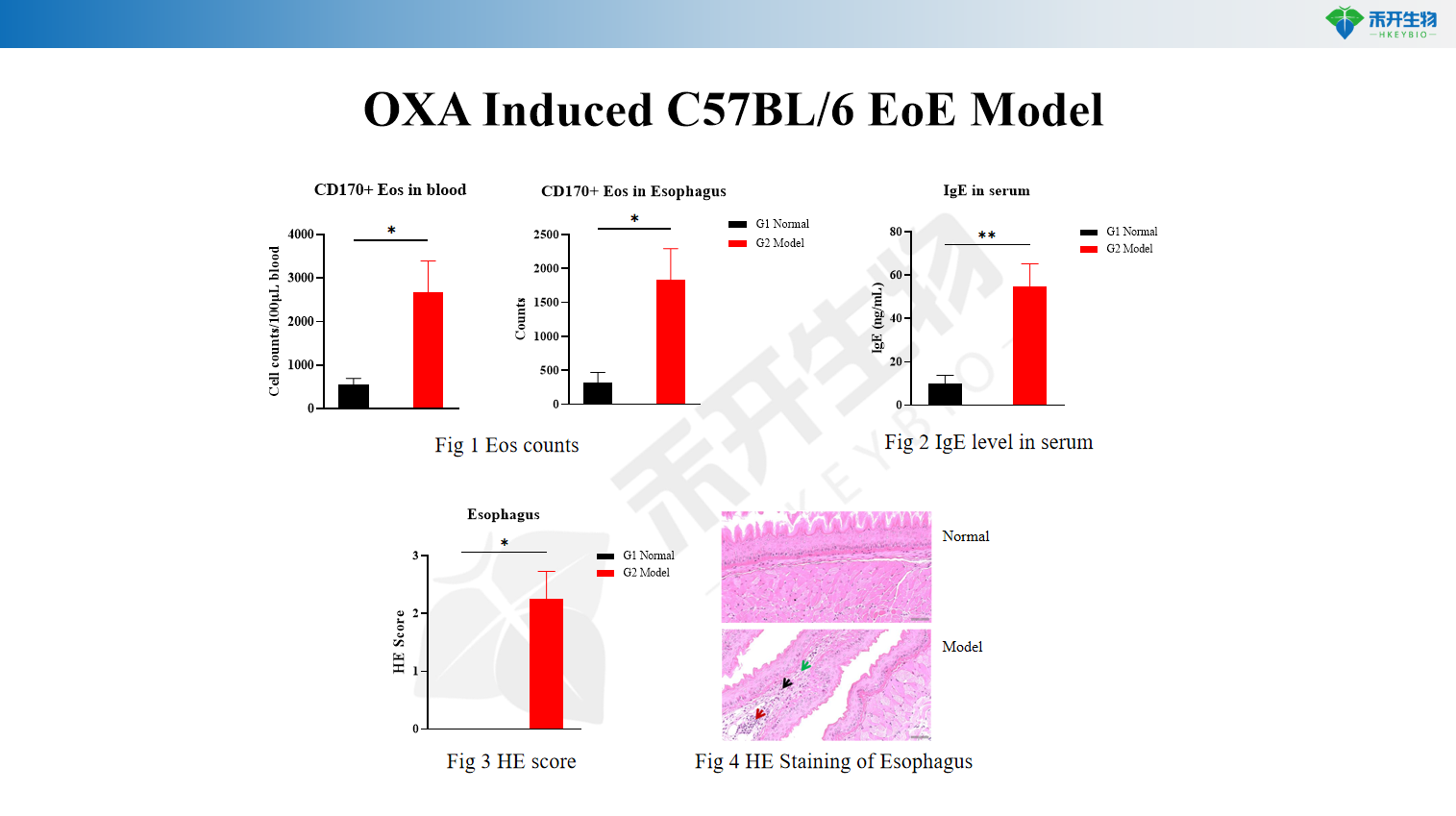
Modèle OXA Induction C57BL/6 EoE
• Tests d'efficacité des produits biologiques (anti-IL-5, anti-IL-13, anti-IL-33, anti-Siglec-8), des inhibiteurs de JAK et des corticostéroïdes
• Validation ciblée de la voie Th2 et du recrutement des éosinophiles
• Découverte de biomarqueurs (IgE, médiateurs dérivés des éosinophiles, cytokines)
• Études du mécanisme d'action (MOA) dans les maladies éosinophiles
• Études pharmacologiques pour soutenir l'IND
portée |
Modèle EoE induit par l'IL-33 |
Modèle EoE induit par OXA |
tension |
Souris C57BL/6 |
Souris C57BL/6 |
méthode d'induction |
IL-33 recombinante (intrapéritonéale ou intranasale), doses multiples sur 5 à 14 jours |
Sensibilisation cutanée induite par l'OXA suivie d'une provocation intraluminale par l'OXA |
temps d'étude |
7 à 21 jours |
10 à 18 jours (sensibilisation + défi) |
point final critique |
Poids corporel, poids de l'œsophage, IgE sériques, nombre d'éosinophiles dans le sang et l'œsophage (cytométrie en flux), score de coloration HE, analyse des granulocytes |
Nombre d'éosinophiles œsophagiens, IgE sériques, score de coloration HE, histopathologie œsophagienne, taux de cytokines Th2 (IL-4, IL-5, IL-13) |
paquet |
Données brutes, rapports d'analyses, fichiers de cytométrie en flux, lames histologiques (HE), bioinformatique (facultatif) | |
Q : Quelle est la différence entre les modèles EoE induits par l’IL-33 et l’OXA ?
R : Le modèle IL-33 active directement les lymphocytes innés du groupe 2 (ILC2) et pilote l'inflammation Th2 via une signalisation d'alarme, imitant l'EoE induite par les cytokines d'origine épithéliale. Le modèle OXA est un modèle d'hypersensibilité de type retardé induit par l'haptène qui active les cellules Th2 via la présentation de l'antigène et représente l'EoE déclenchée par un allergène.
Q : Quel modèle convient le mieux pour tester les thérapies anti-IL-33 ?
Réponse : Le modèle d'induction de l'IL-33 est le choix le plus direct pour évaluer les inhibiteurs de la voie IL-33/ST2. Le modèle OXA est plus adapté pour tester une gamme plus large de modulateurs immunitaires ciblant l’activation des lymphocytes T et les cytokines Th2.
Q : Ces modèles peuvent-ils être utilisés pour les études de support IND ?
Réponse : Oui. Les études peuvent être menées selon les principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différents schémas posologiques, combinaisons avec des allergènes alimentaires) ?
Réponse : Bien sûr. Notre équipe scientifique adapte les protocoles d’induction, les plans de traitement et les analyses des paramètres à votre candidat médicament spécifique.
