| Beskikbaarheid: | |
|---|---|
| Hoeveelheid: | |











Kliniese relevansie - Die kombinasie van sigaretrook en lipopolisakkariedblootstelling modelleer die etiologie en chroniese inflammasie van chroniese obstruktiewe longsiekte by mense.
Veelvuldige spesies - muis- en rotmodelle is beskikbaar om aan verskillende eksperimentele vereistes te voldoen (genetiese gereedskap vs. groter grootte).
Omvattende eindpunt - liggaamsgewig, BALF-sitologie (leukosiete, makrofage, monosiete), longfunksie (weerstand, voldoening), histopatologie (HE-telling) en sitokienanalise.
Translasiewaarde – ideaal vir die toets van anti-inflammatoriese middels (kortikosteroïede, PDE4-inhibeerders), brongodilators en mukolytika.
IND Ready Packet – Navorsing kan in ooreenstemming met GLP-beginsels uitgevoer word.
Rook + LPS veroorsaak C57BL/6 muis COPD model
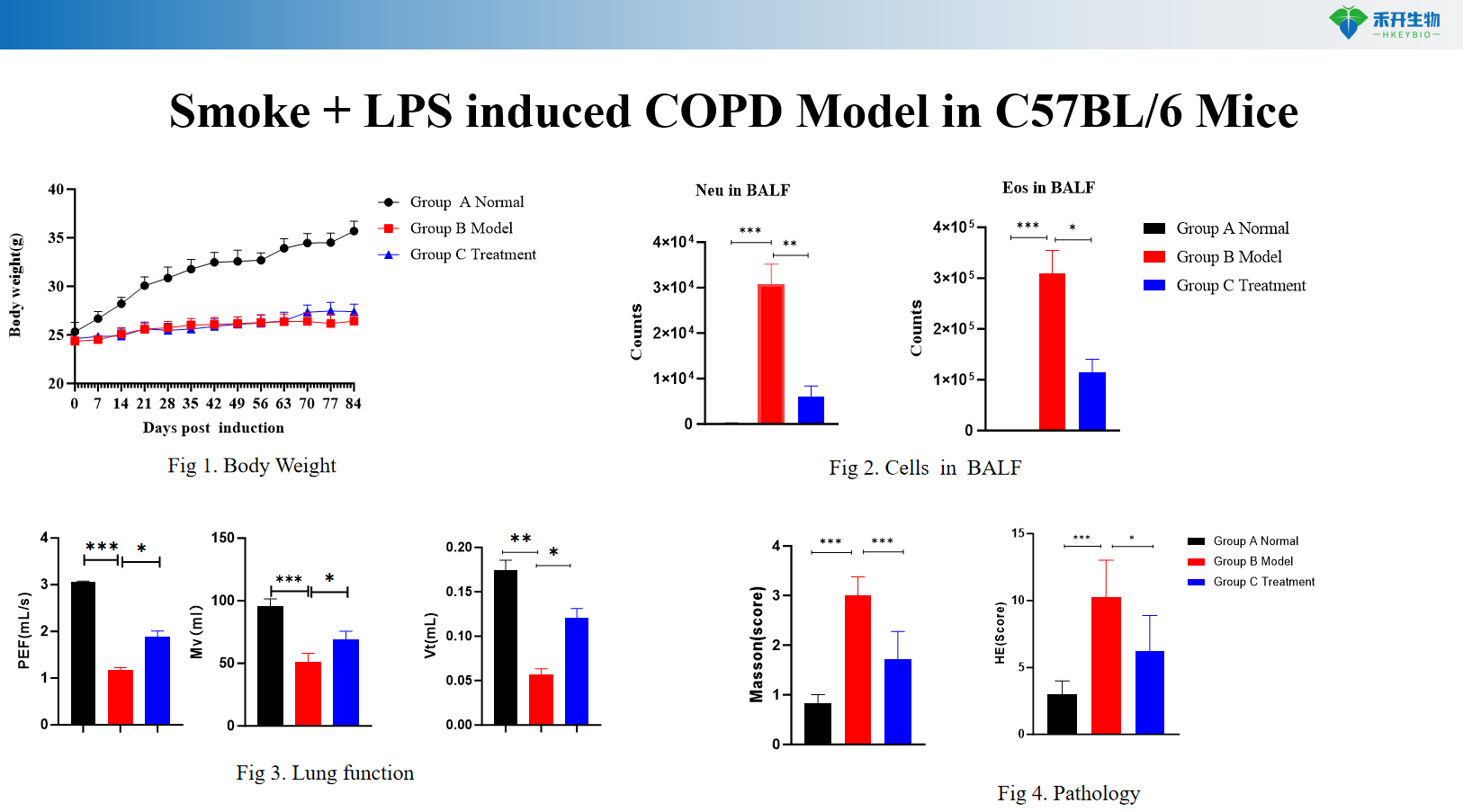
C57BL/6 muis rook-geïnduseerde COPD model
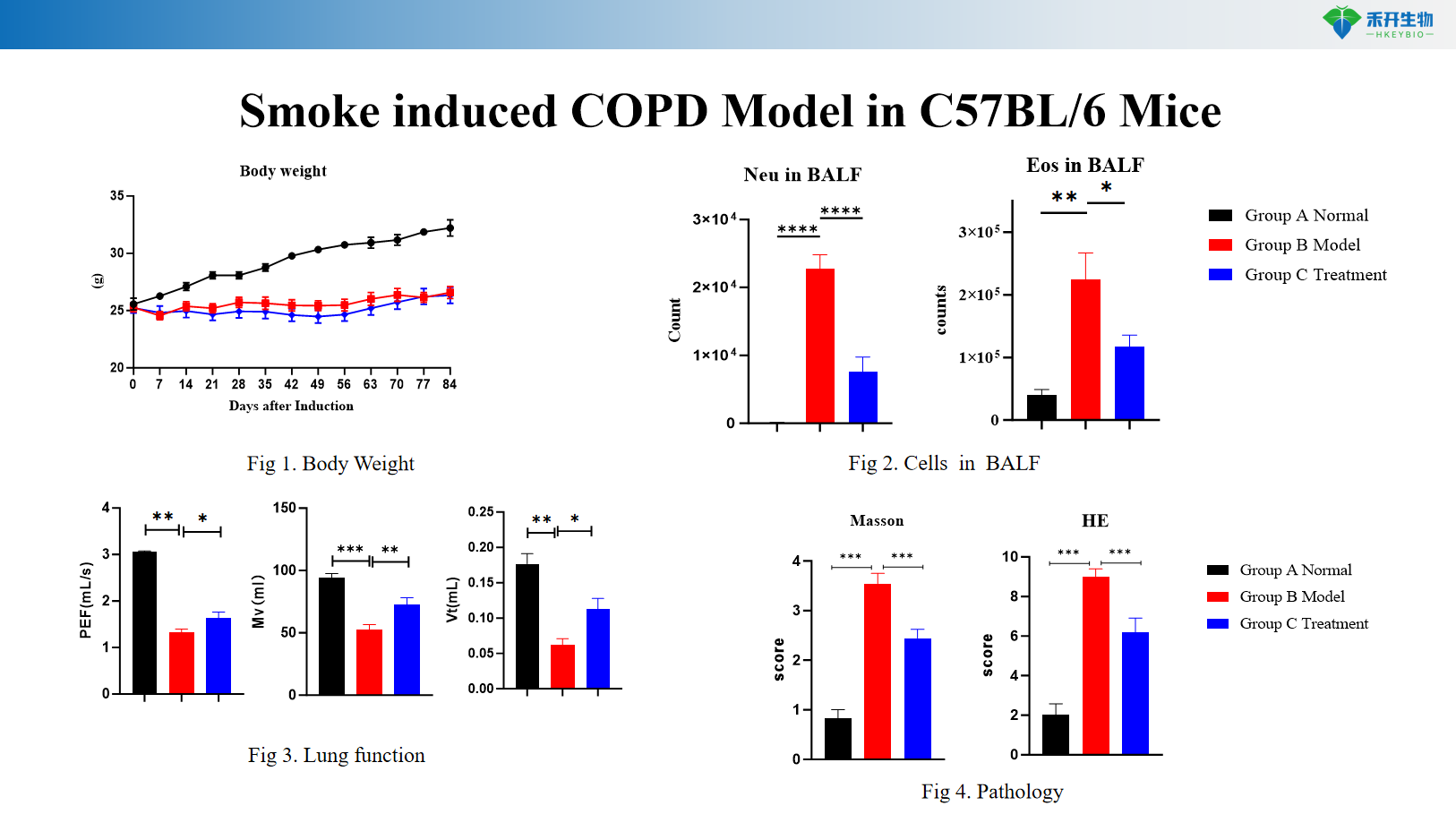
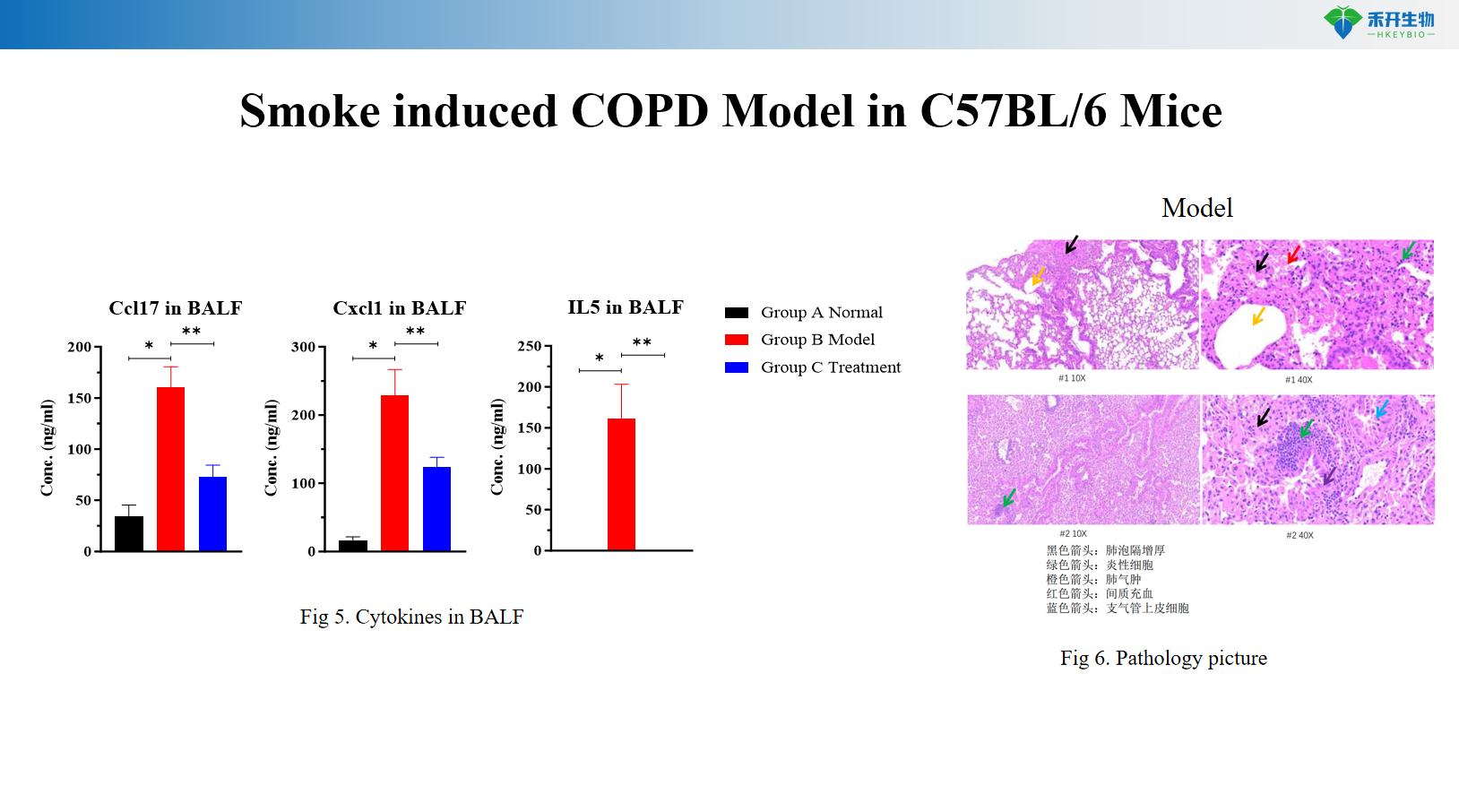
Rook-geïnduseerde COPD-model in transgeniese C57BL/6 muise
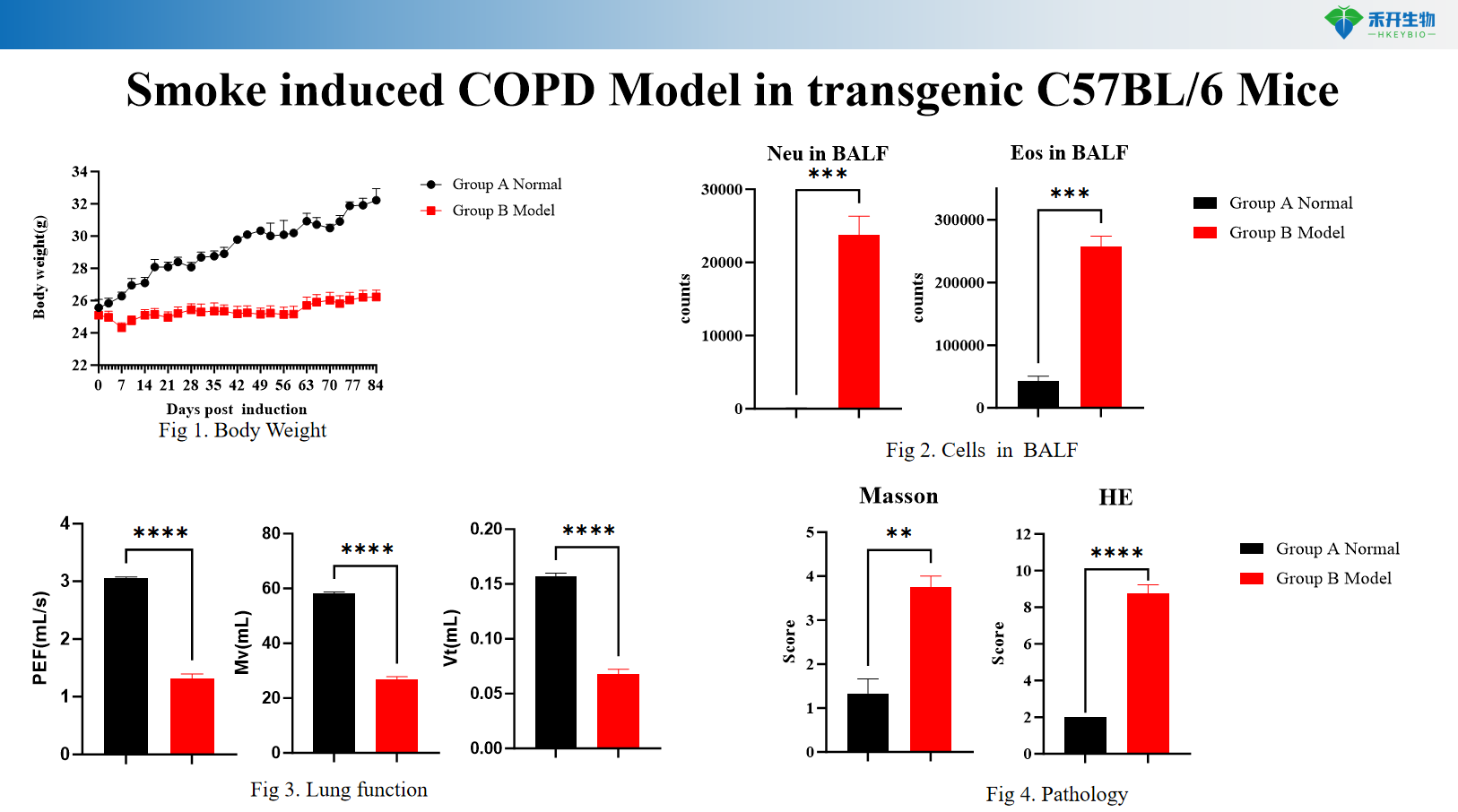
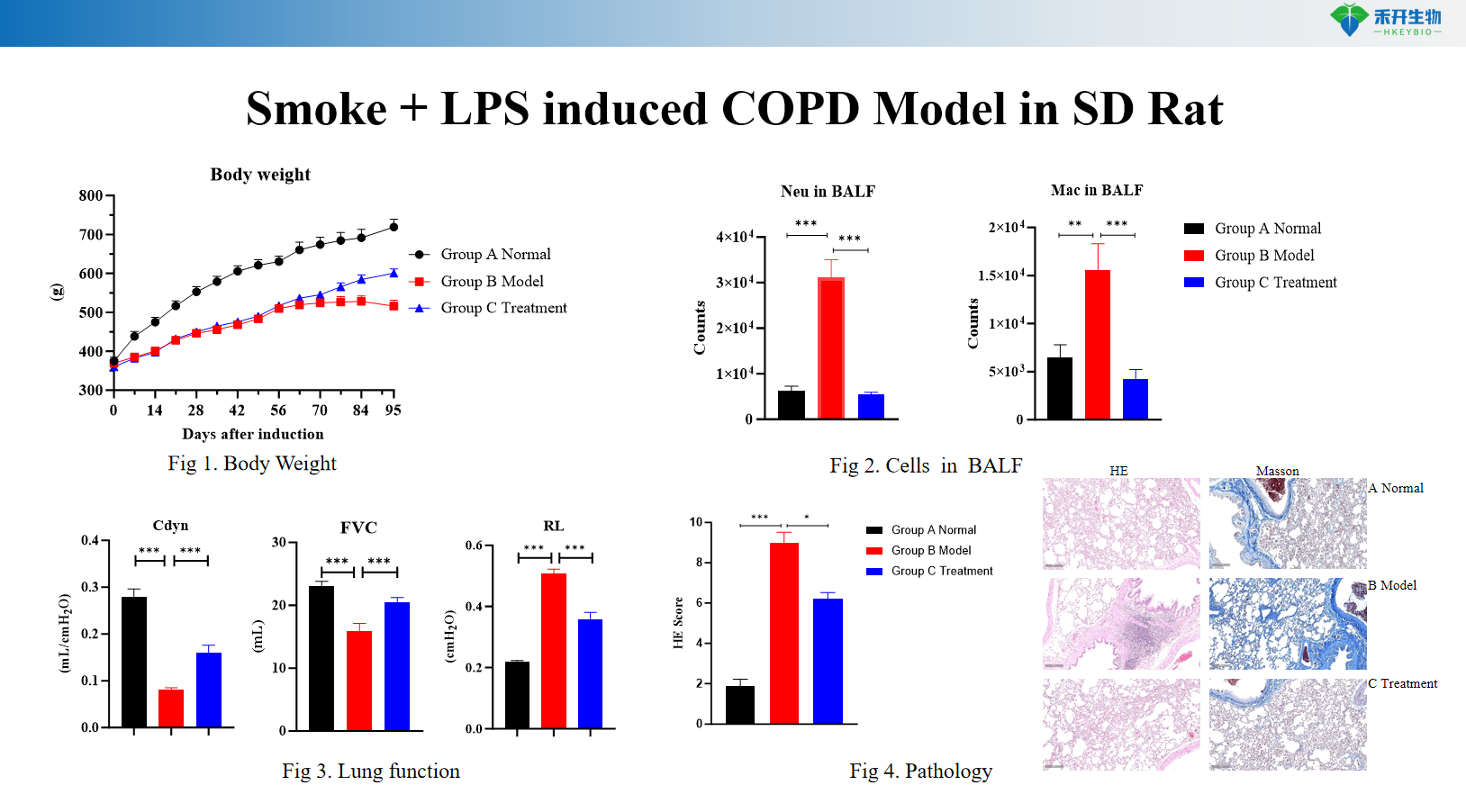
Rook + LPS-geïnduseerde COPD-model in SD-rotte
• Doeltreffendheidtoetsing van anti-inflammatoriese middels (kortikosteroïede, PDE4 inhibeerders, p38 MAPK inhibeerders)
• Evaluering van brongodilators (β2-agoniste, anticholinergiese middels) en kombinasieterapieë
• Toetsing van slymaktiewe middels en antioksidante
• Teiken validering van inflammasie en oksidatiewe stres weë
• Farmakologie en toksikologiestudies om IND te ondersteun
omvang |
Muis chroniese obstruktiewe longsiekte model |
Rotmodel van chroniese obstruktiewe longsiekte |
Spesie/Stam |
C57BL/6 muis |
Sprague-Dawley Rot |
induksie metode |
Chroniese blootstelling aan sigaretrook (slegs die hele liggaam of neus) 5 dae/week vir 4-6 maande + intratrageale LPS (1-2 keer/week) |
|
studietyd |
4–7 maande (induksie + behandeling) |
4–7 maande (induksie + behandeling) |
kritiese eindpunt |
Liggaamsgewig, BALF-seltelling (totaal en differensieel: makrofage, monosiete, neutrofiele), longfunksie (weerstand, nakoming, Penh), histopatologie (HE-telling vir emfiseem en inflammasie), sitokienvlakke in BALF (IL-6, TNF-α, MCP-1), opsioneel: oksidatiewe stres-meta-merkers (PAM)-sep (lineplasia-sel) | |
pakkie |
Rou data, analise verslag, BALF sitologie, longfunksie data, histologiese afdelings, ELISA resultate, bioinformatika (opsioneel) | |
V: Waarom word sigaretrook en LPS in COPD-modelle gekombineer?
A: Sigaretrook veroorsaak chroniese inflammasie en emfiseem, terwyl LPS (nabootsing van bakteriële infeksie) lugwegontsteking en slymproduksie vererger. Die kombinasie herhaal die patologie van menslike COPD nader, insluitend akute verergering.
V: Wat is die belangrikste ooreenkomste met menslike COPD?
A: Hierdie modelle toon progressiewe lugvloeiobstruksie, lugwegontsteking (makrofage, neutrofiele), emfiseem, bekerselmetaplasie en sistemiese effekte wat baie soos menslike COPD lyk.
V: Kan hierdie modelle vir IND-ondersteuningstudies gebruik word?
Antwoord: Ja. Studies kan volgens GLP-beginsels vir regulatoriese voorleggings (FDA, EMA) uitgevoer word.
V: Bied jy pasgemaakte studieprotokolle (bv. verskillende rookblootstellingstye, LPS-dosisse)?
Antwoord: Natuurlik. Ons wetenskaplike span pas protokolle vir rookblootstelling, LPS-dosering en eindpuntanalise aan vir u spesifieke geneesmiddelkandidaat.
