| Beschikbaarheid: | |
|---|---|
| Aantal: | |











Klinische relevantie - De combinatie van sigarettenrook en blootstelling aan lipopolysachariden modelleert de etiologie en chronische ontsteking van chronische obstructieve longziekte bij mensen.
Er zijn meerdere soorten - muis- en rattenmodellen beschikbaar om aan verschillende experimentele vereisten te voldoen (genetische hulpmiddelen versus groter formaat).
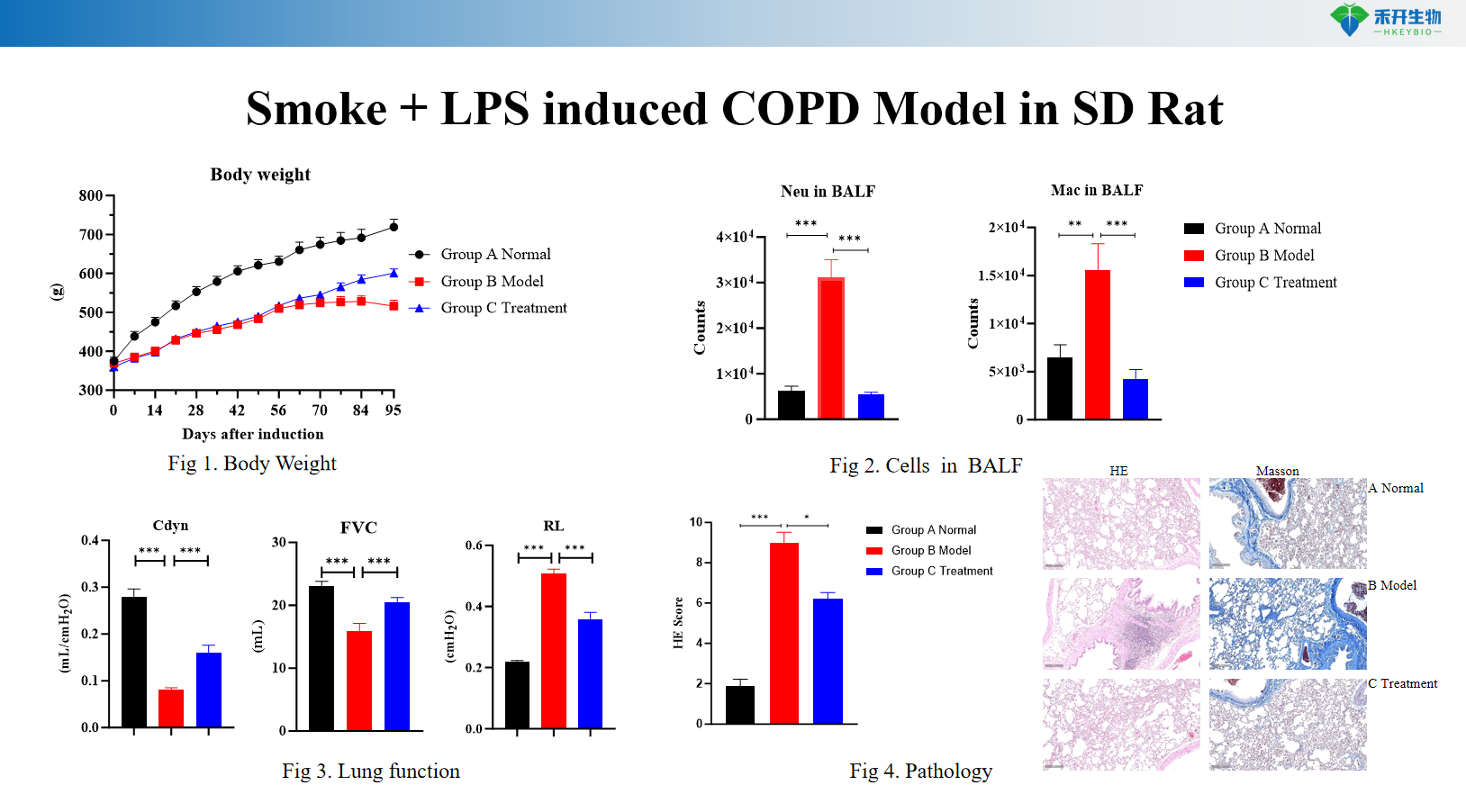
Uitgebreid eindpunt - lichaamsgewicht, BALF-cytologie (leukocyten, macrofagen, monocyten), longfunctie (resistentie, compliantie), histopathologie (HE-score) en cytokine-analyse.
Translationele waarde – ideaal voor het testen van ontstekingsremmende medicijnen (corticosteroïden, PDE4-remmers), luchtwegverwijders en mucolytica.
IND Ready Packet – Onderzoek kan worden uitgevoerd volgens de GLP-principes.
Rook + LPS induceert COPD-model van C57BL/6-muizen
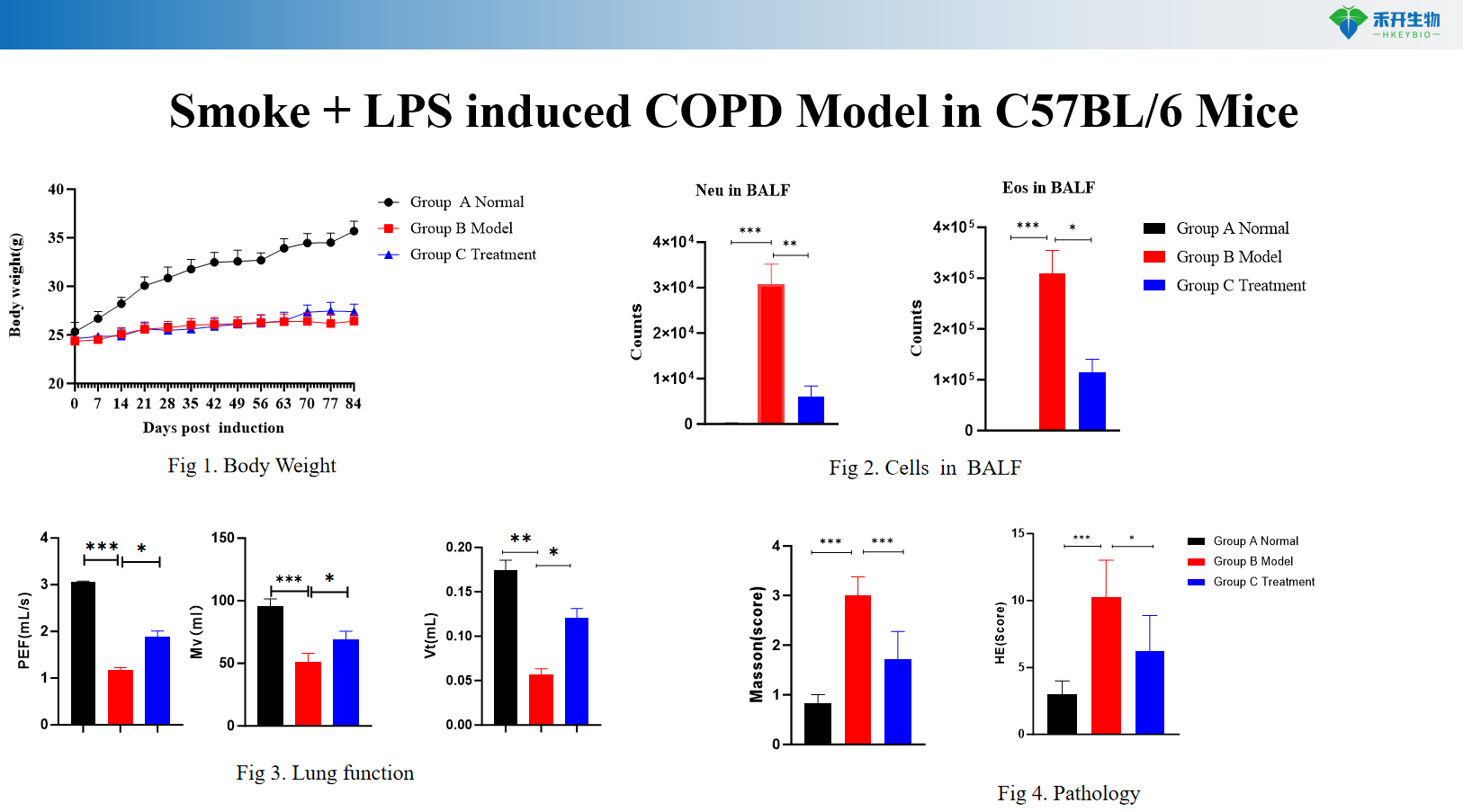
C57BL/6 door rook geïnduceerd COPD-model van muizen
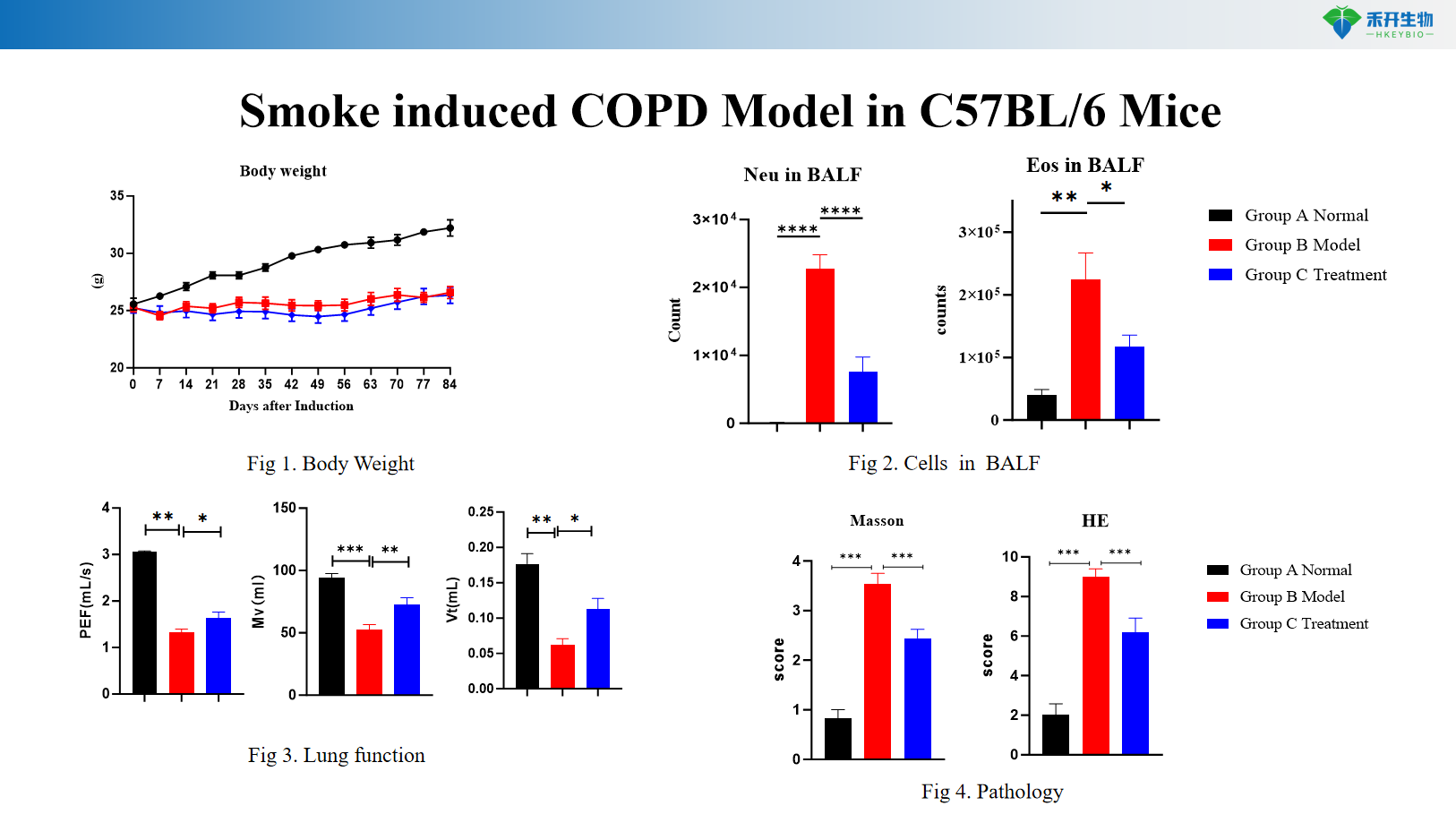
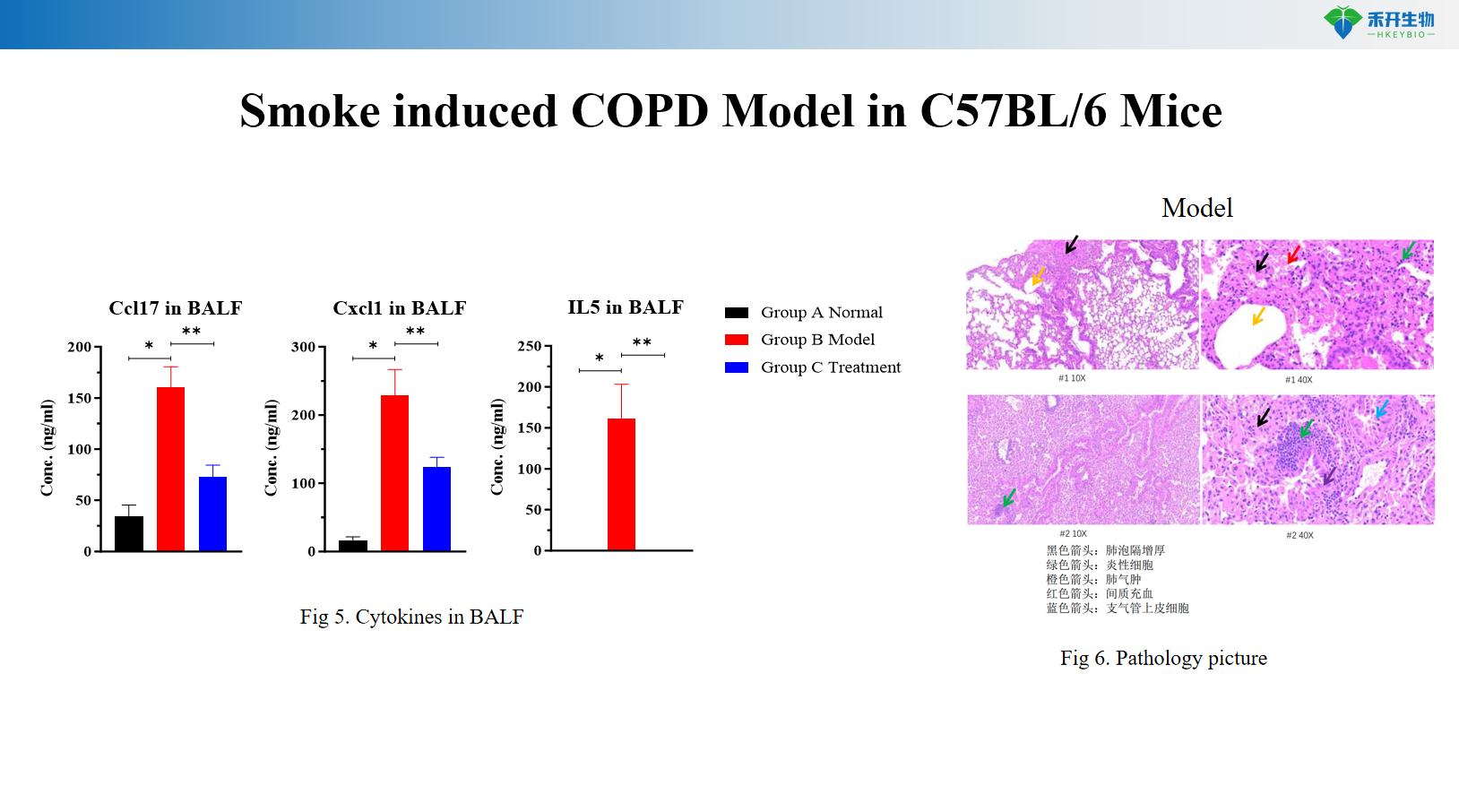
Door rook geïnduceerd COPD-model in transgene C57BL/6-muizen
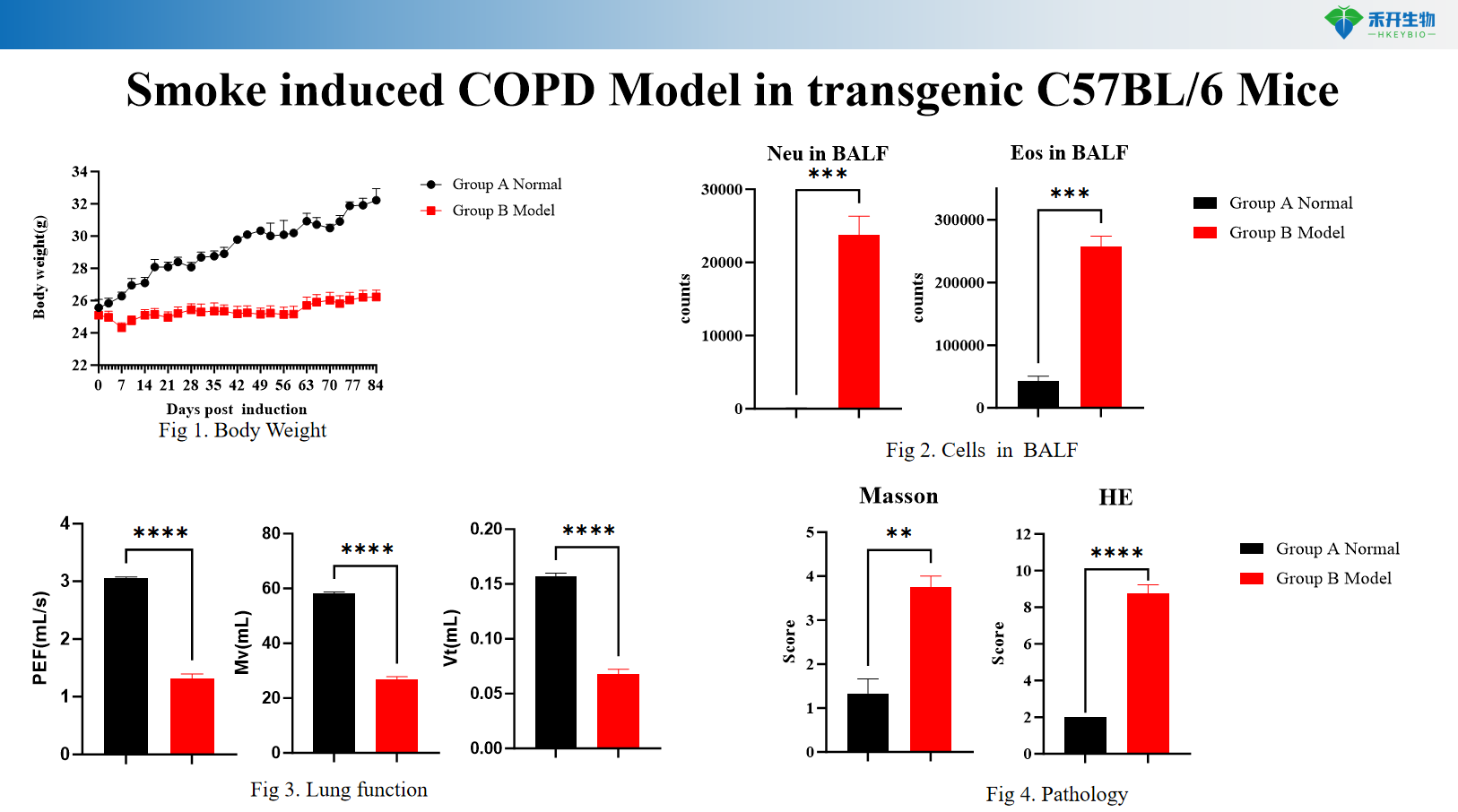
Rook + LPS-geïnduceerd COPD-model bij SD-ratten
• Werkzaamheidstesten van ontstekingsremmende geneesmiddelen (corticosteroïden, PDE4-remmers, p38 MAPK-remmers)
• Evaluatie van luchtwegverwijders (β2-agonisten, anticholinergica) en combinatietherapieën
• Testen van slijmactieve stoffen en antioxidanten
• Doelvalidatie van ontstekings- en oxidatieve stressroutes
• Farmacologische en toxicologische onderzoeken ter ondersteuning van de IND
domein |
Chronische obstructieve longziektemodel bij muizen |
Rattenmodel van chronische obstructieve longziekte |
Soort/stam |
C57BL/6 muis |
Sprague-Dawley Rat |
inductie methode |
Chronische blootstelling aan sigarettenrook (alleen het hele lichaam of de neus) 5 dagen/week gedurende 4-6 maanden + intratracheale LPS (1-2 keer/week) |
|
studie tijd |
4–7 maanden (inductie + behandeling) |
4–7 maanden (inductie + behandeling) |
kritisch eindpunt |
Lichaamsgewicht, BALF-celaantal (totaal en differentieel: macrofagen, monocyten, neutrofielen), longfunctie (resistentie, compliantie, Penh), histopathologie (HE-score voor emfyseem en ontsteking), cytokineniveaus in BALF (IL-6, TNF-α, MCP-1), optioneel: oxidatieve stressmarkers, bekercelmetaplasie (PAS), gemiddelde lineaire intercept (MLI) | |
pakket |
Ruwe gegevens, analyserapport, BALF-cytologie, longfunctiegegevens, histologische coupes, ELISA-resultaten, bio-informatica (optioneel) | |
Vraag: Waarom worden sigarettenrook en LPS gecombineerd in COPD-modellen?
A: Sigarettenrook veroorzaakt chronische ontstekingen en emfyseem, terwijl LPS (simulatie van bacteriële infecties) de luchtwegontsteking en de slijmproductie verergert. De combinatie repliceert beter de pathologie van menselijk COPD, inclusief acute exacerbaties.
Vraag: Wat zijn de belangrijkste overeenkomsten met COPD bij mensen?
A: Deze modellen vertonen progressieve luchtwegobstructie, luchtwegontsteking (macrofagen, neutrofielen), emfyseem, slijmbekercelmetaplasie en systemische effecten die sterk lijken op menselijke COPD.
Vraag: Kunnen deze modellen worden gebruikt voor IND-ondersteuningsonderzoeken?
Antwoord: Ja. Studies kunnen worden uitgevoerd volgens de GLP-principes voor indieningen bij de regelgevende instanties (FDA, EMA).
Vraag: Bieden jullie op maat gemaakte onderzoeksprotocollen aan (bijvoorbeeld verschillende blootstellingstijden aan rook, LPS-doses)?
Antwoord: Natuurlijk. Ons wetenschappelijk team stemt de rookblootstellingsprotocollen, LPS-dosering en eindpuntanalyse af op uw specifieke kandidaat-geneesmiddel.
