| Verfügbarkeit: | |
|---|---|
| Menge: | |











Klinische Relevanz – Die Kombination aus Zigarettenrauch und Lipopolysaccharidexposition modelliert die Ätiologie und chronische Entzündung chronisch obstruktiver Lungenerkrankungen beim Menschen.
Mehrere Arten – Maus- und Rattenmodelle stehen zur Verfügung, um unterschiedliche experimentelle Anforderungen zu erfüllen (genetische Werkzeuge vs. größere Größe).
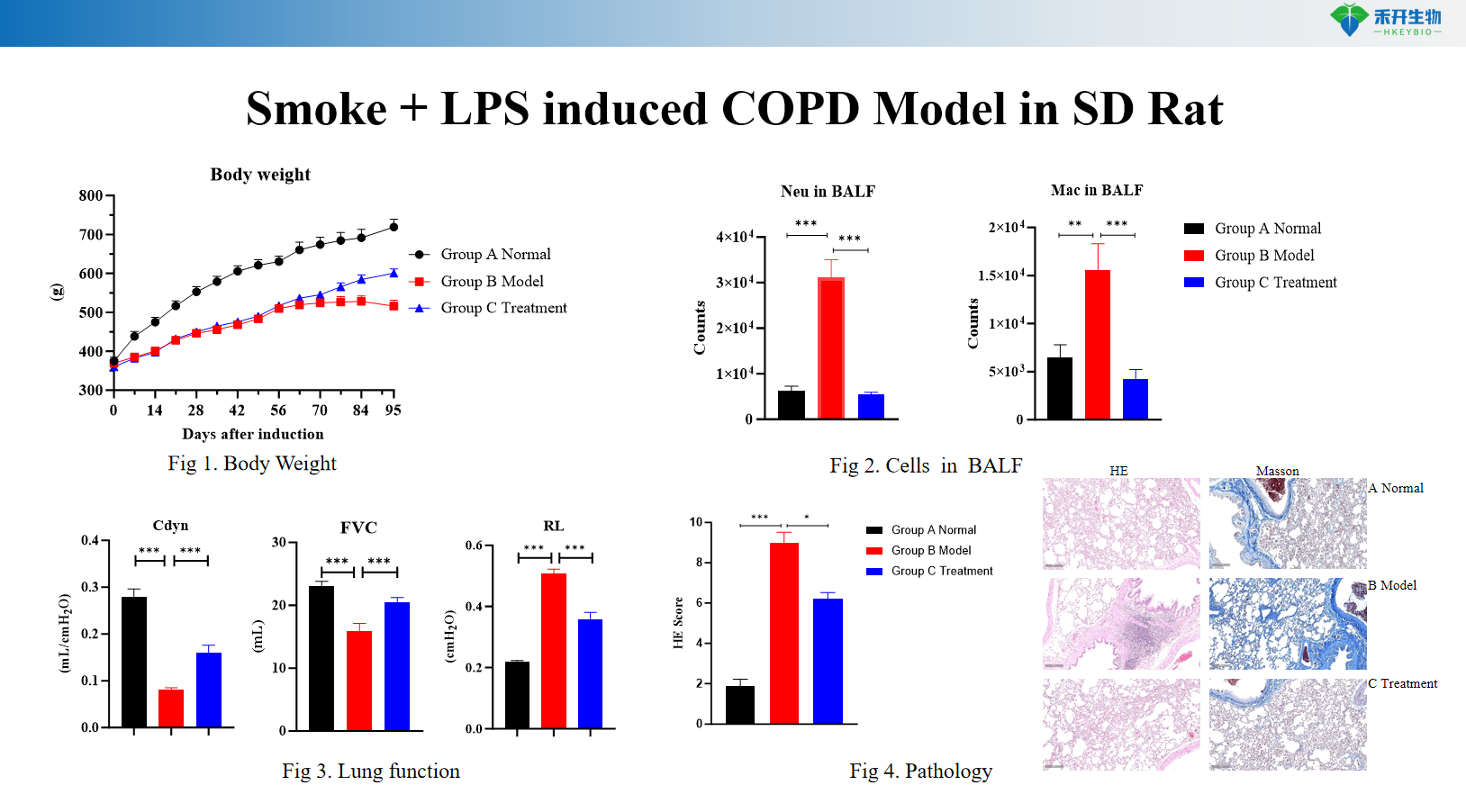
Umfassender Endpunkt – Körpergewicht, BALF-Zytologie (Leukozyten, Makrophagen, Monozyten), Lungenfunktion (Resistenz, Compliance), Histopathologie (HE-Score) und Zytokinanalyse.
Translationaler Wert – ideal zum Testen entzündungshemmender Medikamente (Kortikosteroide, PDE4-Hemmer), Bronchodilatatoren und Mukolytika.
IND Ready Packet – Forschung kann gemäß den GLP-Grundsätzen durchgeführt werden.
Rauch + LPS induziert das COPD-Modell C57BL/6 der Maus
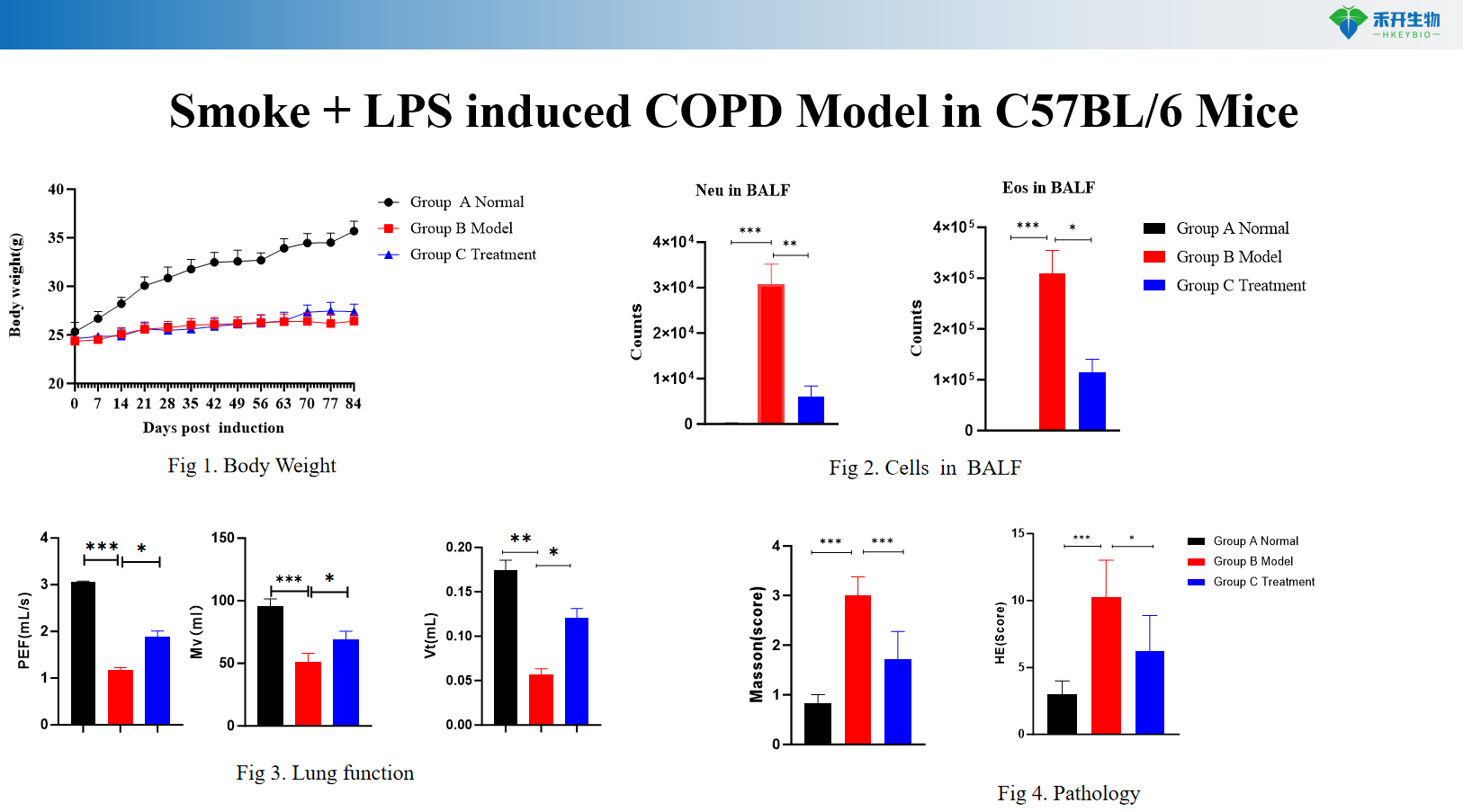
C57BL/6-Mausrauch-induziertes COPD-Modell
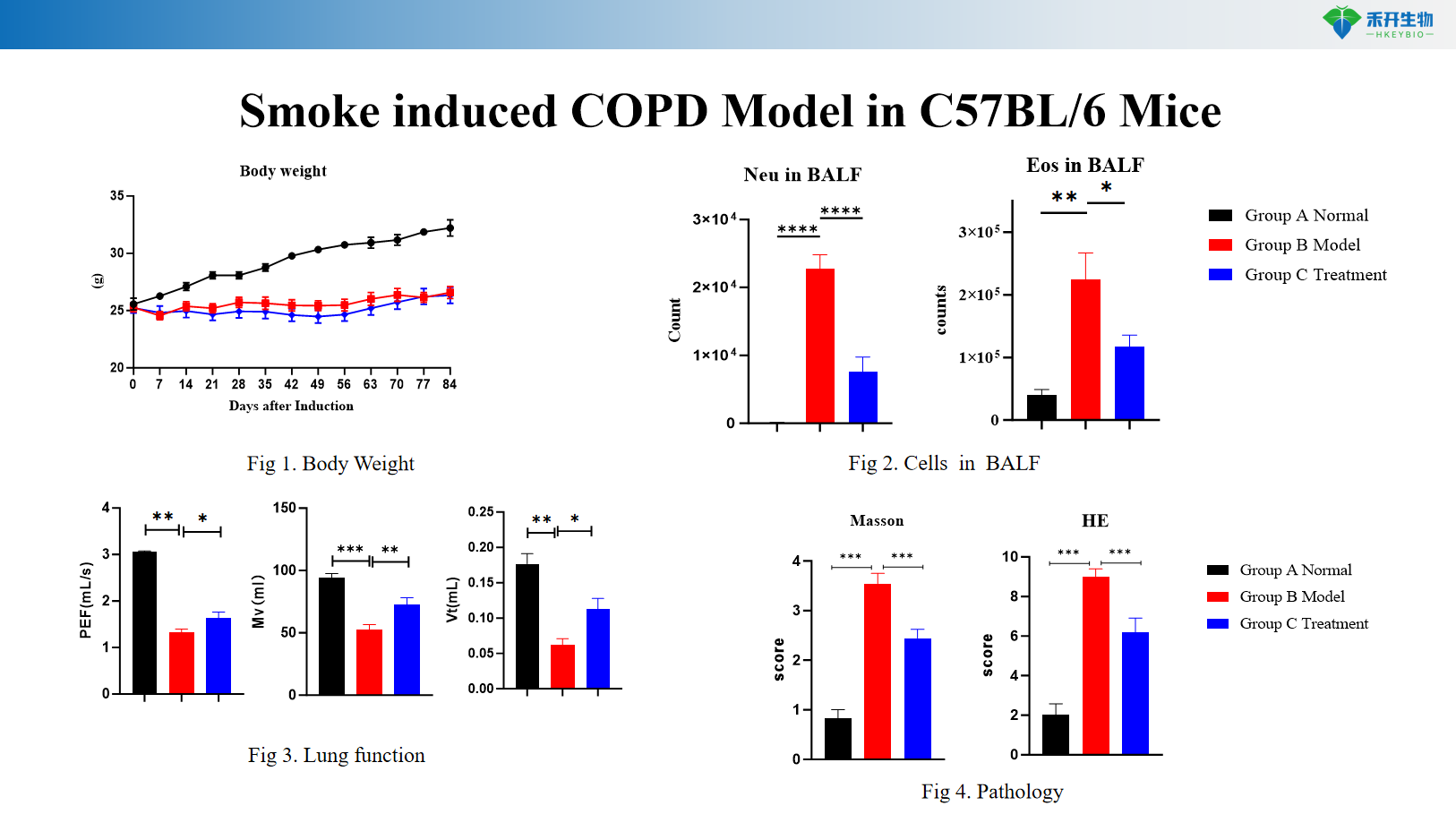
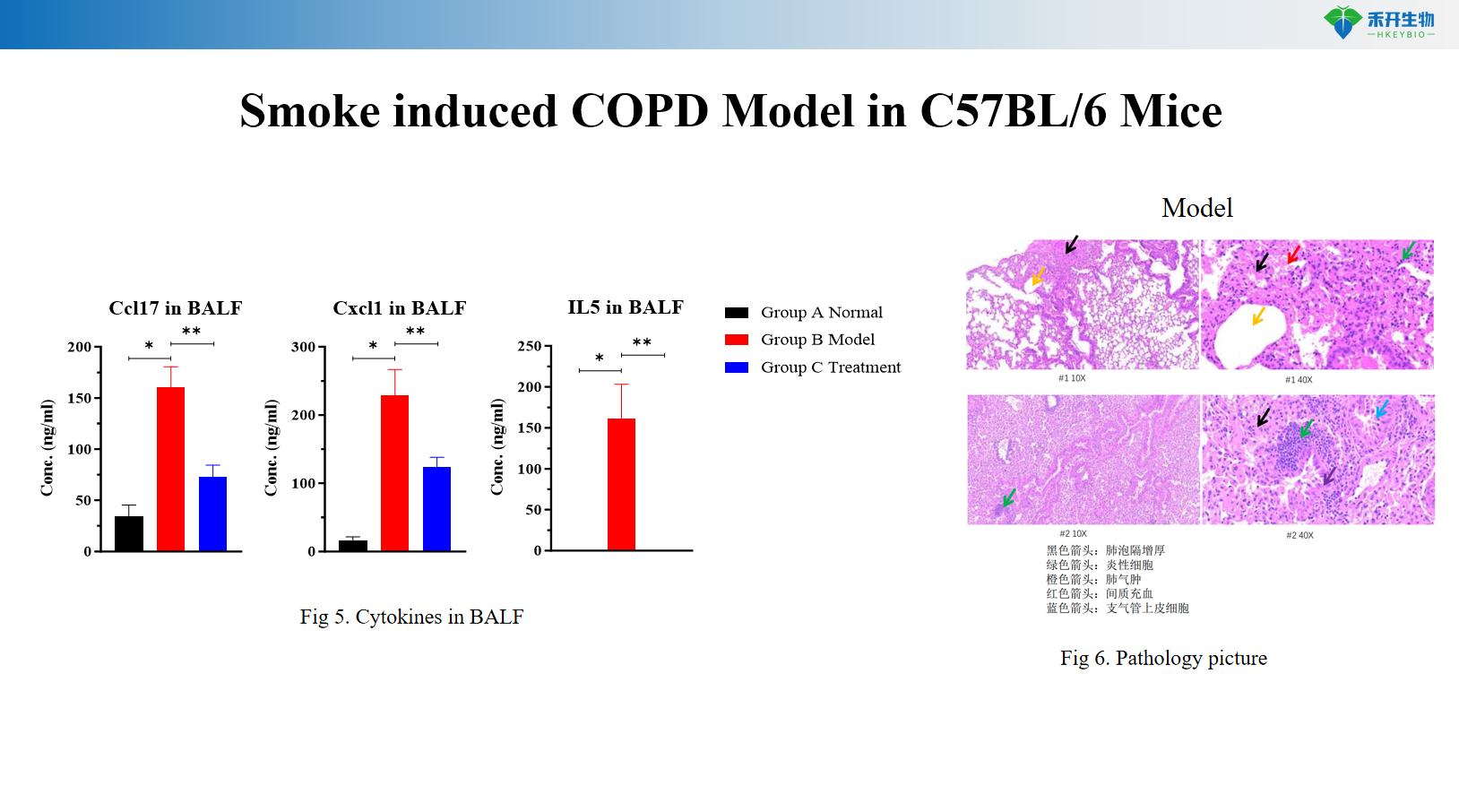
Rauchinduziertes COPD-Modell in transgenen C57BL/6-Mäusen
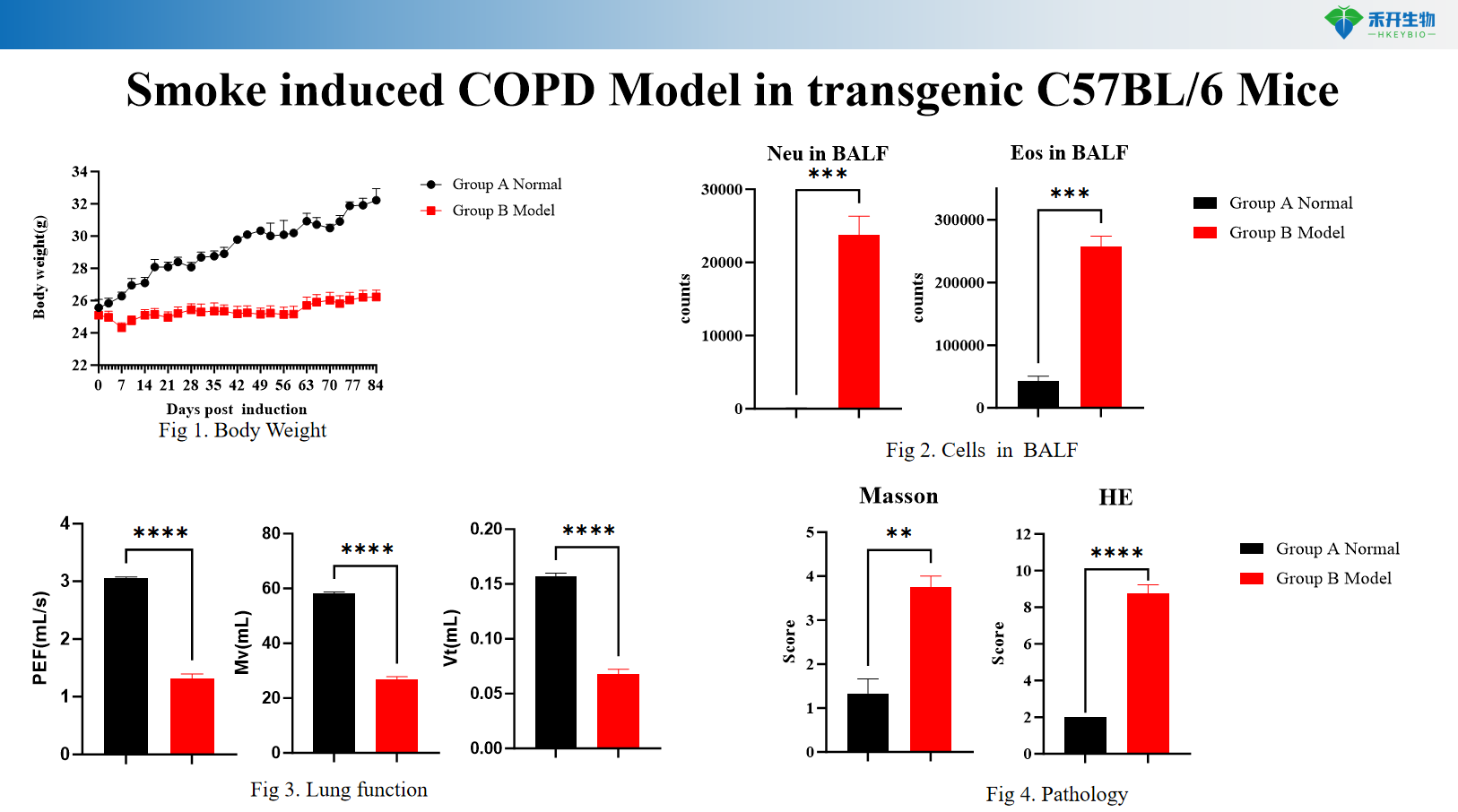
Rauch + LPS-induziertes COPD-Modell bei SD-Ratten
• Wirksamkeitsprüfung entzündungshemmender Medikamente (Kortikosteroide, PDE4-Inhibitoren, p38-MAPK-Inhibitoren)
• Bewertung von Bronchodilatatoren (β2-Agonisten, Anticholinergika) und Kombinationstherapien
• Prüfung von schleimaktiven Wirkstoffen und Antioxidantien
• Zielvalidierung von Entzündungs- und oxidativen Stresswegen
• Pharmakologische und toxikologische Studien zur Unterstützung von IND
Umfang |
Modell einer chronisch obstruktiven Lungenerkrankung bei Mäusen |
Rattenmodell einer chronisch obstruktiven Lungenerkrankung |
Art/Stamm |
C57BL/6-Maus |
Sprague-Dawley-Ratte |
Induktionsmethode |
Chronische Zigarettenrauchexposition (ganzer Körper oder nur Nase) 5 Tage/Woche für 4–6 Monate + intratracheales LPS (1–2 Mal/Woche) |
|
Lernzeit |
4–7 Monate (Einleitung + Behandlung) |
4–7 Monate (Einleitung + Behandlung) |
kritischer Endpunkt |
Körpergewicht, BALF-Zellzahl (gesamt und differenziell: Makrophagen, Monozyten, Neutrophile), Lungenfunktion (Resistenz, Compliance, Penh), Histopathologie (HE-Score für Emphysem und Entzündung), Zytokinspiegel in BALF (IL-6, TNF-α, MCP-1), optional: Marker für oxidativen Stress, Becherzellmetaplasie (PAS), mittlerer linearer Achsenabschnitt (MLI) | |
Paket |
Rohdaten, Analysebericht, BALF-Zytologie, Lungenfunktionsdaten, histologische Schnitte, ELISA-Ergebnisse, Bioinformatik (optional) | |
F: Warum werden Zigarettenrauch und LPS in COPD-Modellen kombiniert?
A: Zigarettenrauch löst chronische Entzündungen und Emphyseme aus, während LPS (das eine bakterielle Infektion simuliert) die Entzündung der Atemwege und die Schleimproduktion verschlimmert. Die Kombination bildet die Pathologie der menschlichen COPD, einschließlich akuter Exazerbationen, besser nach.
F: Was sind die wichtigsten Ähnlichkeiten zur menschlichen COPD?
A: Diese Modelle weisen eine fortschreitende Obstruktion des Luftstroms, Entzündungen der Atemwege (Makrophagen, Neutrophile), Emphyseme, Becherzellmetaplasie und systemische Effekte auf, die der menschlichen COPD sehr ähneln.
F: Können diese Modelle für IND-Unterstützungsstudien verwendet werden?
Antwort: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche Rauchexpositionszeiten, LPS-Dosen)?
Antwort: Natürlich. Unser wissenschaftliches Team passt Rauchexpositionsprotokolle, LPS-Dosierung und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
