| Disponibilità: | |
|---|---|
| Quantità: | |











Rilevanza clinica – La combinazione del fumo di sigaretta e dell’esposizione ai lipopolisaccaridi modella l’eziologia e l’infiammazione cronica della malattia polmonare ostruttiva cronica negli esseri umani.
Specie multiple : sono disponibili modelli di topo e ratto per soddisfare diversi requisiti sperimentali (strumenti genetici rispetto a dimensioni maggiori).
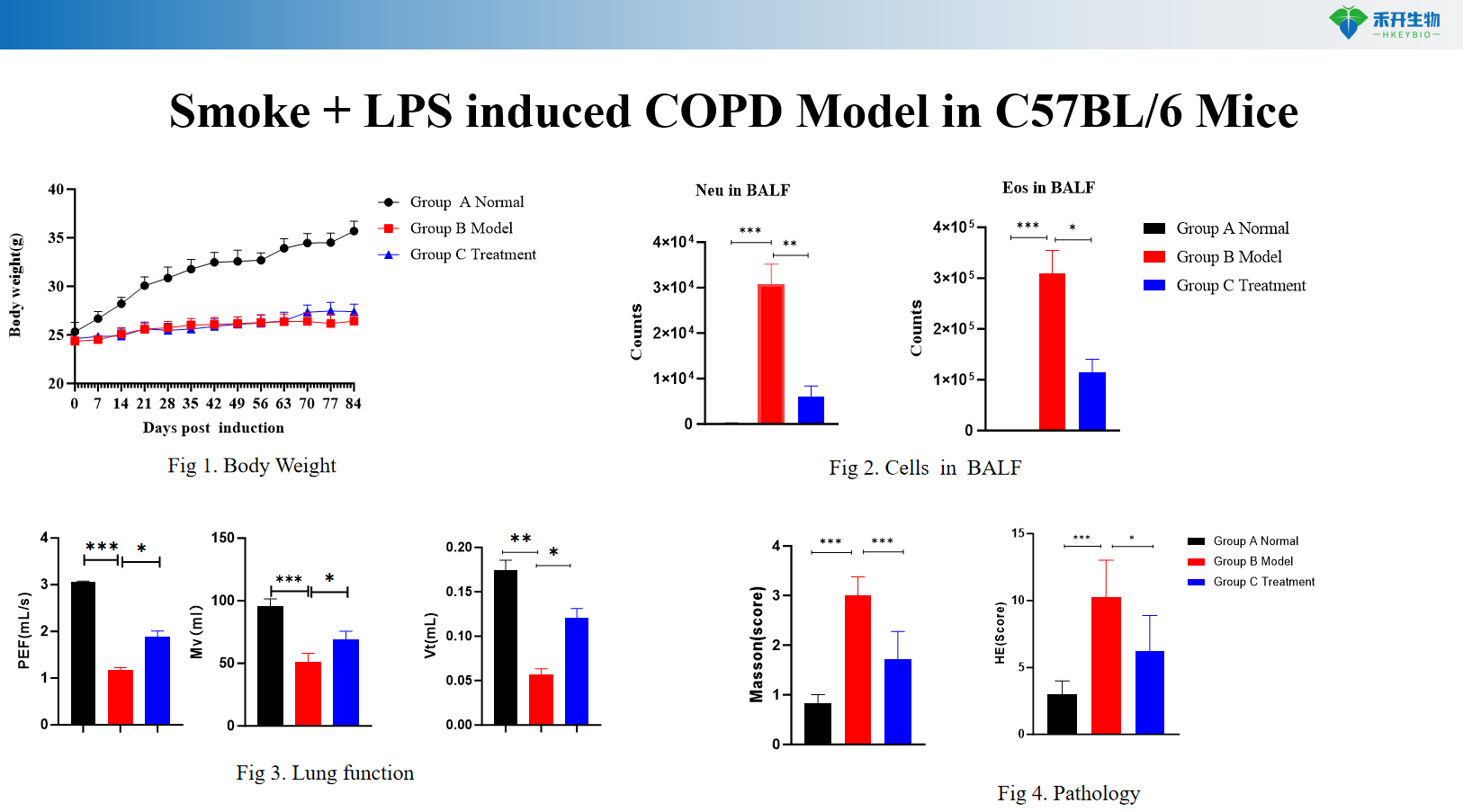
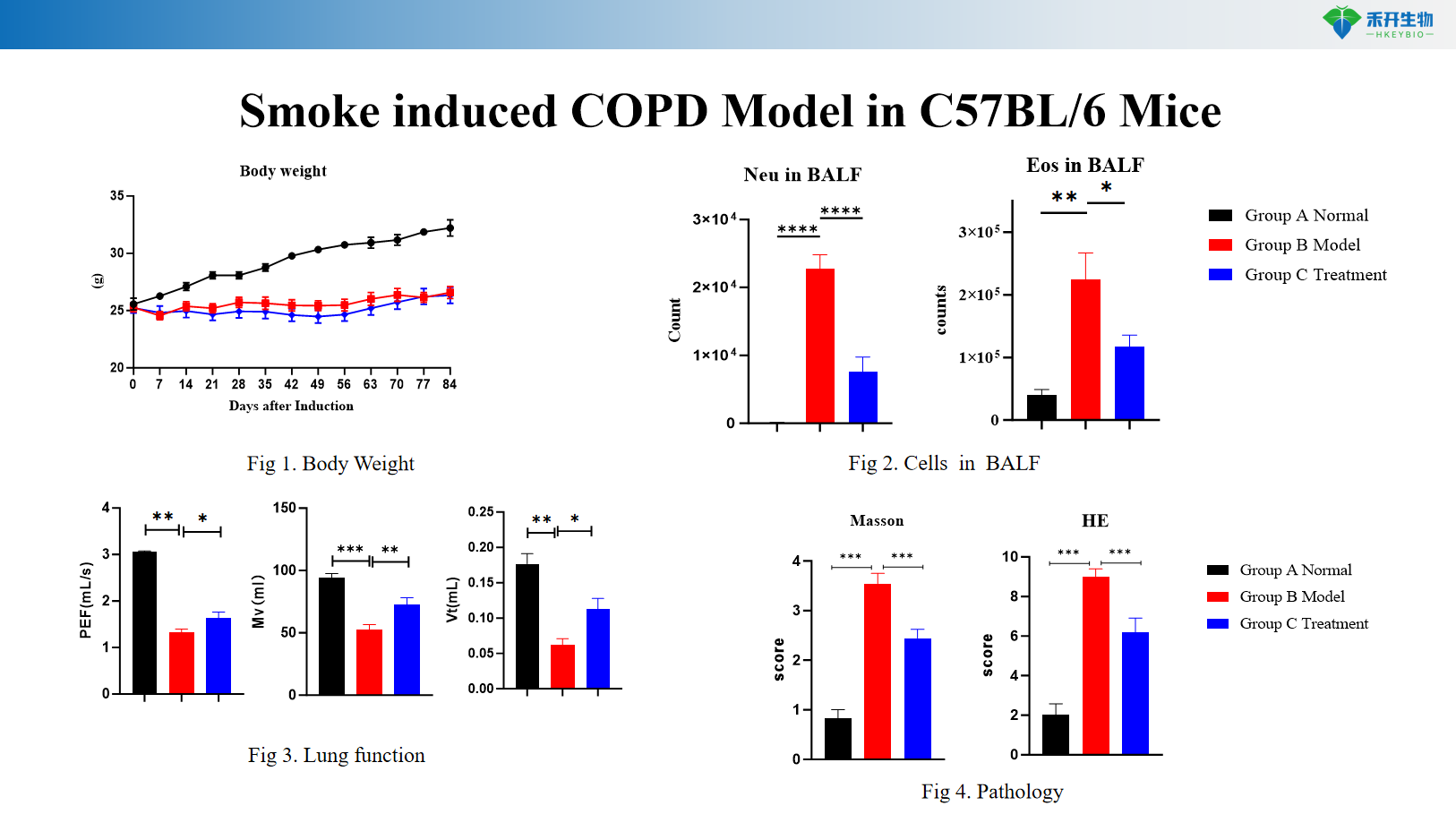
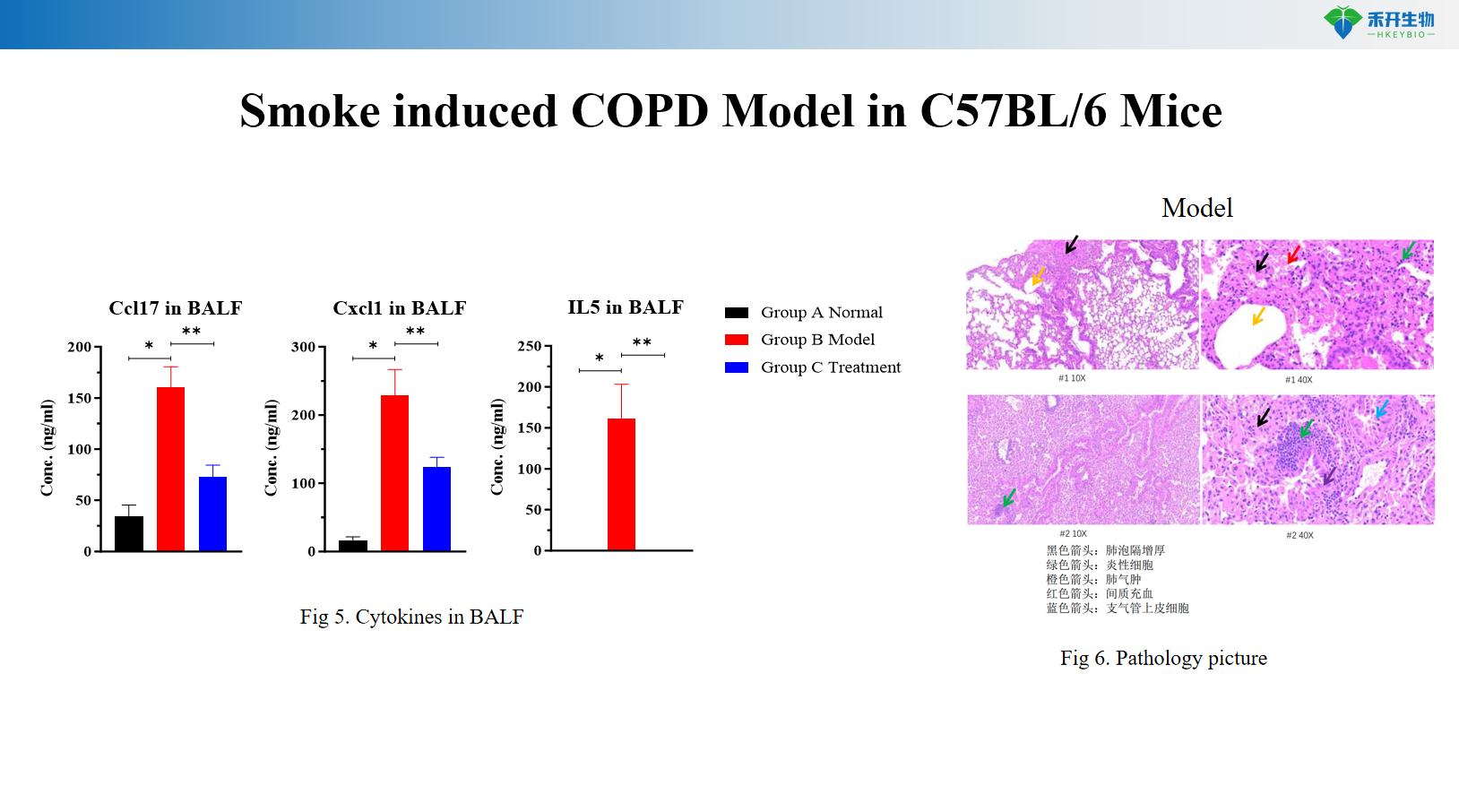
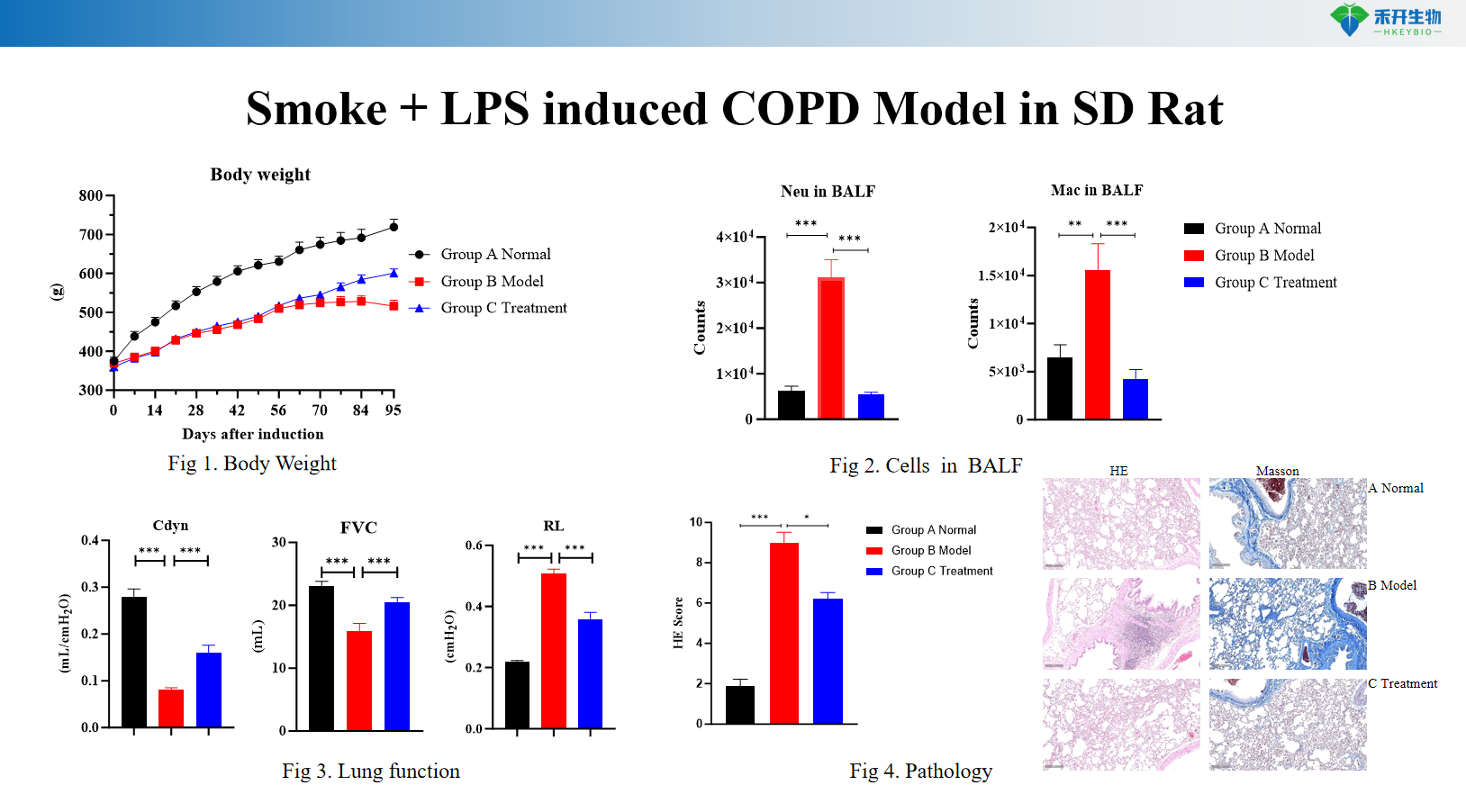
Endpoint completo : peso corporeo, citologia BALF (leucociti, macrofagi, monociti), funzione polmonare (resistenza, compliance), istopatologia (punteggio HE) e analisi delle citochine.
Valore traslazionale : ideale per testare farmaci antinfiammatori (corticosteroidi, inibitori della PDE4), broncodilatatori e mucolitici.
IND Ready Packet – La ricerca può essere condotta in conformità con i principi GLP.
Smoke + LPS induce il modello di BPCO murino C57BL/6
Modello di BPCO indotta dal fumo nel topo C57BL/6
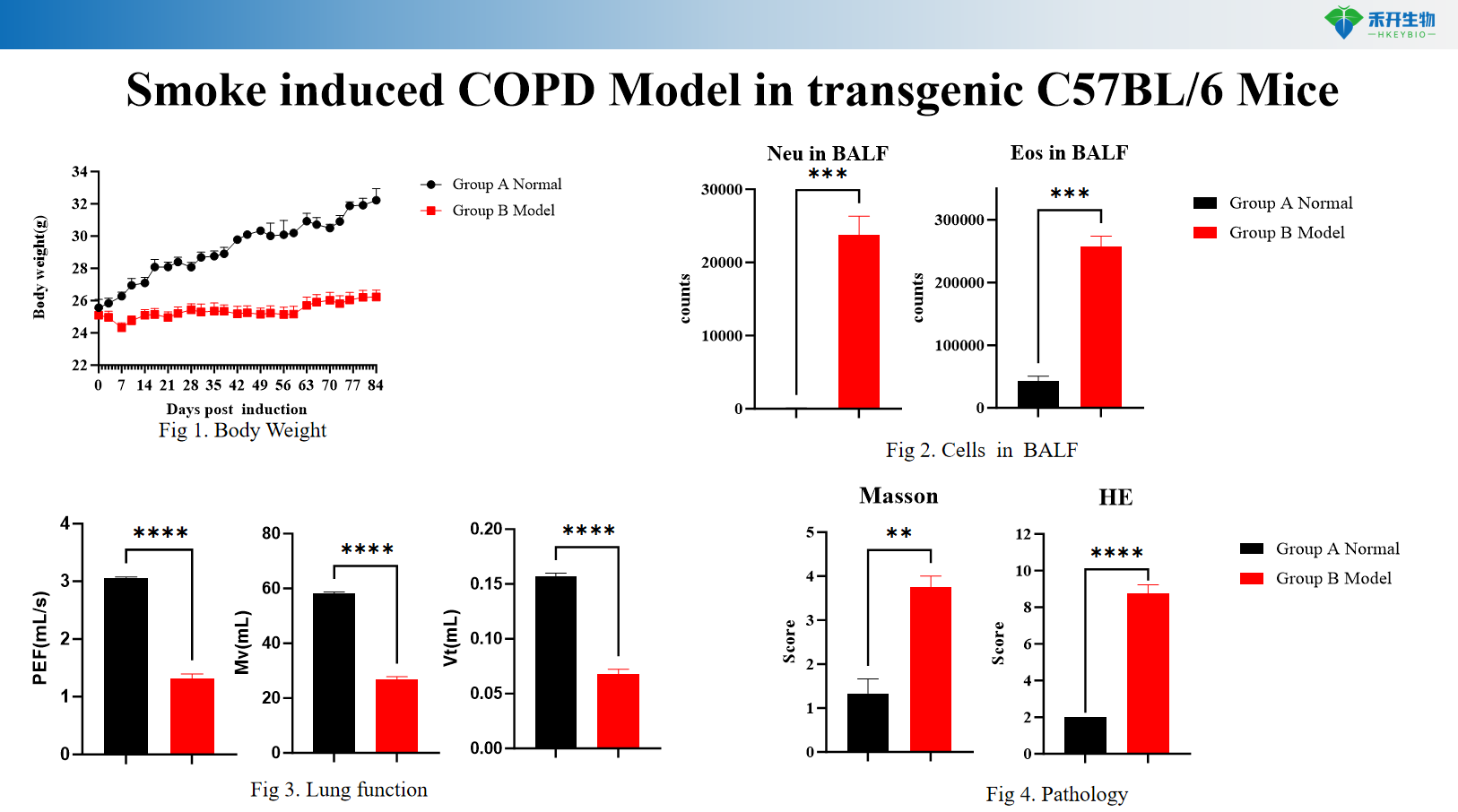
Modello di BPCO indotta dal fumo in topi transgenici C57BL/6
Modello di BPCO indotta da fumo + LPS nei ratti SD
• Test di efficacia di farmaci antinfiammatori (corticosteroidi, inibitori della PDE4, inibitori della p38 MAPK)
• Valutazione dei broncodilatatori (β2 agonisti, anticolinergici) e delle terapie combinate
• Test degli agenti attivi del muco e degli antiossidanti
• Convalida mirata delle vie dell'infiammazione e dello stress ossidativo
• Studi farmacologici e tossicologici a sostegno dell'IND
ambito |
Modello murino di malattia polmonare ostruttiva cronica |
Modello di ratto di malattia polmonare cronica ostruttiva |
Specie/ceppo |
Mouse C57BL/6 |
Ratto Sprague-Dawley |
metodo di induzione |
Esposizione cronica al fumo di sigaretta (solo corpo intero o naso) 5 giorni/settimana per 4-6 mesi + LPS intratracheale (1-2 volte/settimana) |
|
tempo di studio |
4–7 mesi (induzione + trattamento) |
4–7 mesi (induzione + trattamento) |
punto finale critico |
Peso corporeo, conta delle cellule BALF (totale e differenziale: macrofagi, monociti, neutrofili), funzione polmonare (resistenza, compliance, Penh), istopatologia (punteggio HE per enfisema e infiammazione), livelli di citochine nel BALF (IL-6, TNF-α, MCP-1), opzionale: marcatori di stress ossidativo, metaplasia delle cellule caliciformi (PAS), intercetta lineare media (MLI) | |
pacchetto |
Dati grezzi, rapporto di analisi, citologia BALF, dati di funzionalità polmonare, sezioni istologiche, risultati ELISA, bioinformatica (opzionale) | |
D: Perché il fumo di sigaretta e l'LPS vengono combinati nei modelli BPCO?
R: Il fumo di sigaretta induce infiammazione cronica ed enfisema, mentre l'LPS (che simula un'infezione batterica) aggrava l'infiammazione delle vie aeree e la produzione di muco. La combinazione replica più fedelmente la patologia della BPCO umana, comprese le riacutizzazioni.
D: Quali sono le principali somiglianze con la BPCO umana?
R: Questi modelli mostrano un'ostruzione progressiva del flusso aereo, infiammazione delle vie aeree (macrofagi, neutrofili), enfisema, metaplasia delle cellule mucipare caliciformi ed effetti sistemici che ricordano da vicino la BPCO umana.
D: Questi modelli possono essere utilizzati per studi di supporto IND?
Risposta: sì. Gli studi possono essere condotti secondo i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diversi tempi di esposizione al fumo, dosi di LPS)?
Risposta: certo. Il nostro team scientifico personalizza i protocolli di esposizione al fumo, il dosaggio di LPS e l'analisi degli endpoint in base al tuo specifico farmaco candidato.
