| Disponibilité : | |
|---|---|
| Quantité : | |











Pertinence clinique - La combinaison de la fumée de cigarette et de l'exposition aux lipopolysaccharides modélise l'étiologie et l'inflammation chronique de la maladie pulmonaire obstructive chronique chez l'homme.
Plusieurs espèces : des modèles de souris et de rats sont disponibles pour répondre à différentes exigences expérimentales (outils génétiques ou taille plus grande).
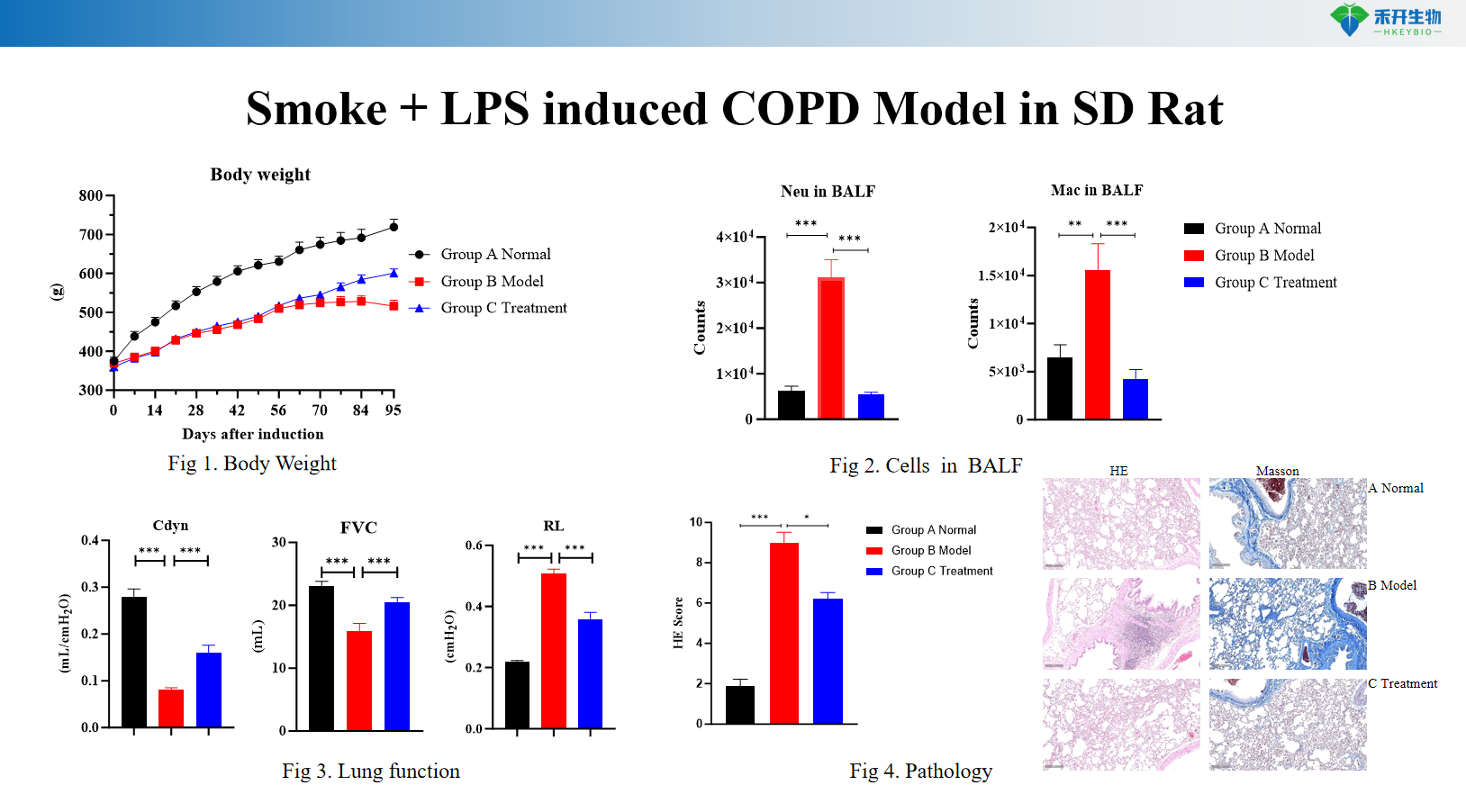
Critère d'évaluation complet : poids corporel, cytologie BALF (leucocytes, macrophages, monocytes), fonction pulmonaire (résistance, observance), histopathologie (score HE) et analyse des cytokines.
Valeur translationnelle – idéale pour tester les médicaments anti-inflammatoires (corticostéroïdes, inhibiteurs de la PDE4), les bronchodilatateurs et les mucolytiques.
IND Ready Packet – La recherche peut être menée conformément aux principes BPL.
La fumée + LPS induit un modèle de BPCO chez la souris C57BL/6
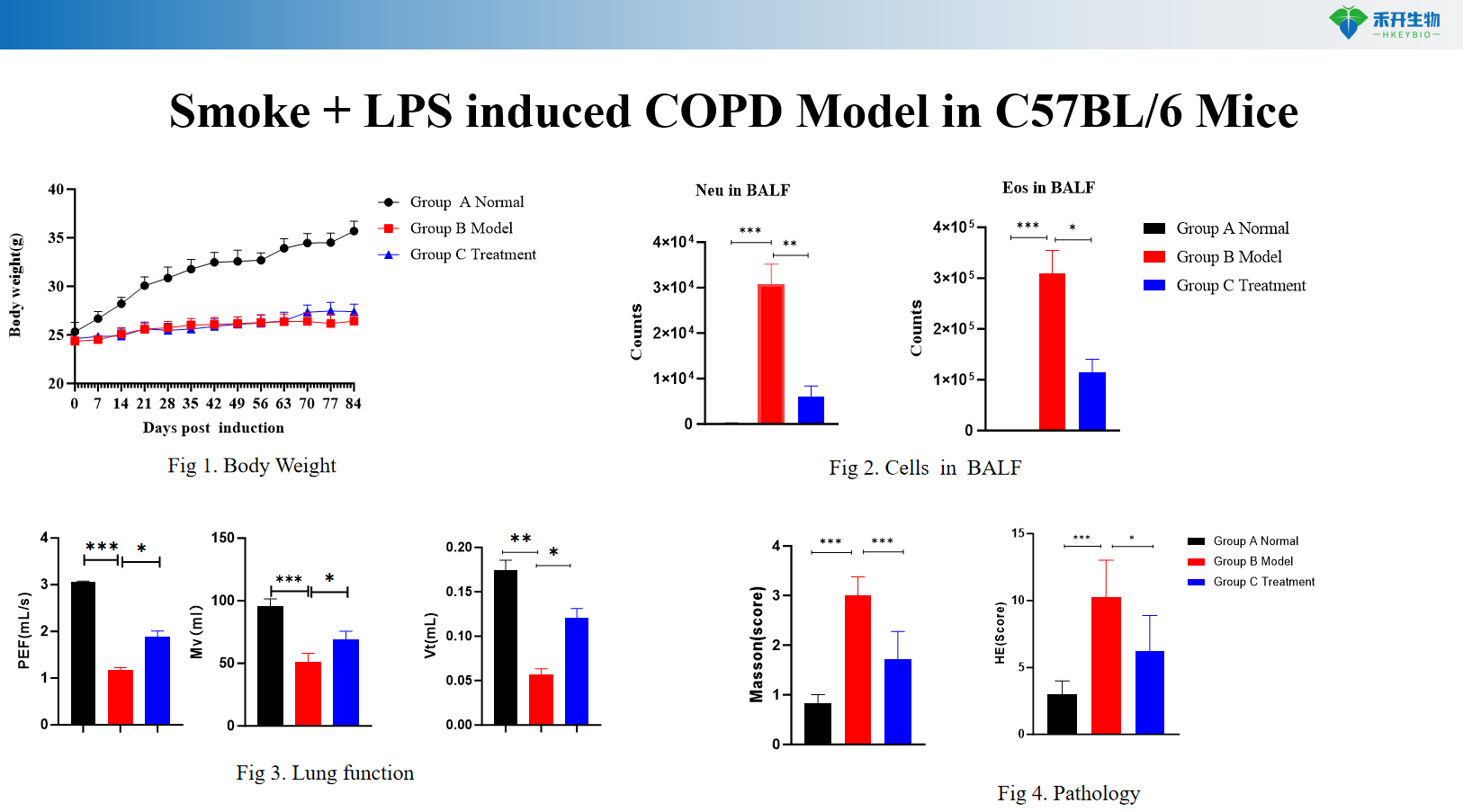
Modèle de BPCO induite par la fumée chez la souris C57BL/6
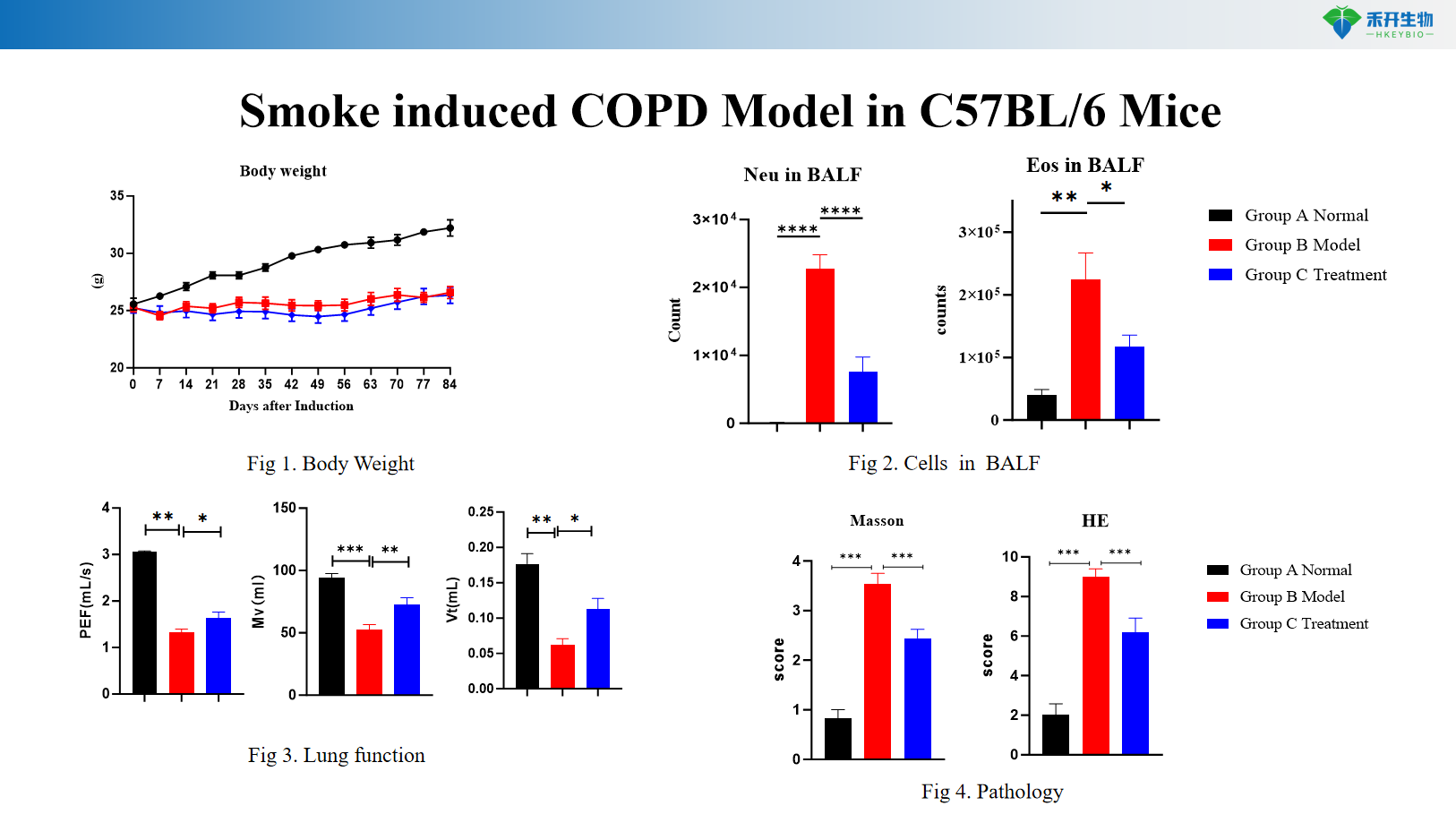
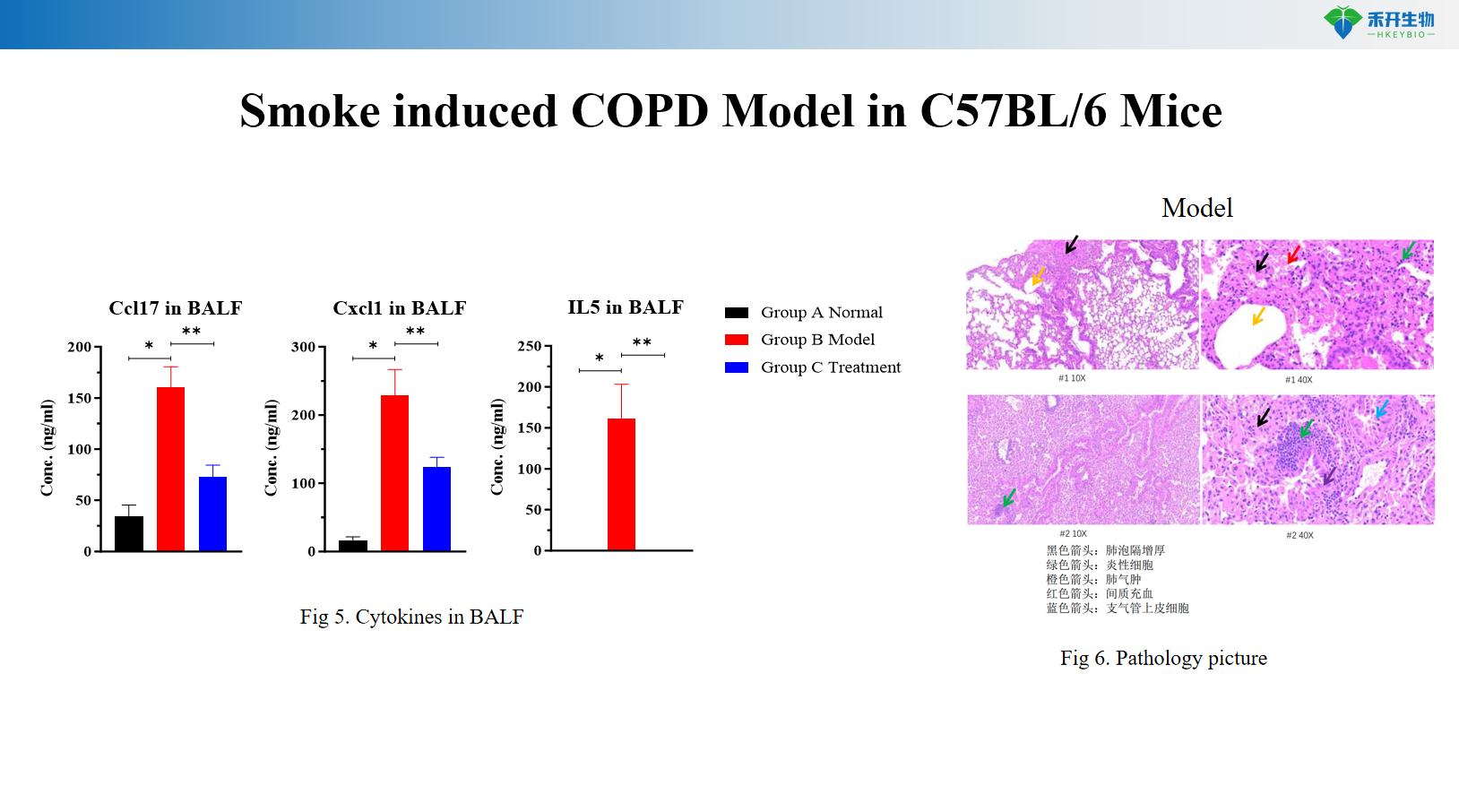
Modèle de BPCO induite par la fumée chez des souris transgéniques C57BL/6
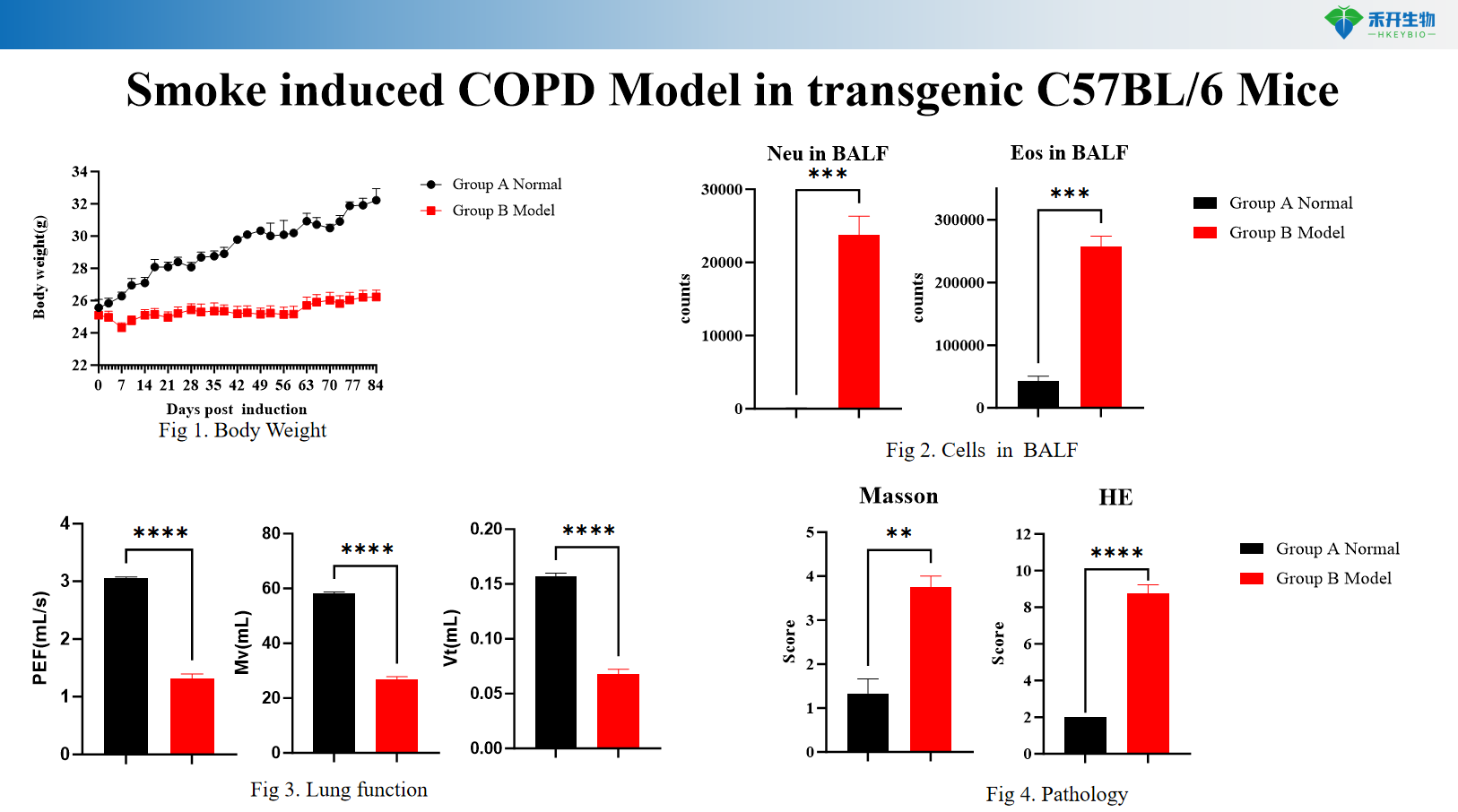
Modèle de BPCO induit par la fumée + LPS chez les rats SD
• Tests d'efficacité des médicaments anti-inflammatoires (corticostéroïdes, inhibiteurs de PDE4, inhibiteurs de p38 MAPK)
• Évaluation des bronchodilatateurs (agonistes β2, anticholinergiques) et des thérapies combinées
• Test des agents actifs du mucus et des antioxydants
• Validation ciblée des voies de l'inflammation et du stress oxydatif
• Études de pharmacologie et de toxicologie pour soutenir l'IND
portée |
Modèle de maladie pulmonaire obstructive chronique chez la souris |
Modèle de rat de maladie pulmonaire obstructive chronique |
Espèce/souche |
Souris C57BL/6 |
Rat Sprague-Dawley |
méthode d'induction |
Exposition chronique à la fumée de cigarette (corps entier ou nez uniquement) 5 jours/semaine pendant 4 à 6 mois + LPS intratrachéal (1 à 2 fois/semaine) |
|
temps d'étude |
4 à 7 mois (induction + traitement) |
4 à 7 mois (induction + traitement) |
point final critique |
Poids corporel, numération cellulaire BALF (totale et différentielle : macrophages, monocytes, neutrophiles), fonction pulmonaire (résistance, observance, Penh), histopathologie (score HE pour l'emphysème et l'inflammation), taux de cytokines dans BALF (IL-6, TNF-α, MCP-1), facultatif : marqueurs de stress oxydatif, métaplasie des cellules caliciformes (PAS), intercept linéaire moyen (MLI). | |
paquet |
Données brutes, rapport d'analyse, cytologie BALF, données de fonction pulmonaire, coupes histologiques, résultats ELISA, bioinformatique (facultatif) | |
Q : Pourquoi la fumée de cigarette et le LPS sont-ils combinés dans les modèles BPCO ?
R : La fumée de cigarette induit une inflammation chronique et un emphysème, tandis que le LPS (simulant une infection bactérienne) exacerbe l'inflammation des voies respiratoires et la production de mucus. La combinaison reproduit plus fidèlement la pathologie de la BPCO humaine, y compris les exacerbations aiguës.
Q : Quelles sont les principales similitudes avec la BPCO humaine ?
R : Ces modèles présentent une obstruction progressive des voies respiratoires, une inflammation des voies respiratoires (macrophages, neutrophiles), un emphysème, une métaplasie des cellules caliciformes et des effets systémiques qui ressemblent beaucoup à la BPCO humaine.
Q : Ces modèles peuvent-ils être utilisés pour les études de support IND ?
Réponse : Oui. Les études peuvent être menées selon les principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différentes durées d'exposition à la fumée, doses de LPS) ?
Réponse : Bien sûr. Notre équipe scientifique adapte les protocoles d'exposition à la fumée, le dosage du LPS et l'analyse des paramètres à votre candidat-médicament spécifique.
