| Ketersediaan: | |
|---|---|
| Kuantiti: | |











Perkaitan Klinikal - Gabungan asap rokok dan pendedahan lipopolisakarida memodelkan etiologi dan keradangan kronik penyakit pulmonari obstruktif kronik pada manusia.
Berbilang spesies - model tetikus dan tikus tersedia untuk memenuhi keperluan percubaan yang berbeza (alat genetik berbanding saiz yang lebih besar).
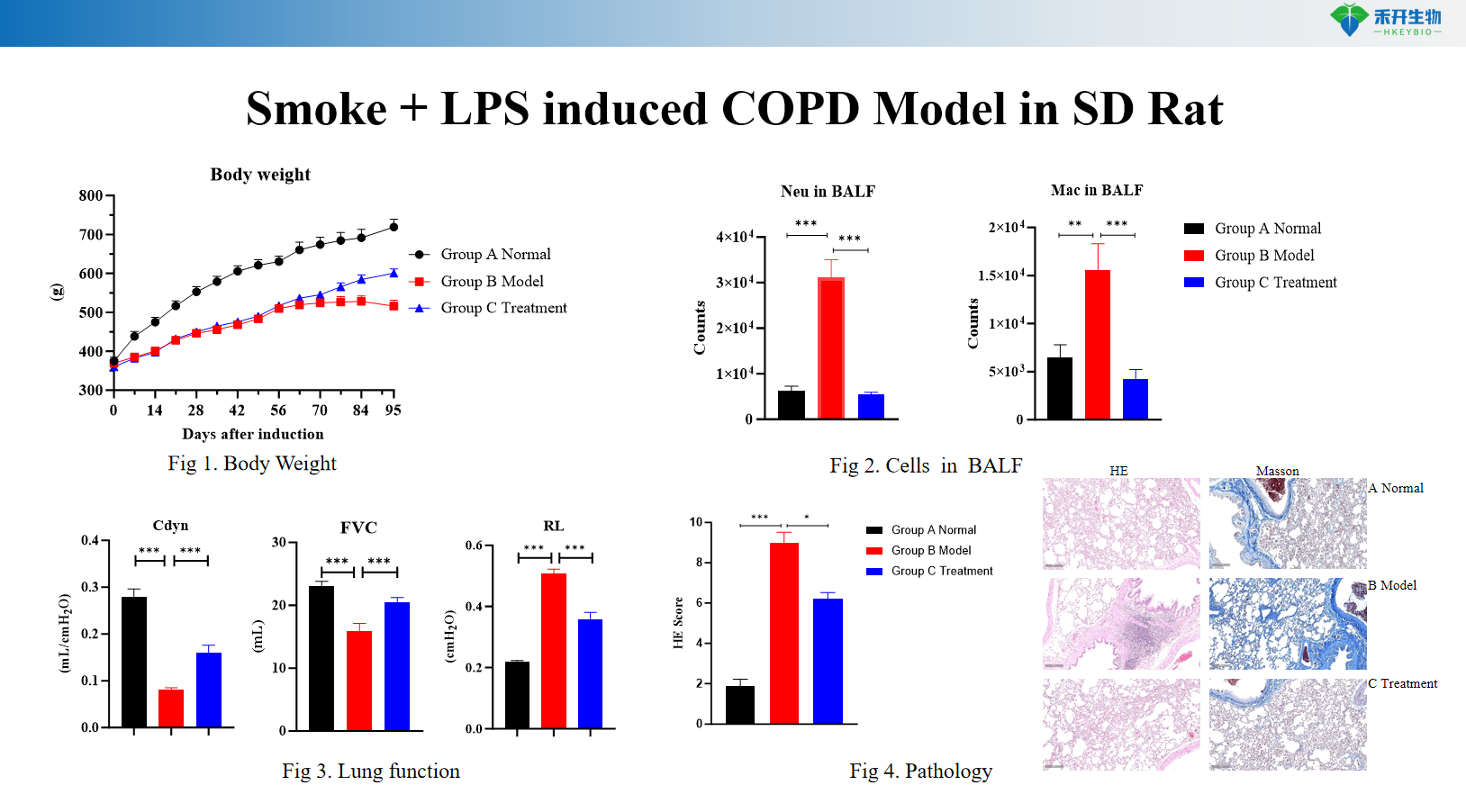
Titik akhir yang komprehensif - berat badan, sitologi BALF (leukosit, makrofaj, monosit), fungsi paru-paru (rintangan, pematuhan), histopatologi (skor HE), dan analisis sitokin.
Nilai translasi – sesuai untuk menguji ubat anti-radang (kortikosteroid, perencat PDE4), bronkodilator dan mukolitik.
Paket Sedia IND – Penyelidikan boleh dijalankan mengikut prinsip GLP.
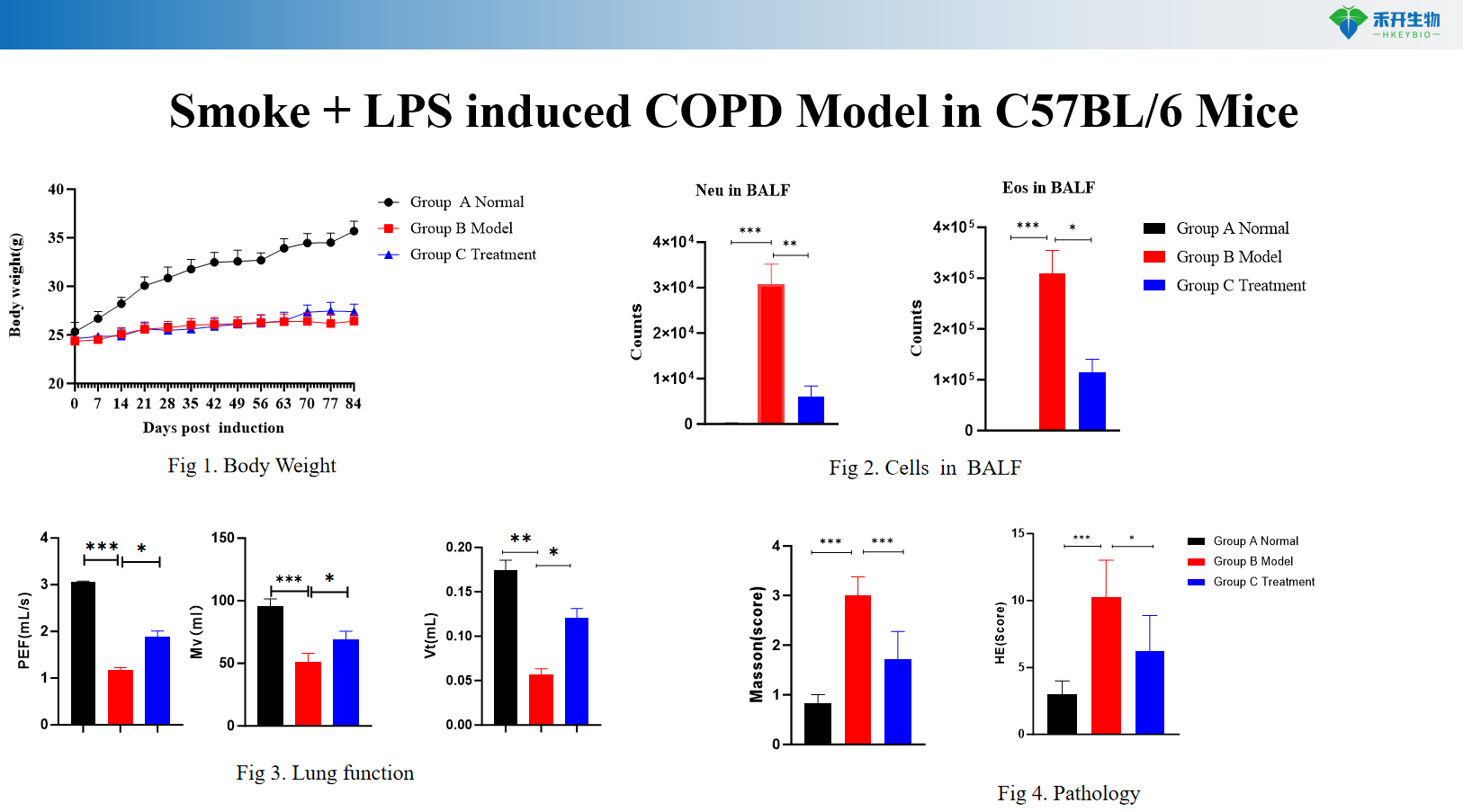
Asap + LPS mendorong model COPD tetikus C57BL/6
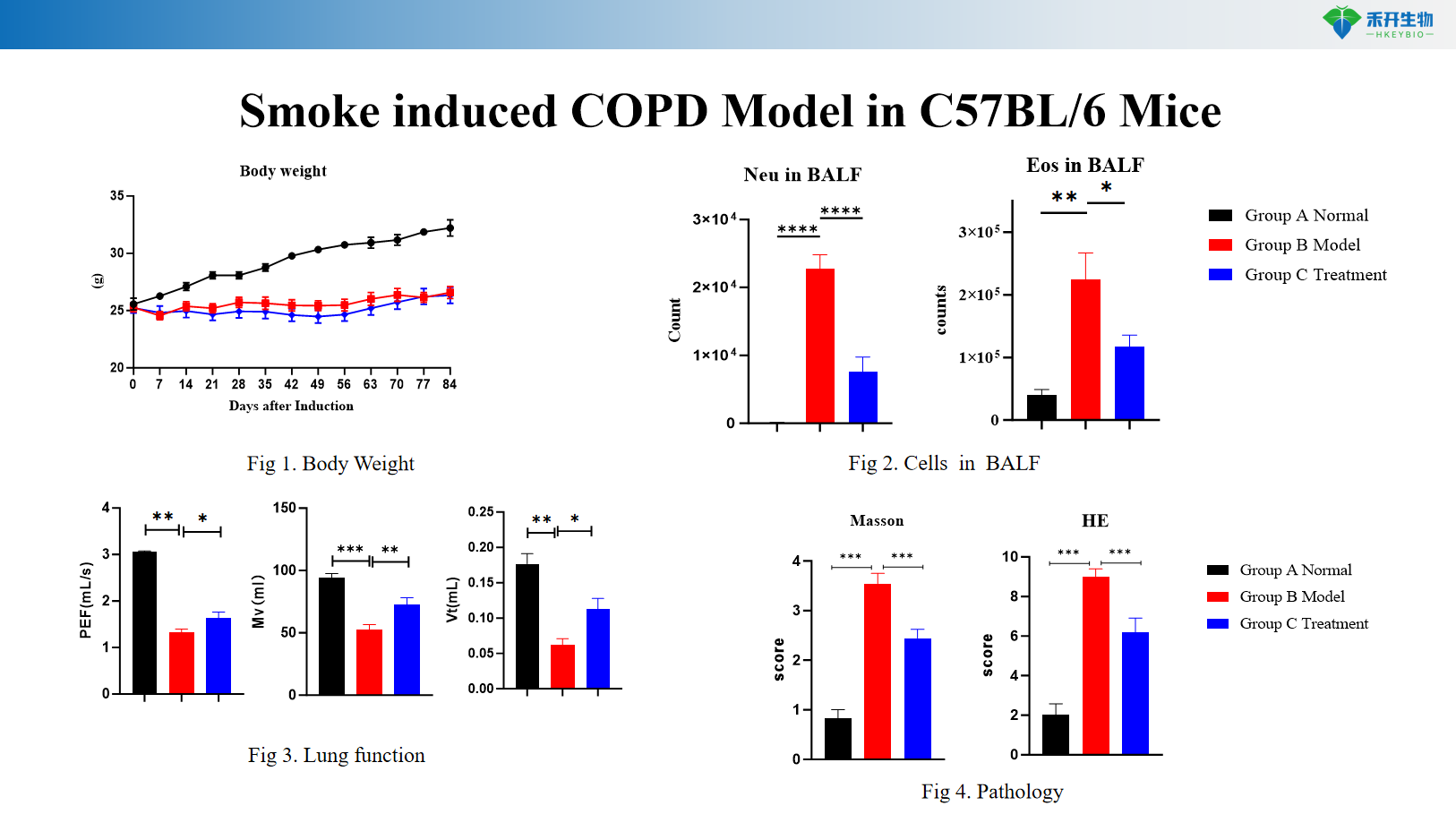
Model COPD akibat asap tetikus C57BL/6
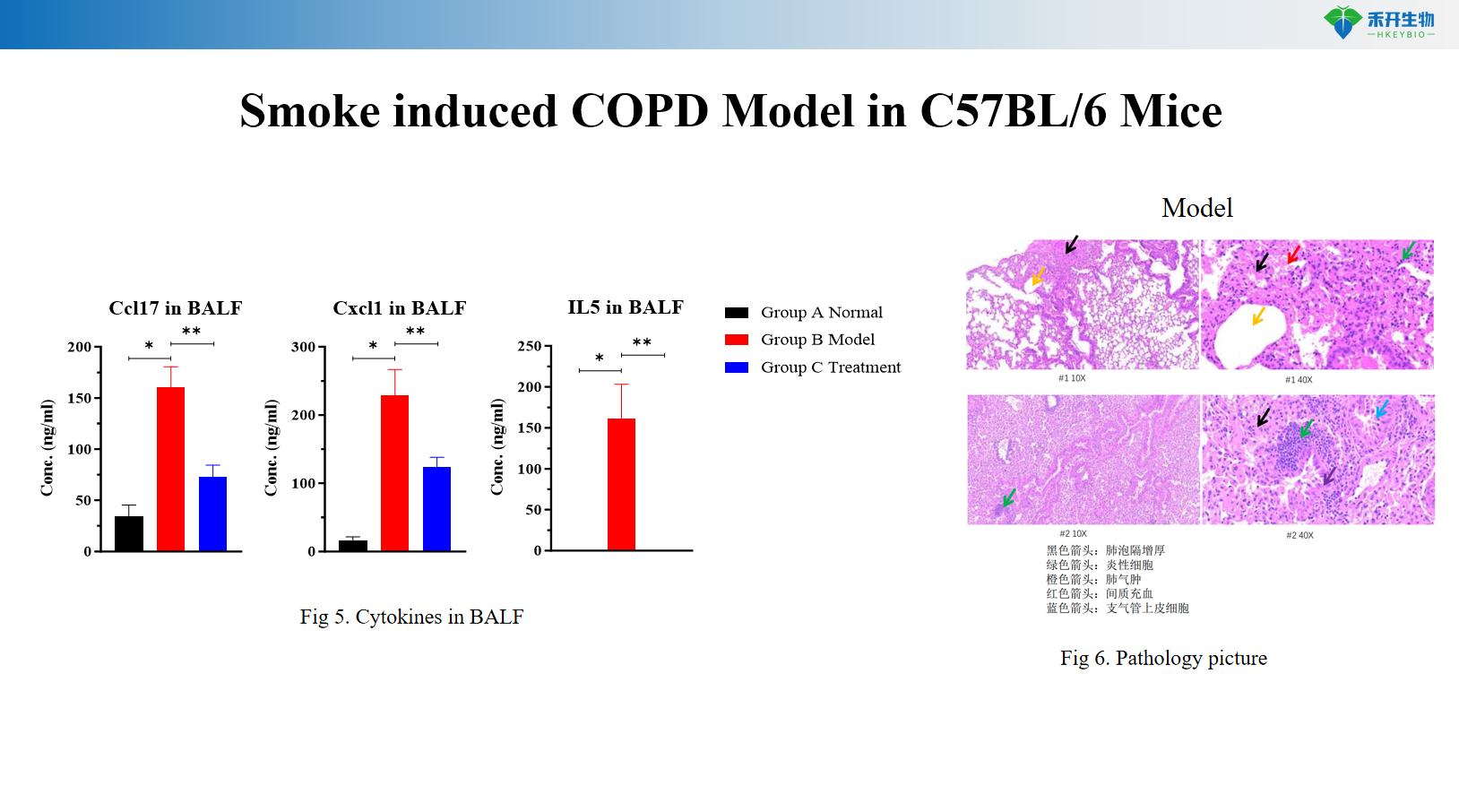
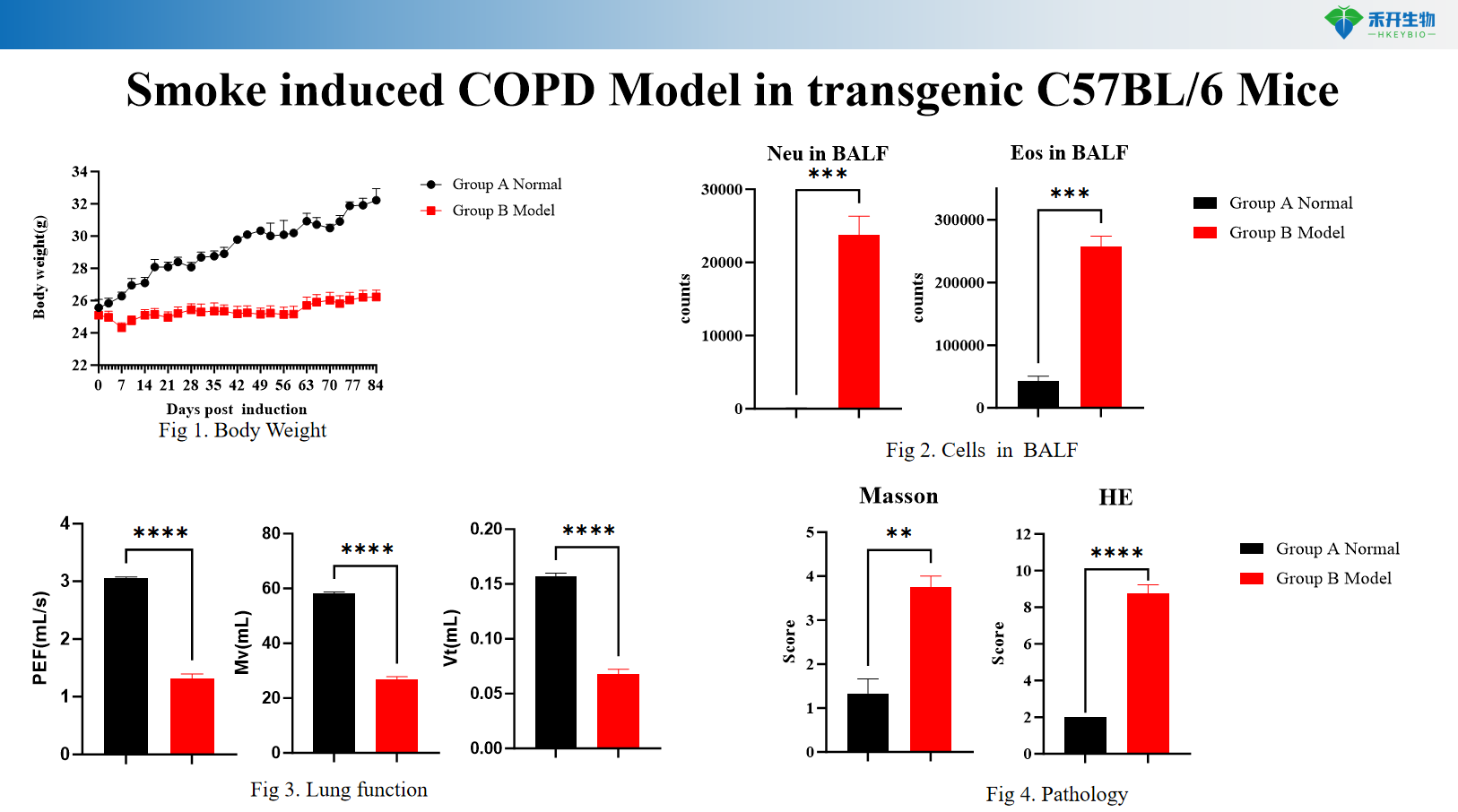
Model COPD yang disebabkan oleh asap dalam tikus C57BL/6 transgenik
Model COPD teraruh Asap + LPS dalam tikus SD
• Ujian keberkesanan ubat anti-radang (kortikosteroid, perencat PDE4, perencat p38 MAPK)
• Penilaian bronkodilator (agonis β2, antikolinergik) dan terapi gabungan
• Ujian agen aktif mukus dan antioksidan
• Pengesahan sasaran keradangan dan laluan tekanan oksidatif
• Kajian farmakologi dan toksikologi untuk menyokong IND
skop |
Model penyakit pulmonari obstruktif kronik tikus |
Model tikus penyakit pulmonari obstruktif kronik |
Spesies/Terikan |
C57BL/6 tetikus |
Tikus Sprague-Dawley |
kaedah induksi |
Pendedahan asap rokok kronik (seluruh badan atau hidung sahaja) 5 hari/minggu selama 4-6 bulan + LPS intratracheal (1-2 kali/minggu) |
|
masa belajar |
4-7 bulan (induksi + rawatan) |
4-7 bulan (induksi + rawatan) |
titik akhir kritikal |
Berat badan, kiraan sel BALF (jumlah dan pembezaan: makrofaj, monosit, neutrofil), fungsi paru-paru (rintangan, pematuhan, Penh), histopatologi (skor HE untuk emfisema dan keradangan), tahap sitokin dalam BALF (IL-6, TNF-α, MCP-1), pilihan: penanda tekanan oksidatif, sel goblet metaplasia (metaplasia sel goblet) | |
peket |
Data mentah, laporan analisis, sitologi BALF, data fungsi paru-paru, bahagian histologi, keputusan ELISA, bioinformatik (pilihan) | |
S: Mengapa asap rokok dan LPS digabungkan dalam model COPD?
A: Asap rokok menyebabkan keradangan kronik dan emfisema, manakala LPS (mensimulasikan jangkitan bakteria) memburukkan lagi keradangan saluran pernafasan dan pengeluaran lendir. Gabungan lebih rapat mereplikasi patologi COPD manusia, termasuk pemburukan akut.
S: Apakah persamaan utama dengan COPD manusia?
J: Model ini mempamerkan halangan aliran udara yang progresif, keradangan saluran udara (makrofaj, neutrofil), emfisema, metaplasia sel goblet, dan kesan sistemik yang hampir menyerupai COPD manusia.
S: Bolehkah model ini digunakan untuk kajian sokongan IND?
Jawapan: Ya. Kajian boleh dijalankan mengikut prinsip GLP untuk penyerahan peraturan (FDA, EMA).
S: Adakah anda menawarkan protokol kajian tersuai (cth, masa pendedahan asap yang berbeza, dos LPS)?
Jawapan: Sudah tentu. Pasukan saintifik kami menyesuaikan protokol pendedahan asap, dos LPS dan analisis titik akhir kepada calon ubat khusus anda.
