| Disponibilidad: | |
|---|---|
| Cantidad: | |











Amplia cartera de modelos : cubre la RSC eosinófila (papaína), la RSC inducida por proteasas fúngicas (Aspergillus), la RSC asociada a superantígenos (SEB) y la rinitis alérgica clásica (OVA).
Múltiples cepas : C57BL/6 y BALB/c disponibles para adaptarse a diferentes orígenes genéticos y sesgos Th1/Th2.
Criterios de valoración integrales : peso corporal, recuento de células del lavado nasal (eosinófilos, células totales), IgE sérica (total y específica de OVA), comportamiento de rascado nasal, histopatología de la mucosa nasal (HE), perfil de citocinas (IL-33, citocinas Th2).
Valor traslacional : ideal para probar corticosteroides, antihistamínicos, productos biológicos (anti-IgE, anti-IL-5, anti-IL-4Rα) y nuevos inmunomoduladores.
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
Modelo de rinosinusitis eosinofílica C57BL/6 inducida por papaína
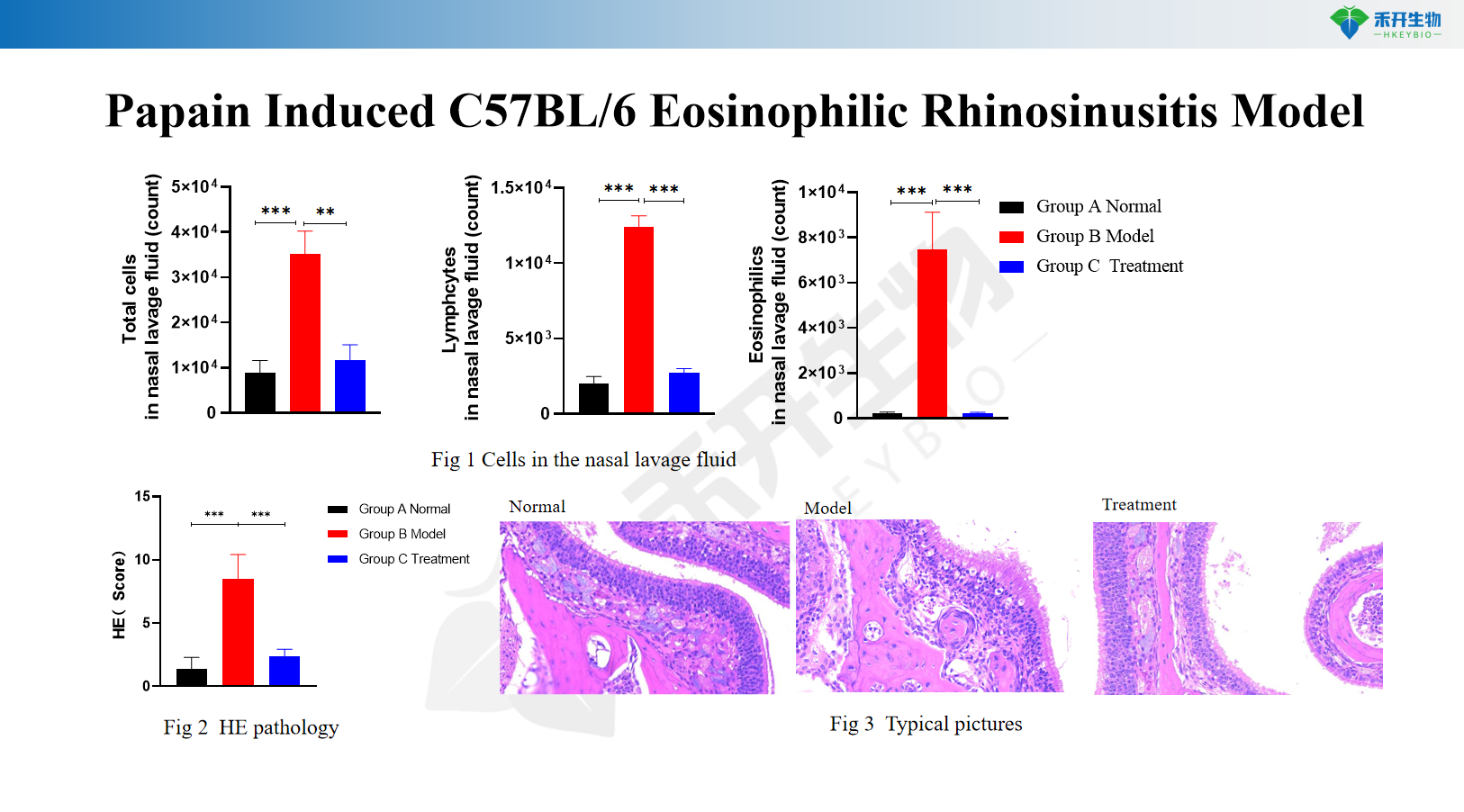
Modelo C57BL/6 CRS inducido por proteinasa de Aspergillus oryzae y OVA
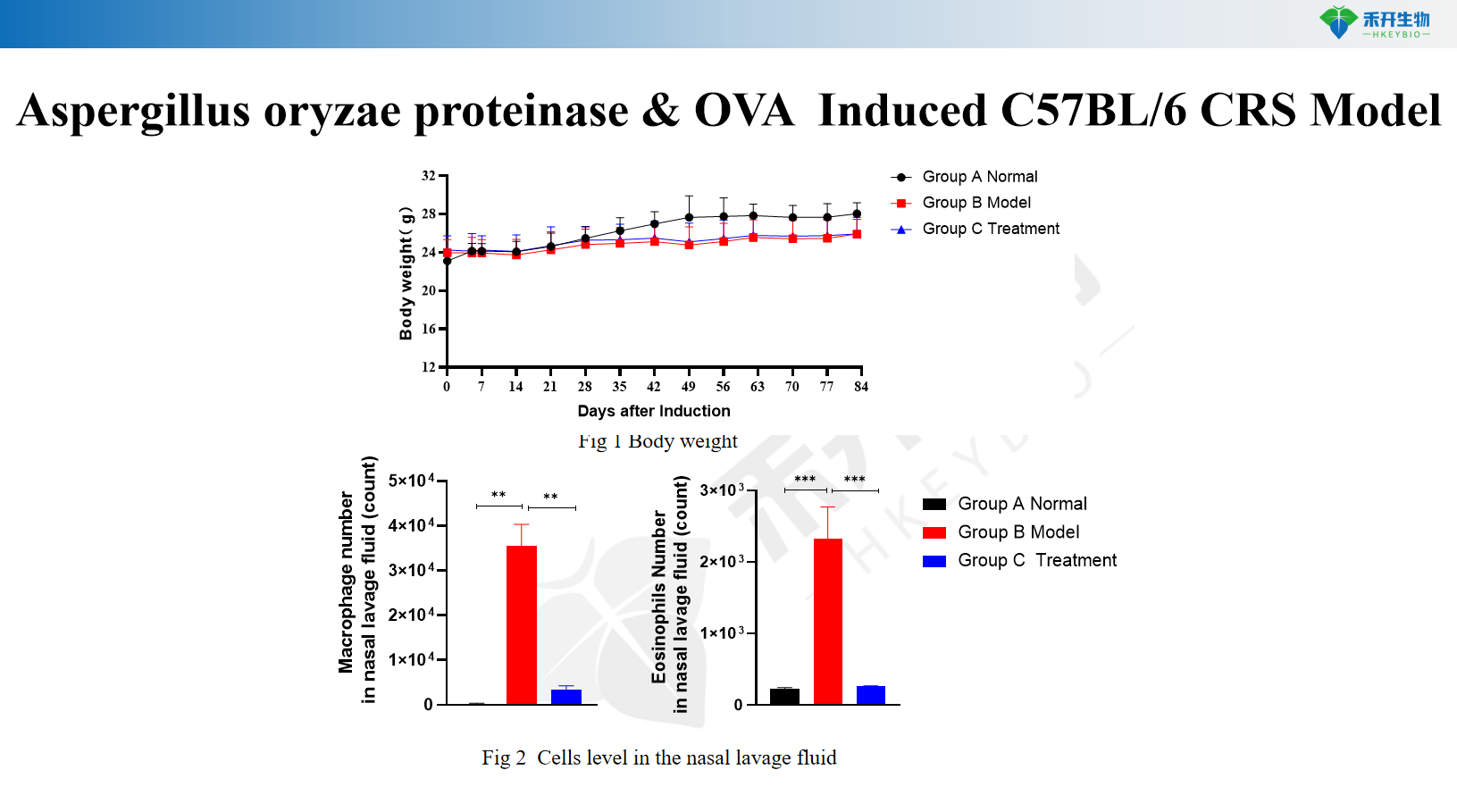
Modelo BALB/c CRS inducido por proteinasa de Aspergillus oryzae y OVA
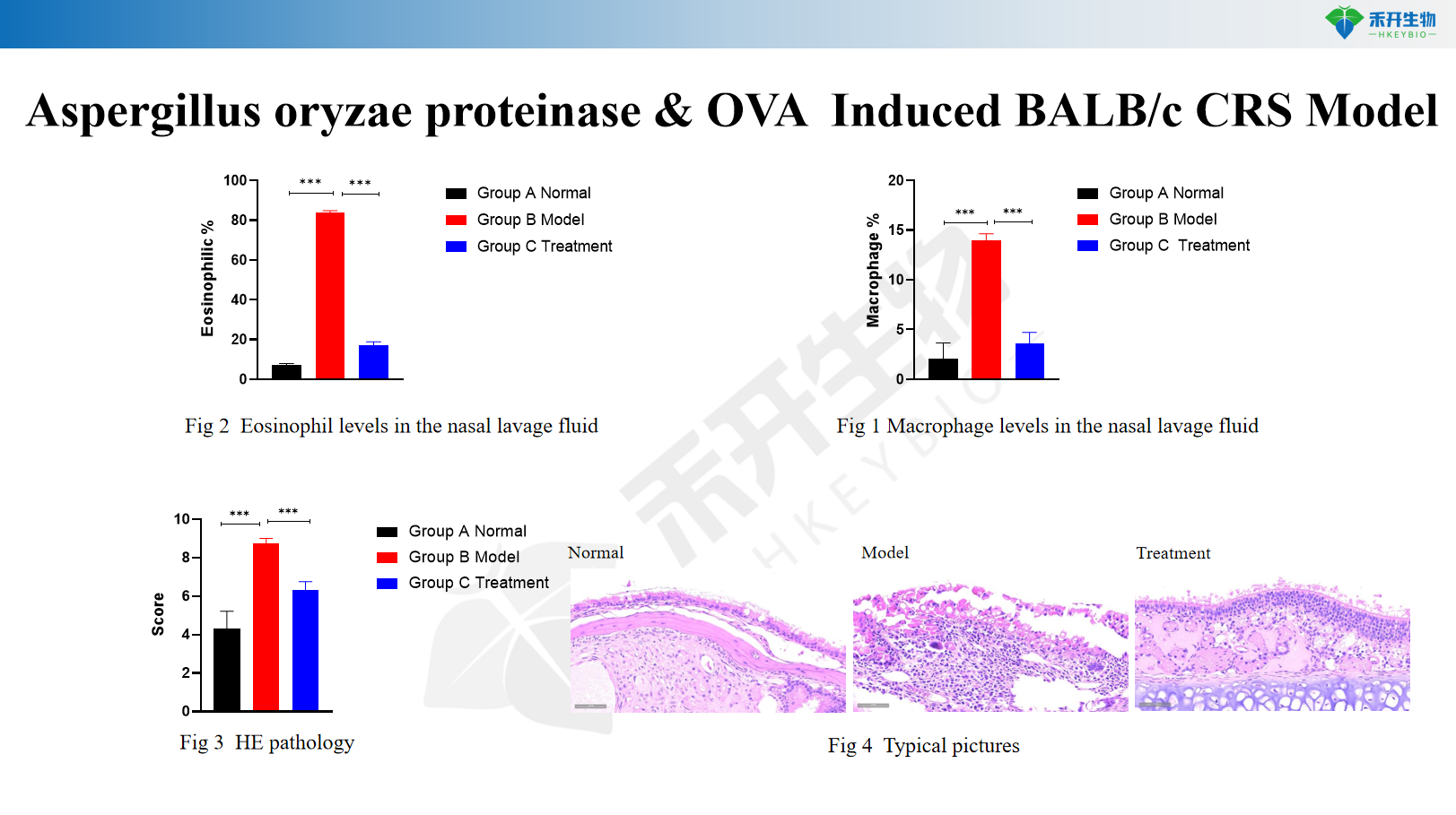
Modelo CRS inducido por SEB y OVA
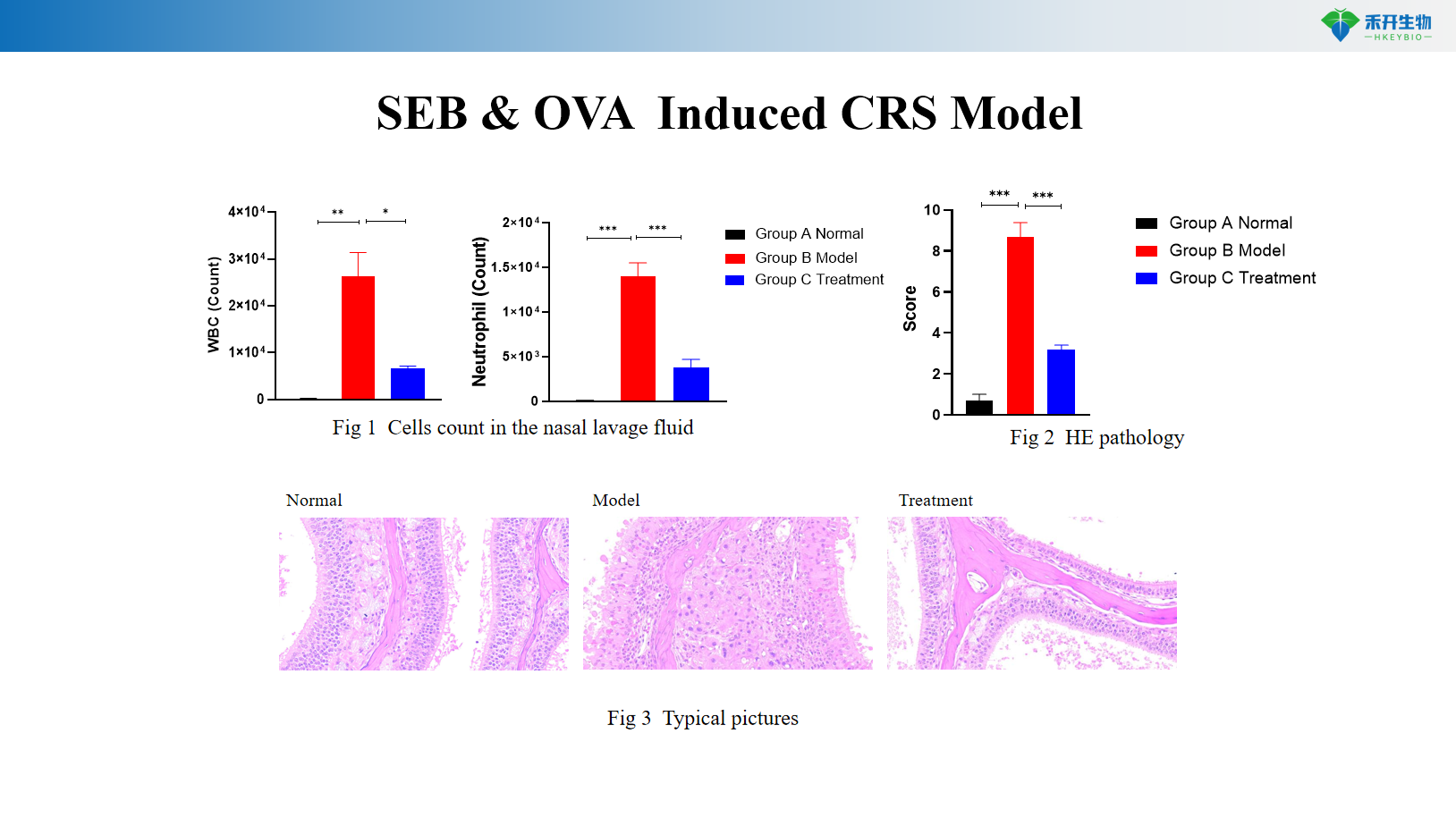
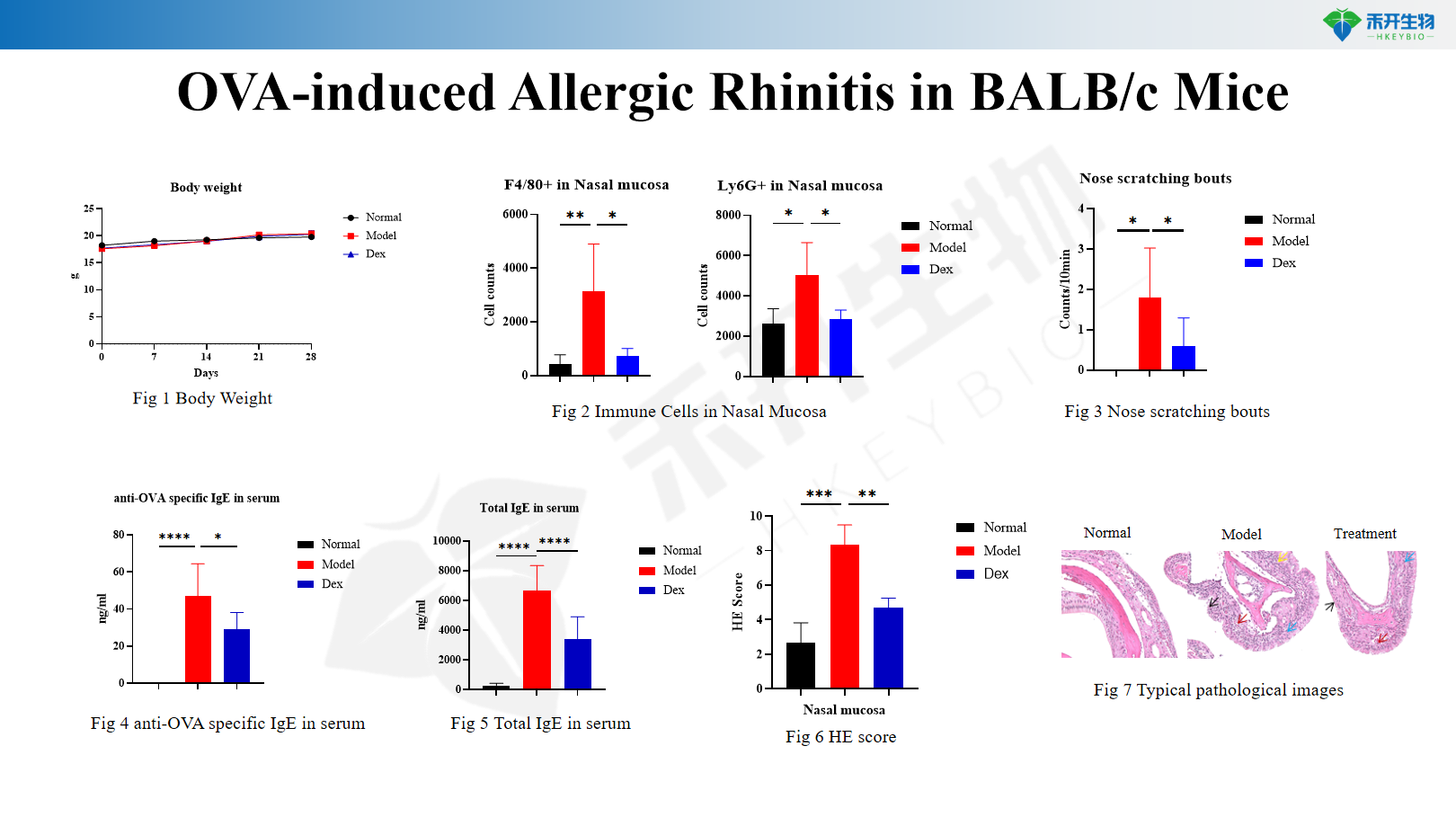
Rinitis alérgica inducida por OVA en ratones BALB/c
• Pruebas de eficacia de corticosteroides, antihistamínicos y descongestionantes intranasales y sistémicos
• Evaluación de productos biológicos dirigidos a las vías Th2 (anti-IL-4Rα, anti-IL-5, anti-IL-13, anti-IgE)
• Validación de objetivos para citoquinas derivadas de epitelio (TSLP, IL-33, IL-25) y vías activadas por proteasas
• Descubrimiento de biomarcadores (IgE, peroxidasa de eosinófilos, firmas de citocinas)
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Especificación |
Especie/Cepa |
Ratón (C57BL/6, BALB/c) |
Método de inducción |
Papaína (proteasa); Proteasa de Aspergillus + OVA; SEB + OVA; OVA + alumbre |
Duración del estudio |
3 a 6 semanas (fases de sensibilización + desafío) |
Puntos finales clave |
Peso corporal, recuento de células del lavado nasal (total y diferencial), IgE total sérica e IgE específica de OVA, comportamiento de rascado nasal (rinitis alérgica), histopatología de la mucosa nasal (puntuación HE para inflamación, infiltración eosinofílica, hiperplasia de células caliciformes), niveles de citoquinas (IL-4, IL-5, IL-13, IL-33) en tejido/lavado nasal |
Paquete de datos |
Datos brutos, informes de análisis, citología de lavado nasal, resultados de ELISA, portaobjetos de histología, datos de comportamiento, bioinformática (opcional) |
P: ¿Cómo elijo el modelo correcto para mi fármaco candidato?
R: Para CRS eosinófilo, se recomiendan los modelos de papaína o proteasa de Aspergillus. Para la RSC asociada a superantígeno, el modelo SEB+OVA es apropiado. Para la rinitis alérgica clásica, el modelo OVA es la opción estándar. Los ratones BALB/c exhiben respuestas Th2 más fuertes, mientras que C57BL/6 permiten el uso de líneas transgénicas. Nuestro equipo científico puede guiar la selección del modelo en función de su objetivo específico.
P: ¿Cuál es el papel de la actividad de la proteasa en los modelos CRS?
R: Las proteasas (papaína, proteasa de Aspergillus) alteran las uniones estrechas epiteliales, lo que provoca una disfunción de la barrera y la liberación de citocinas epiteliales (IL-33, TSLP), que provocan inflamación tipo 2 e infiltración eosinofílica, imitando la fisiopatología de la RSC humana.
P: ¿Se pueden utilizar estos modelos para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes dosis de alérgenos, programas de sensibilización)?
R: Absolutamente. Nuestro equipo científico adapta los protocolos de inducción, los programas de tratamiento y los análisis de criterios de valoración a su fármaco candidato específico.
