| Disponibilidad: | |
|---|---|
| Cantidad: | |











Clínicamente relevante : la ALI inducida por LPS imita estrechamente la ALI/SDRA humana con inflamación aguda, infiltración de leucocitos y edema pulmonar.
Criterios de valoración integrales : recuento de células BALF (linfocitos, neutrófilos, macrófagos), perfil de citocinas (MCP-1, IL-6, IL-10), histopatología pulmonar (HE, IHC), evaluación del edema pulmonar (proporción húmedo/seco).
Impulsado por mecanismos : el LPS activa la señalización de TLR4, lo que desencadena la vía NF-κB y una respuesta inflamatoria sólida, que refleja la lesión pulmonar inducida por la sepsis por gramnegativos.
Valor traslacional : ideal para probar medicamentos antiinflamatorios, inhibidores de citocinas, inhibidores de la elastasa de neutrófilos y terapias celulares.
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
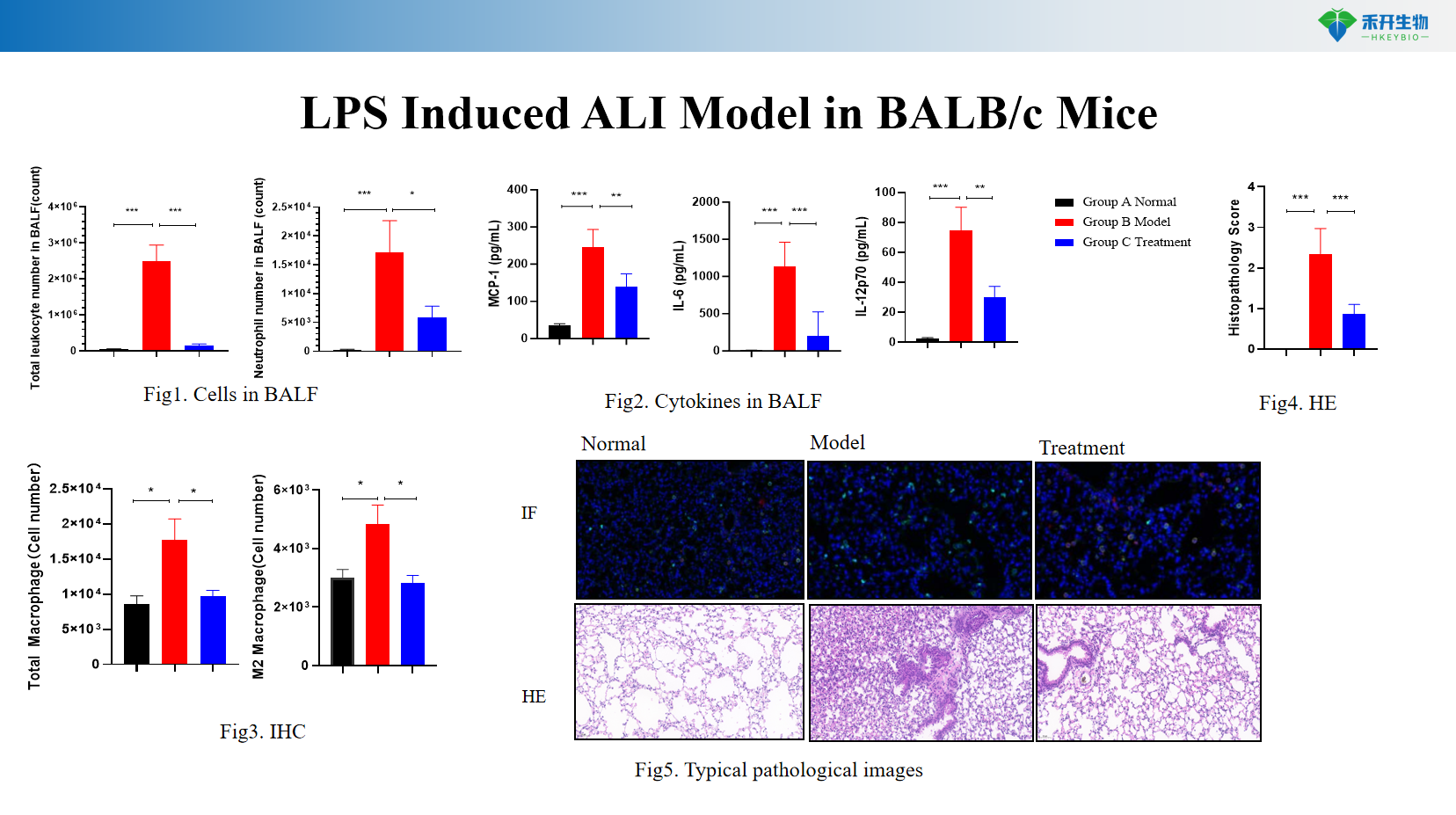
Modelo ALI inducido por LPS en ratones BALB/c
• Pruebas de eficacia de fármacos antiinflamatorios (corticosteroides, AINE), inhibidores de citocinas (anti-IL-6, anti-TNF-α) e inhibidores de la elastasa de neutrófilos
• Evaluación de la terapia con células madre mesenquimales (MSC) y tratamientos basados en vesículas extracelulares
• Validación de objetivos para la señalización de TLR4, la vía NF-κB y las cascadas inflamatorias
• Descubrimiento de biomarcadores (perfiles de células BALF, firmas de citocinas, marcadores de lesión pulmonar)
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Especificación |
Especie/Cepa |
Ratón BALB/c |
Método de inducción |
Administración intratraqueal, intranasal o intraperitoneal de lipopolisacárido (LPS, 5 a 10 mg/kg) |
Duración del estudio |
Agudo: 6 a 48 horas después de la administración de LPS |
Puntos finales clave |
Recuento de células BALF (total y diferencial: neutrófilos, macrófagos, linfocitos), niveles de citoquinas BALF (MCP-1, IL-6, IL-10 por ELISA), histopatología pulmonar (tinción HE con puntuación de lesión pulmonar), inmunohistoquímica (IHC) para marcadores inflamatorios, relación de peso seco/húmedo del pulmón (edema pulmonar), opcional: actividad MPO, marcadores de estrés oxidativo |
Paquete de datos |
Datos sin procesar, informes de análisis, recuentos de células BALF, resultados de ELISA, portaobjetos de histología (HE, IHC), bioinformática (opcional) |
P: ¿Cómo induce el LPS una lesión pulmonar aguda en ratones?
R: El LPS se une al TLR4 en las células inmunes, activando las vías NF-κB y MAPK, lo que conduce a una respuesta inflamatoria robusta con liberación de citocinas (IL-6, TNF-α, MCP-1), reclutamiento de neutrófilos en los pulmones, aumento de la permeabilidad vascular y daño alveolar, imitando de cerca la ALI inducida por sepsis por gramnegativos.
P: ¿Cuáles son las similitudes clave con ALI/ARDS humanos?
R: El modelo muestra infiltración de neutrófilos, citocinas proinflamatorias elevadas, edema pulmonar y características histopatológicas (engrosamiento alveolar, formación de membrana hialina) idénticas a las de ALI/SDRA humano.
P: ¿Se puede utilizar este modelo para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes dosis de LPS, vías de administración, momentos temporales)?
R: Absolutamente. Nuestro equipo científico adapta los regímenes de dosificación, las rutas de administración y los análisis de criterios de valoración de LPS a su fármaco candidato específico.
