| Disponibilidad: | |
|---|---|
| Cantidad: | |











Amplia cartera de modelos : modelos de análogos de hapteno, citoquinas, alérgenos y vitamina D que cubren endotipos de EA aguda, crónica y Th2/Th17/Th22 dominante.
Múltiples especies/cepas : BALB/c (propensa a Th2), C57BL/6 (propensa a Th1/Th17) y rata SD disponibles.
Criterios de valoración integrales : peso corporal, grosor de la oreja, puntuación de la piel, eventos de picazón, IgE sérica, perfil de citoquinas (IL-4, IL-13, IL-17, IL-36), histopatología (HE, azul de toluidina), grosor epidérmico.
Valor traslacional : ideal para probar inhibidores de JAK, productos biológicos (anti‑IL‑4Rα, anti‑IL‑13), inhibidores de PDE4 y agentes tópicos.
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
Modelo DNCB Inducido C57BL/6 AD
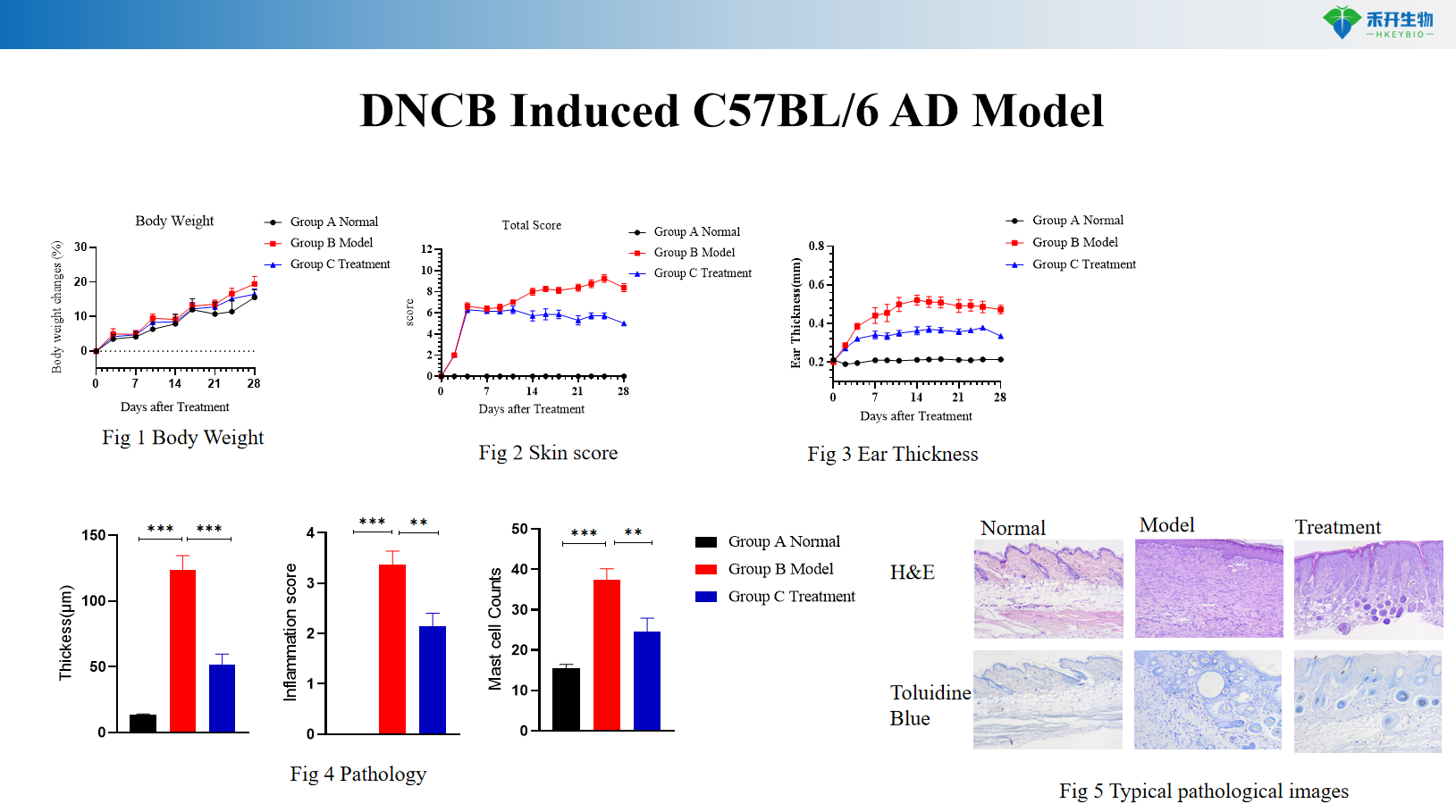
Modelo de AD inducido por DNCB en ratones BALB/c
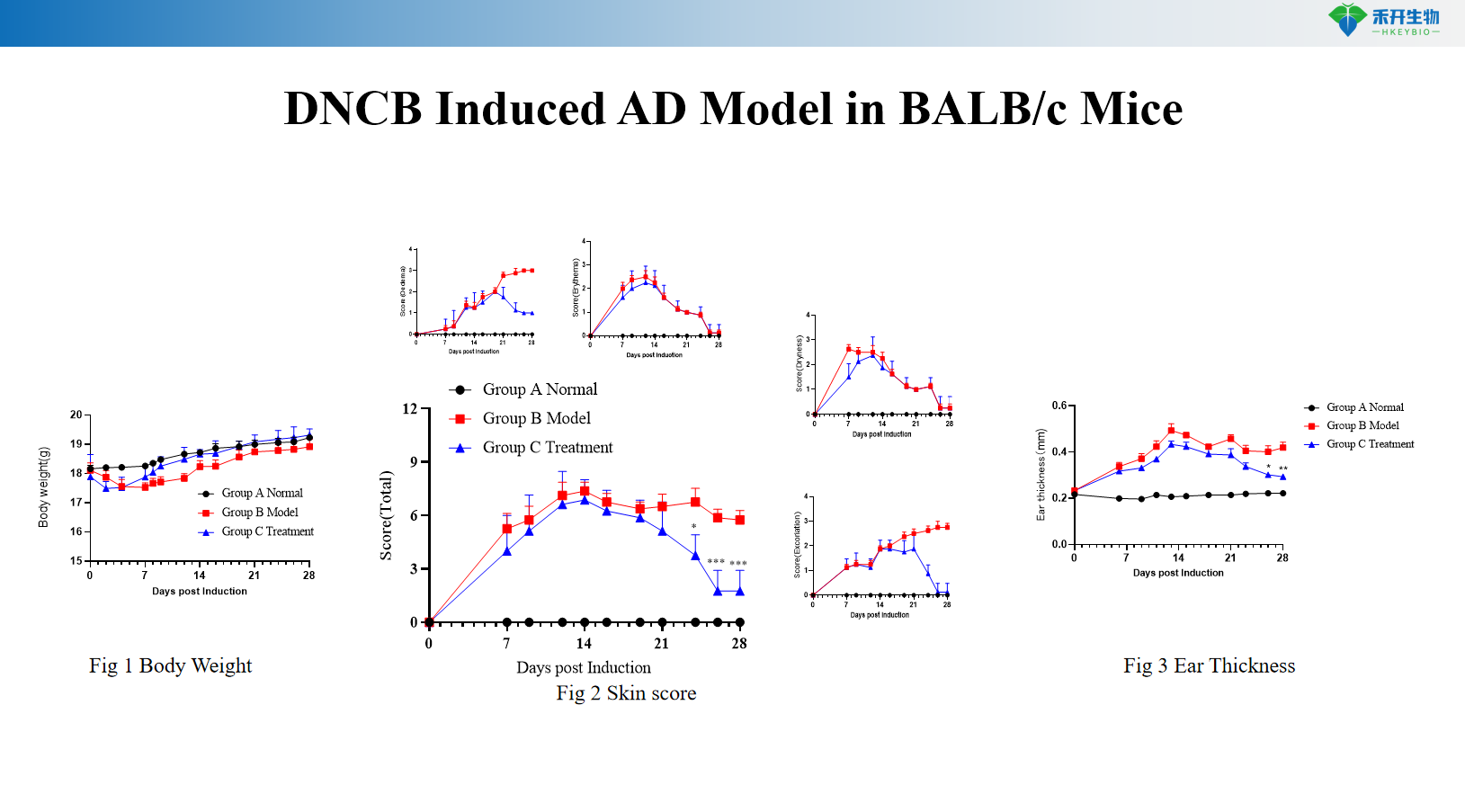
Modelo C57BL/6 AD inducido por OXA
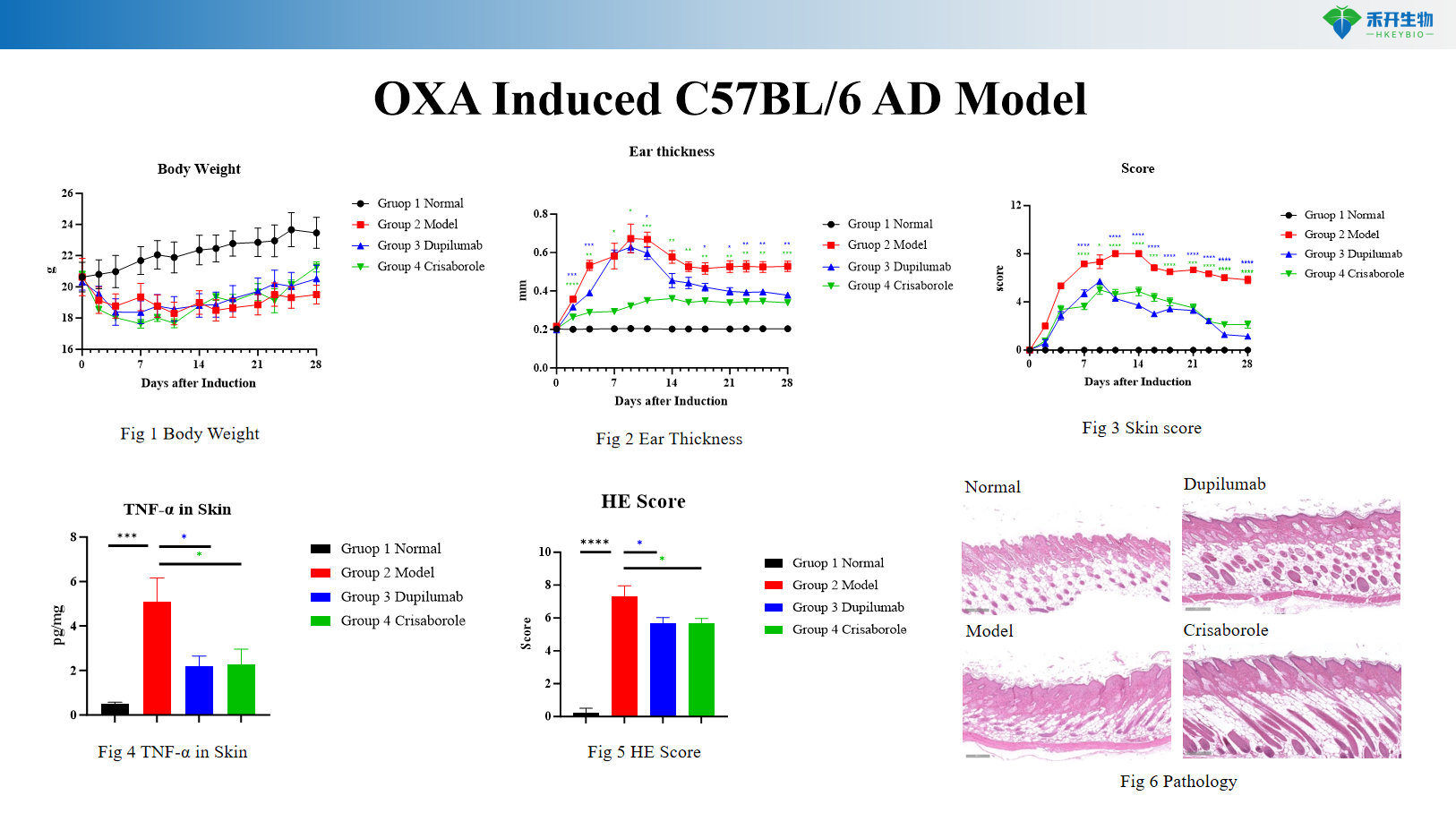
Modelo BALB/c AD inducido por OXA
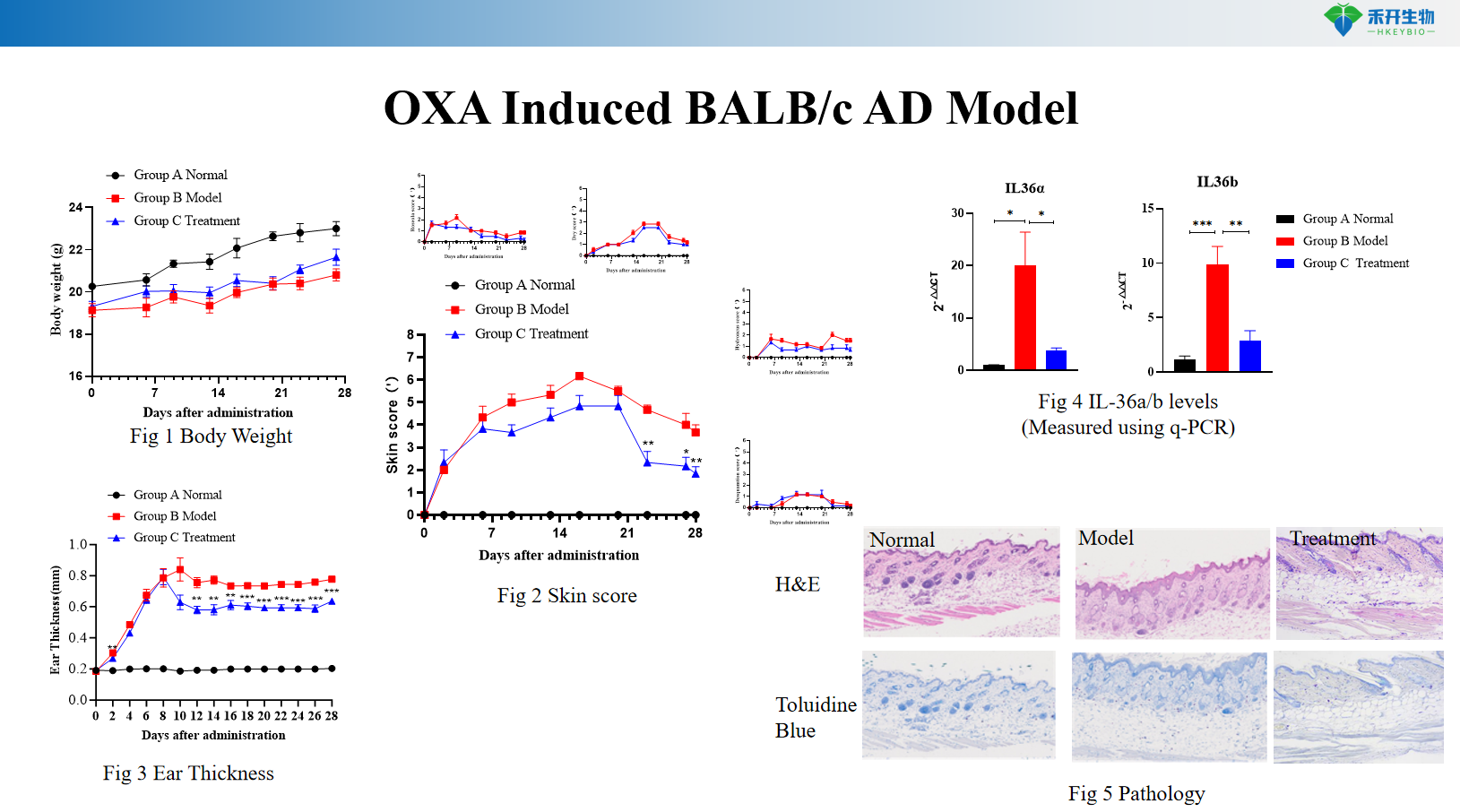
MC903 Modelo C57BL/6 AD inducido

Modelo BALB/c AD inducido MC903


Modelo de AD inducido por MC903 y OXA en BALB/c

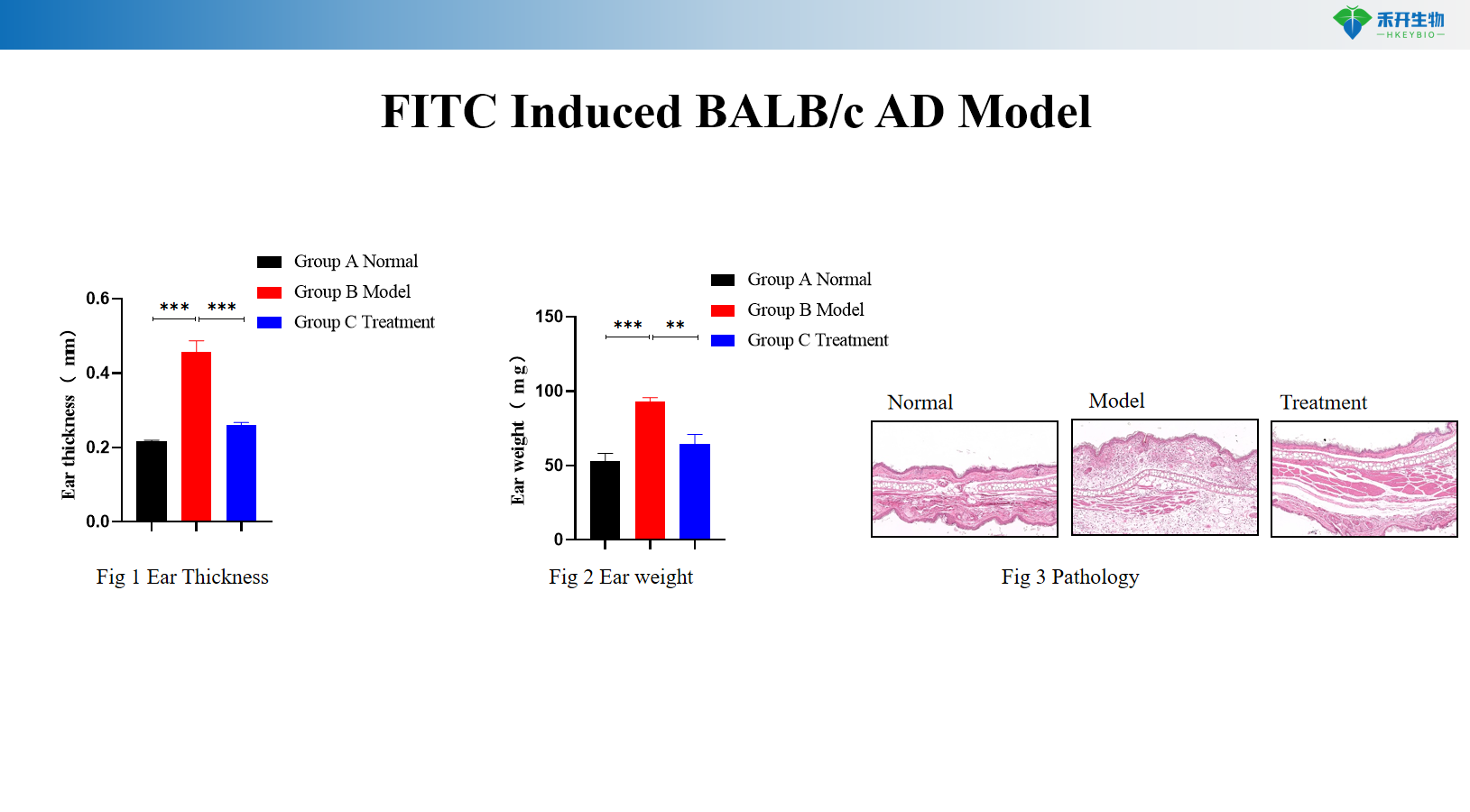
Modelo BALB/c AD inducido por FITC
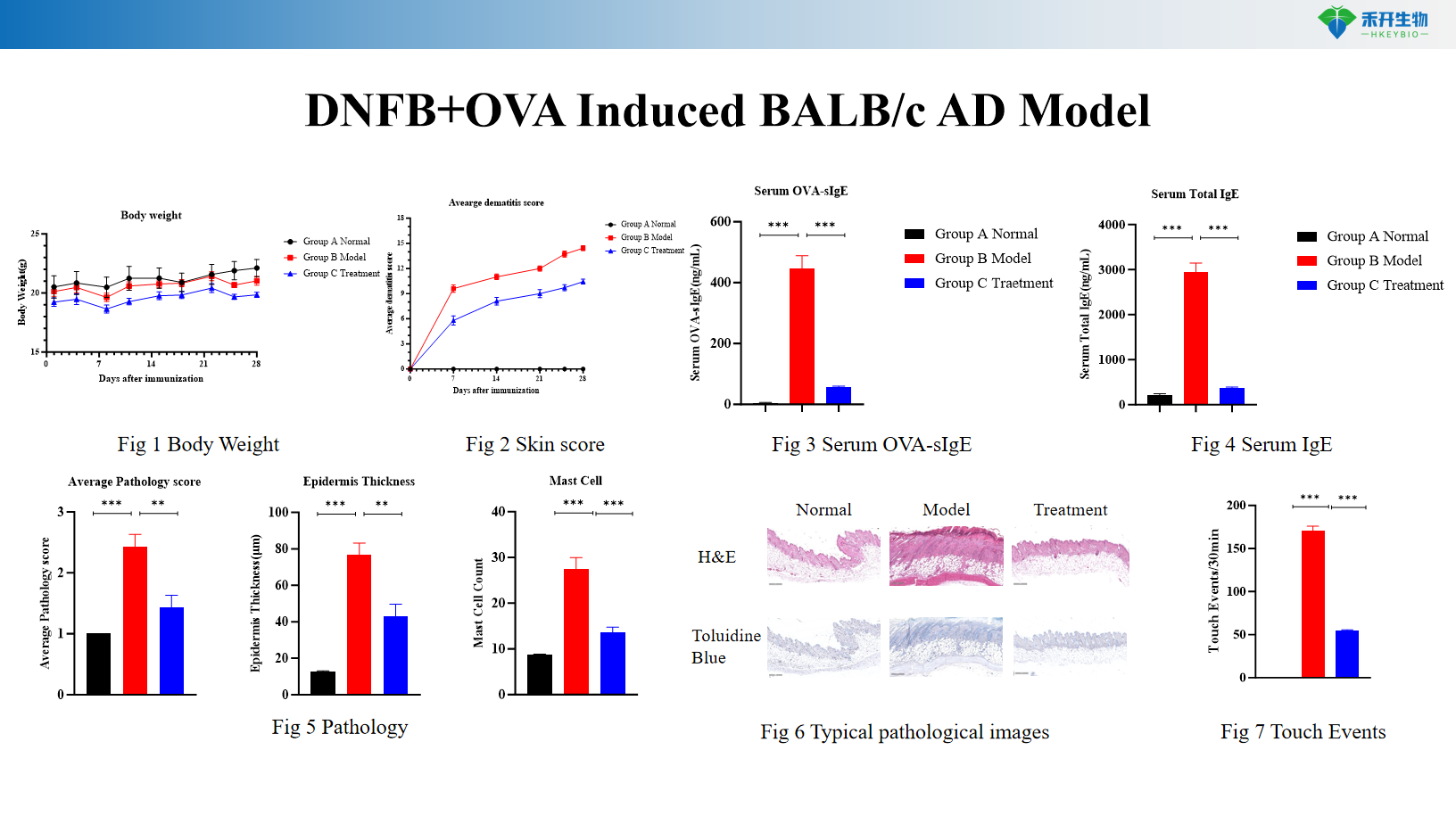
Modelo BALB/c AD inducido por DNFB+OVA
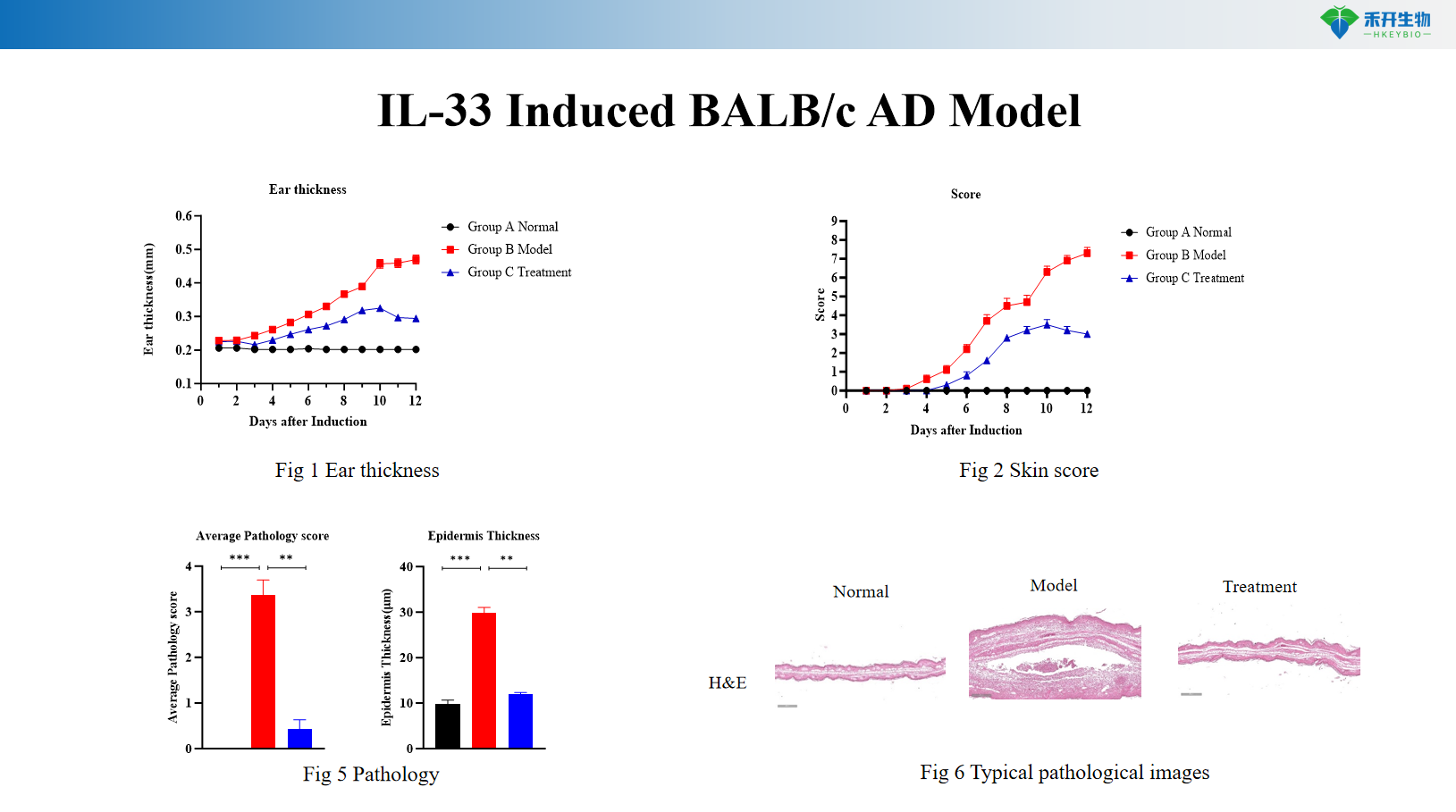
Modelo BALB/c AD inducido por IL-33
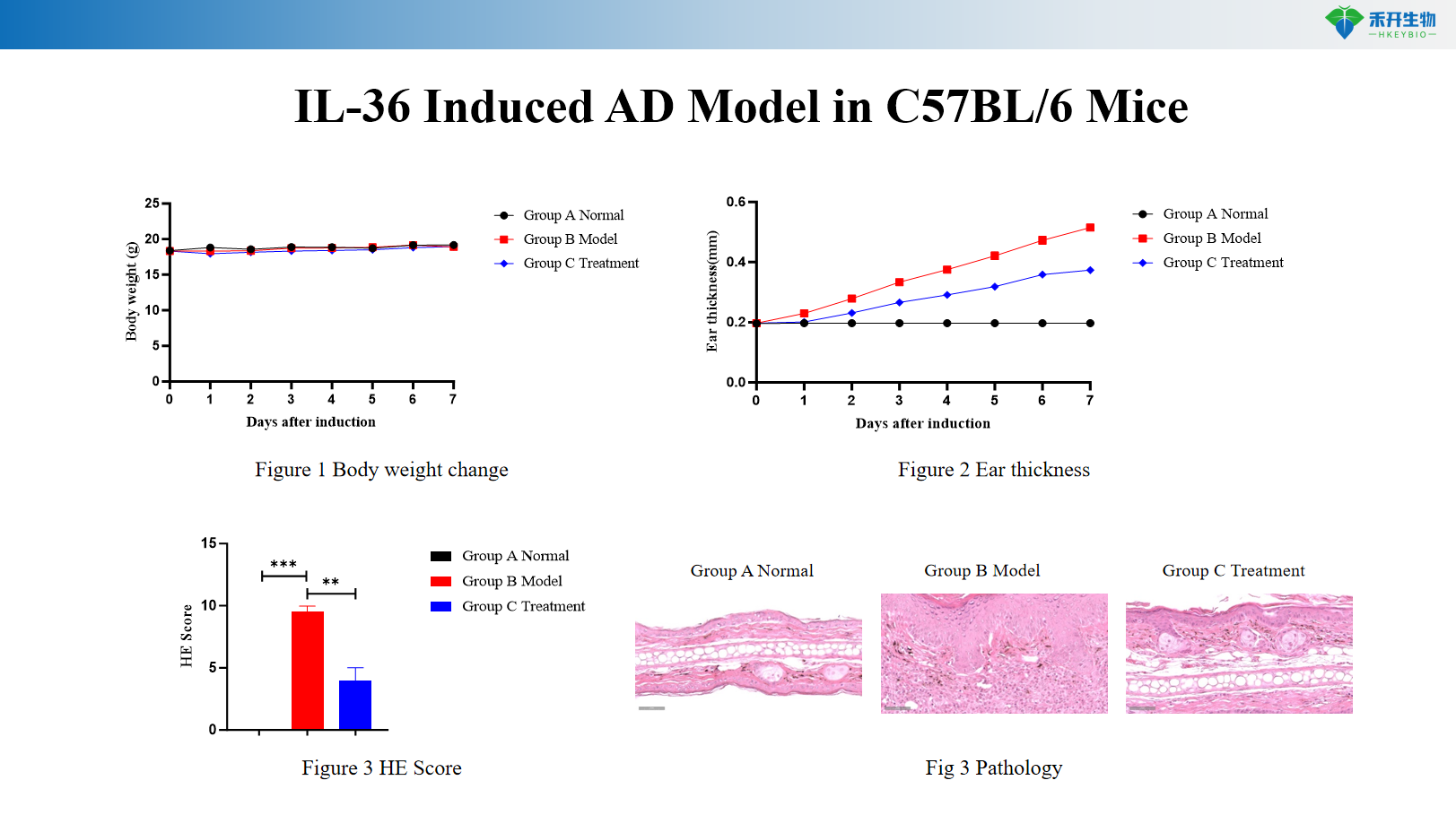
Modelo de AD inducido por IL-36 en ratones C57BL/6
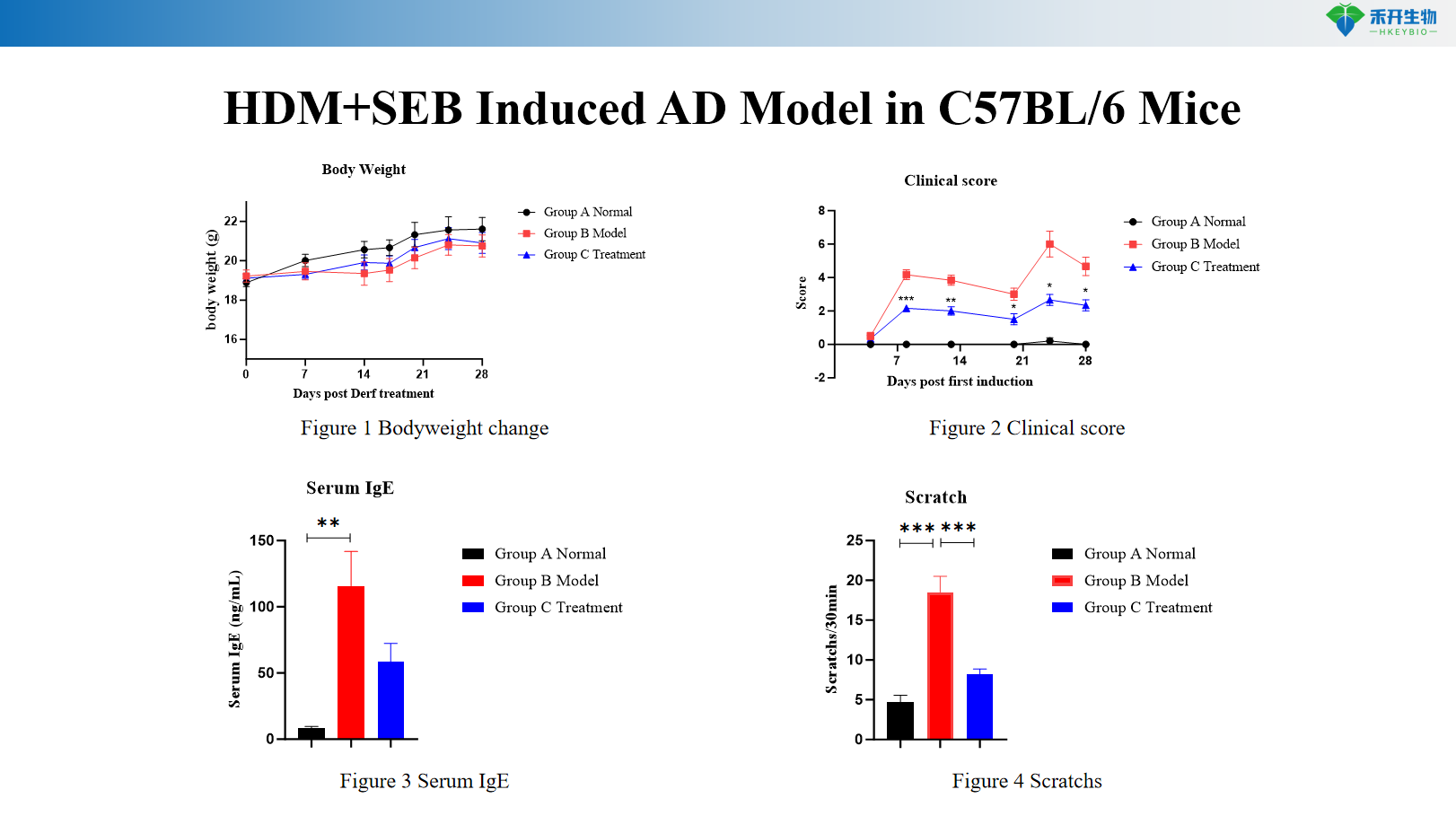
Modelo de AD inducido por HDM+SEB en ratones C57BL/6
• Pruebas de eficacia de terapias tópicas y sistémicas para la EA (inhibidores de JAK, inhibidores de PDE4, productos biológicos dirigidos a IL-4/13, IL-31, IL-33, TSLP)
• Validación de objetivos para Th2, Th17, Th22 y las vías de picazón.
• Descubrimiento de biomarcadores (IgE, firmas de citoquinas, proteínas de barrera cutánea)
• Estudios de mecanismo de acción (MOA)
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Especificaciones |
Especie/Cepa |
Ratón (BALB/c, C57BL/6); Rata (SD) |
Método de inducción |
Haptenos (DNCB, OXA, DNFB+OVA, FITC), análogo de vitamina D (MC903), citocinas (IL‑33, IL‑36), alérgenos (HDM+SEB), combinaciones (MC903+OXA) |
Duración del estudio |
7 a 28 días (según el modelo) |
Puntos finales clave |
Peso corporal, grosor de la oreja, puntuación clínica de la piel, episodios de picazón (rascado), IgE total sérica e IgE específica de antígeno, niveles de citoquinas (IL-4, IL-13, IL-17, IL-36, TNF-α), histopatología (H&E, azul de toluidina), espesor epidérmico, infiltración de células inmunitarias (FACS/IHC) |
Paquete de datos |
Datos brutos, informes de análisis, fotografías clínicas, portaobjetos de histología, archivos de citometría de flujo, bioinformática (opcional) |
P: ¿Cómo elijo el modelo de AD adecuado para mi medicamento candidato?
R: Considere el mecanismo de su fármaco: los productos biológicos dirigidos a Th2 (p. ej., anti-IL-4Rα) se evalúan mejor en modelos de hapteno o MC903; Los compuestos relacionados con Th17 pueden ser adecuados para los modelos IL-36 o HDM+SEB. Los ratones BALB/c exhiben respuestas Th2 más fuertes, mientras que C57BL/6 muestran perfiles Th1/Th17 más equilibrados. Nuestro equipo científico puede guiar la selección del modelo en función de su objetivo específico.
P: ¿Se pueden utilizar estos modelos para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes esquemas de dosificación, terapias combinadas)?
R: Absolutamente. Nuestro equipo científico adapta los protocolos de inducción, los programas de tratamiento y los análisis de criterios de valoración a su fármaco candidato específico.
P: ¿Cuál es el cronograma típico para un estudio piloto de eficacia?
R: La mayoría de los modelos de EA se completan en un plazo de 2 a 4 semanas, incluidas las fases de sensibilización/desafío y tratamiento. Los plazos específicos dependen de la elección del modelo y los criterios de valoración.
