| Disponibilidad: | |
|---|---|
| Cantidad: | |











Amplia cartera de modelos : modelos de alérgenos (OVA, HDM, Fel d 1), combinados con adyuvantes (LPS, c-di-GMP) y basados en TSLP (MC903) que cubren endotipos de asma granulocítica eosinófila, neutrofílica y mixta.
Múltiples cepas : ratones transgénicos C57BL/6, BALB/c, HIS humanizados y IL4/IL4R disponibles.
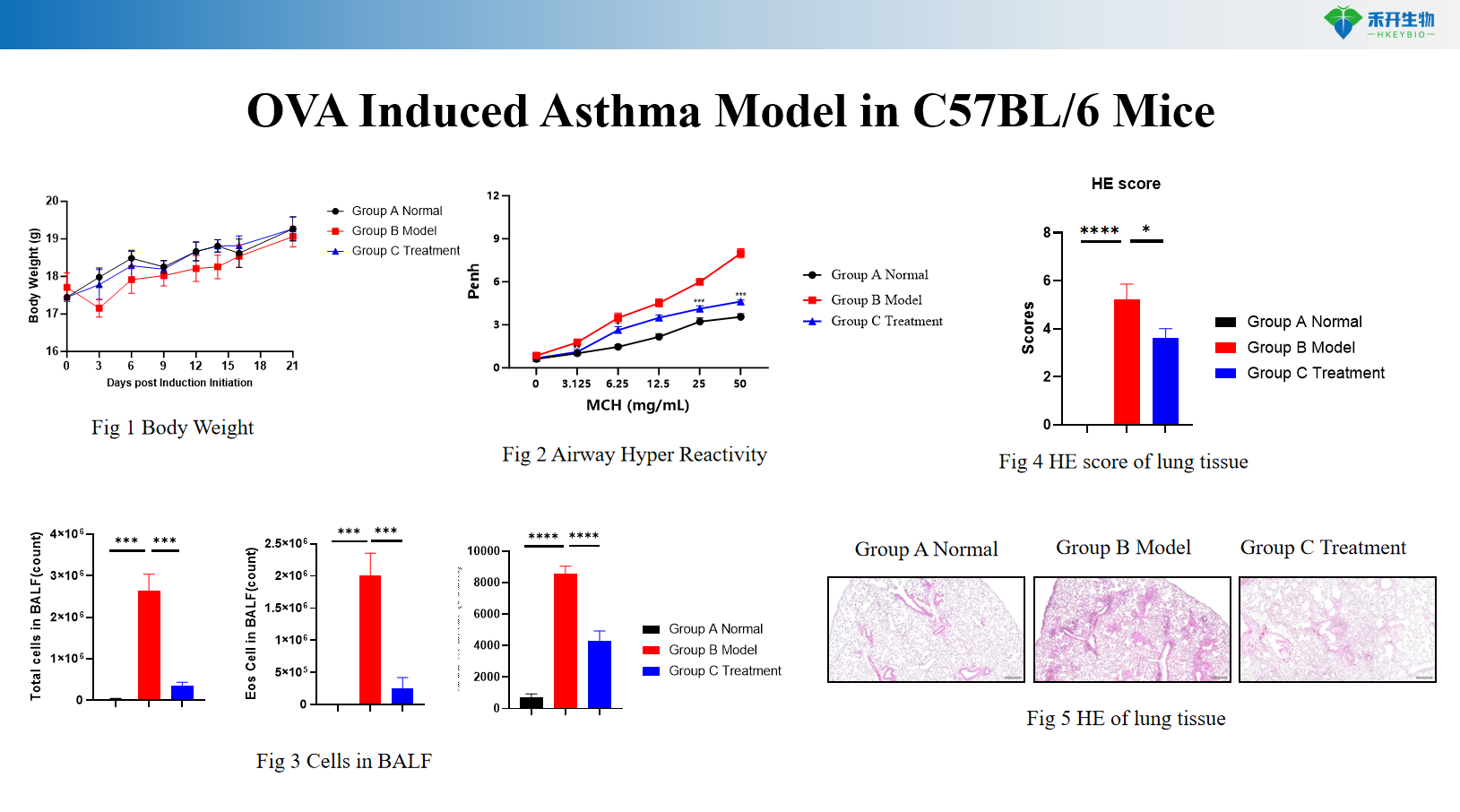
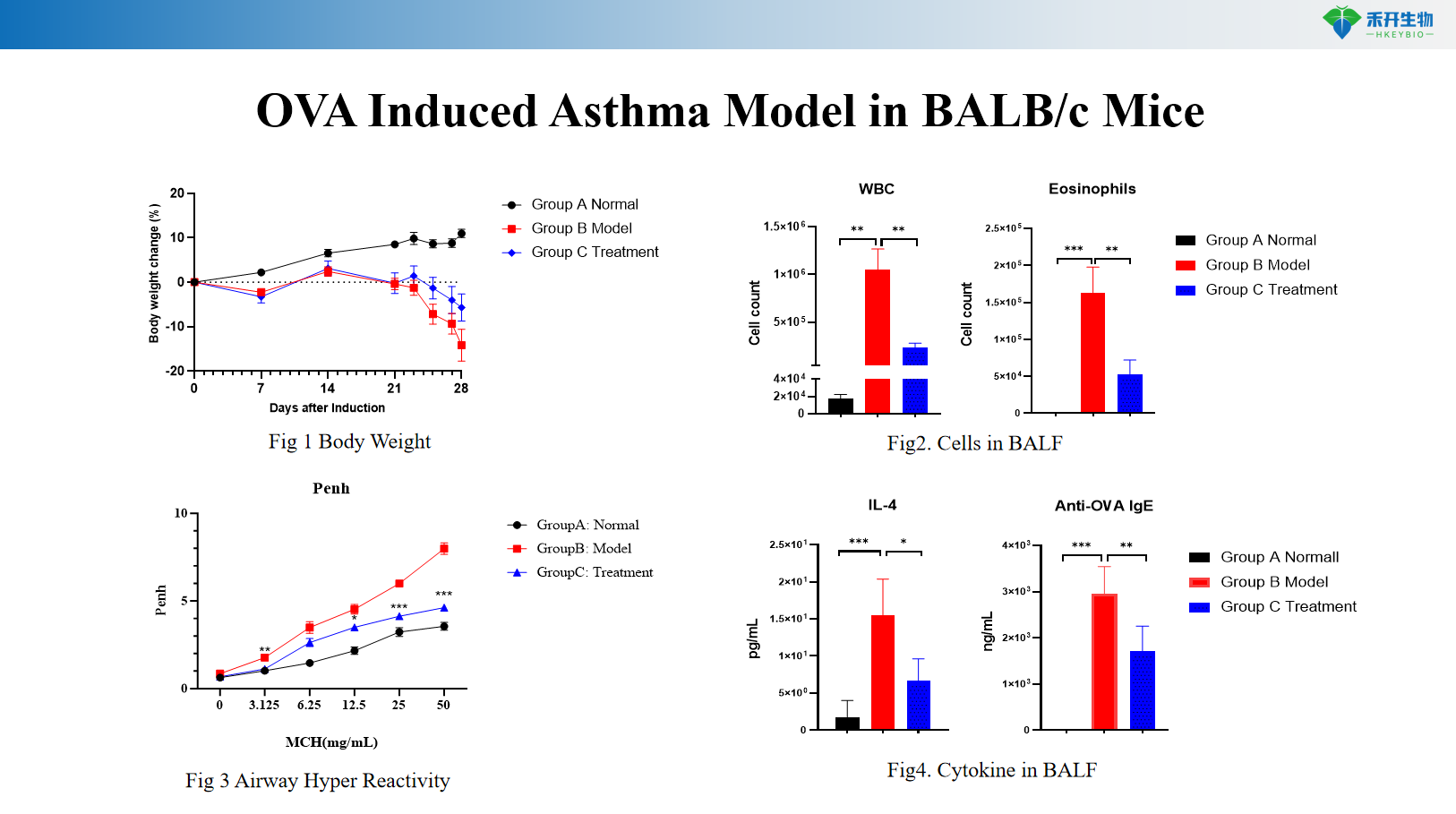
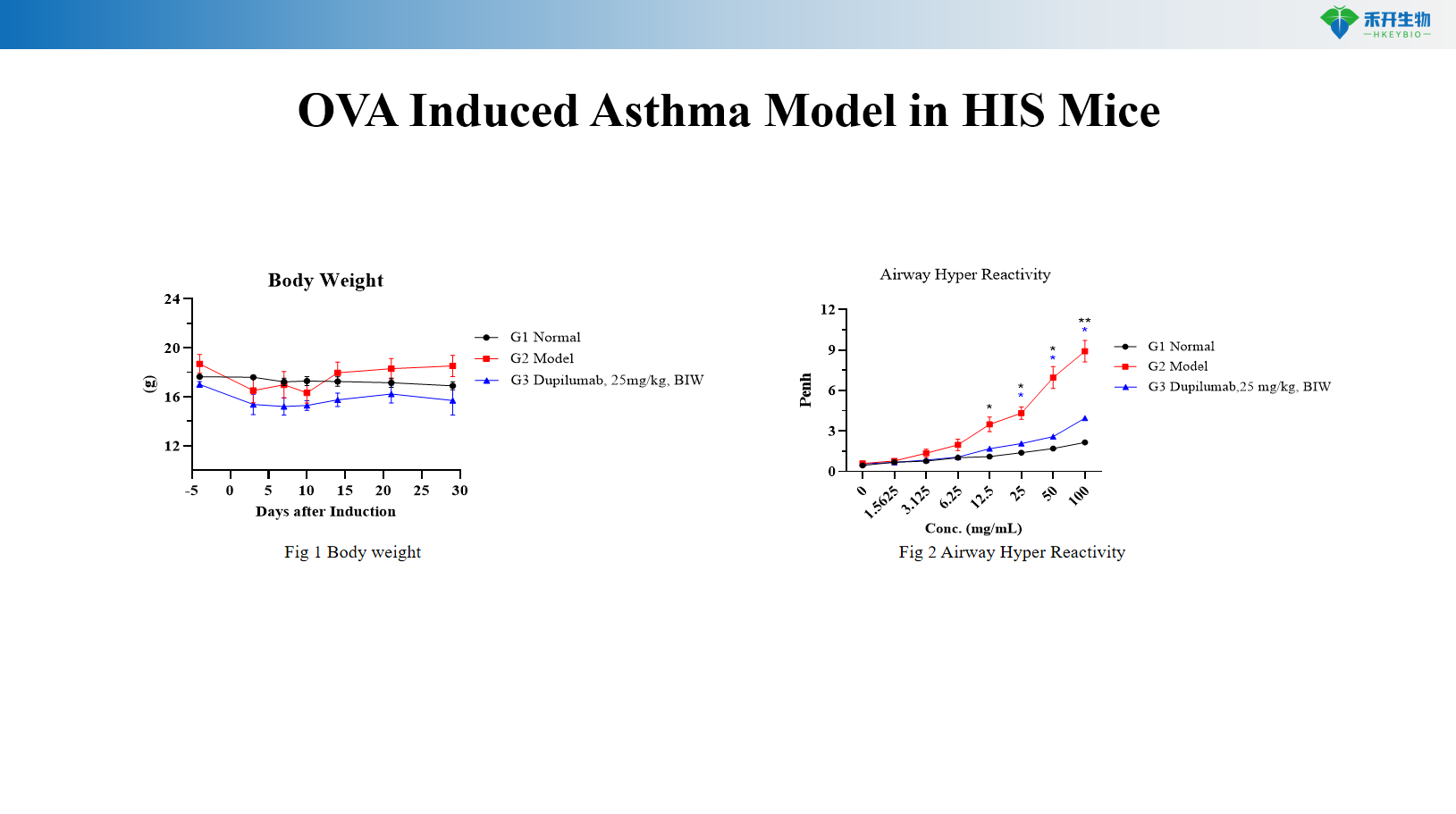
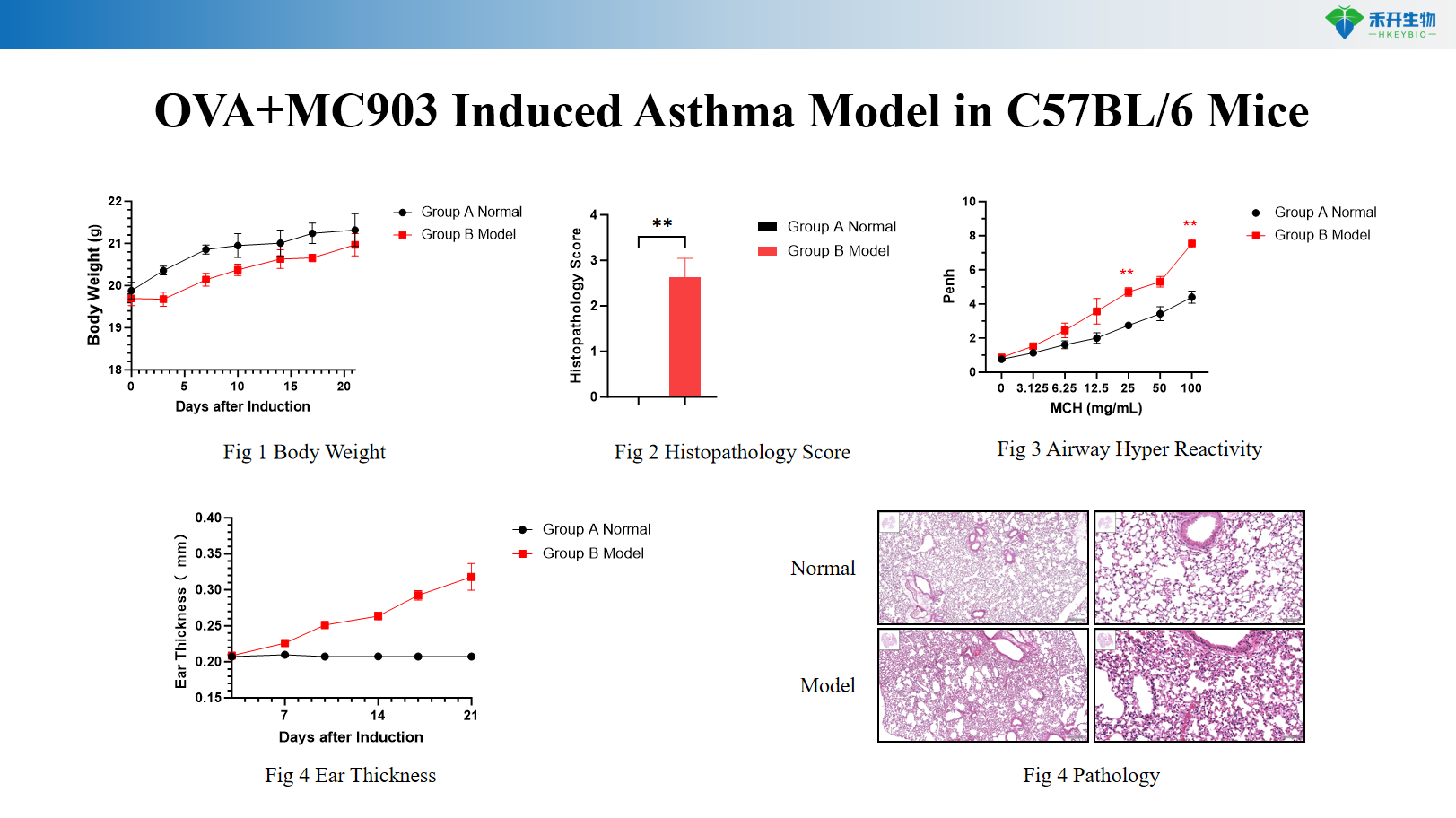
Criterios de valoración integrales : peso corporal, AHR (Penh, resistencia), recuentos de células BALF (eosinófilos, neutrófilos, macrófagos), IgE total en suero e IgE específica de alérgeno, perfil de citoquinas (IL-4, IL-5, IL-13, IL-17), histopatología pulmonar (HE, Masson, PAS), hematología.
Valor traslacional : ideal para probar productos biológicos (anti‑IL‑4Rα, anti‑IL‑5, anti‑IL‑13, anti‑TSLP, anti‑IL‑33), inhibidores de JAK, corticosteroides y broncodilatadores.
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
Modelo de asma inducida por OVA en ratones C57BL/6
Modelo de asma inducida por OVA en ratones BALB/c
Modelo de asma inducida por OVA en ratones HIS
Modelo de asma inducida OVA+MC903 en ratones C57BL/6
Modelo de asma neutrofílica inducida por OVA+LPS en ratones C57BL/6
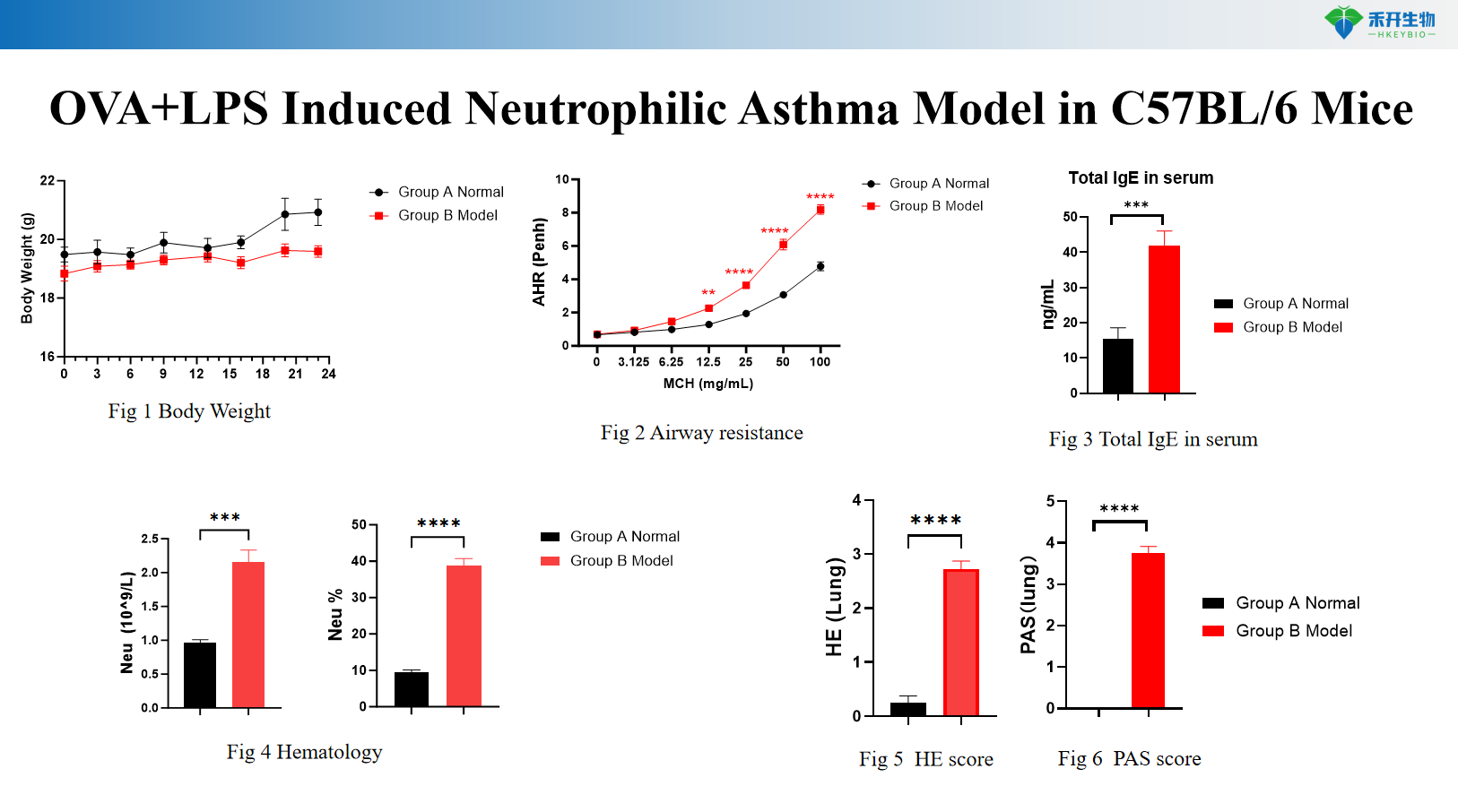
Modelo de asma inducida por HDM en ratones C57BL/6
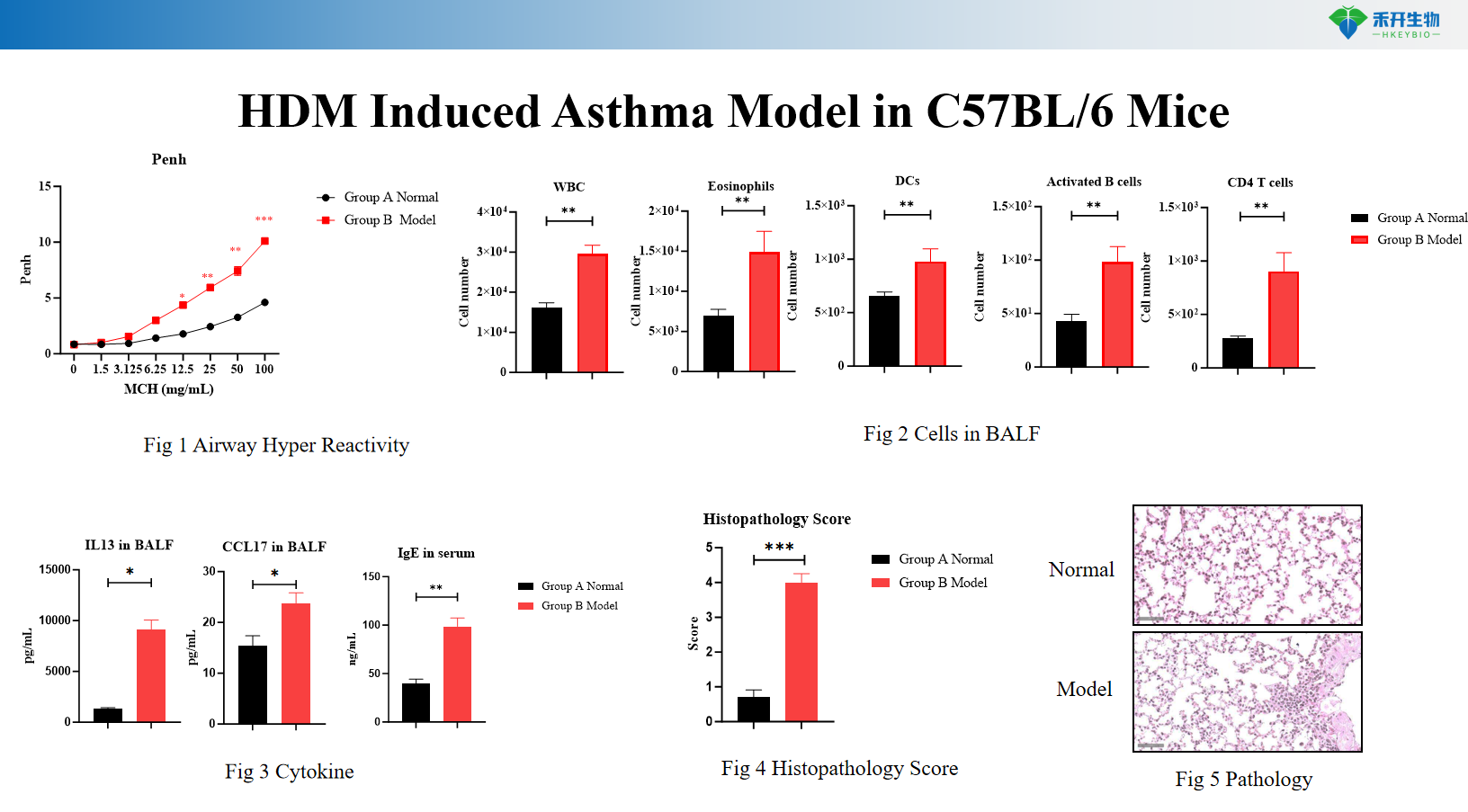
Modelo de asma inducida por HDM en ratones IL4/IL4R
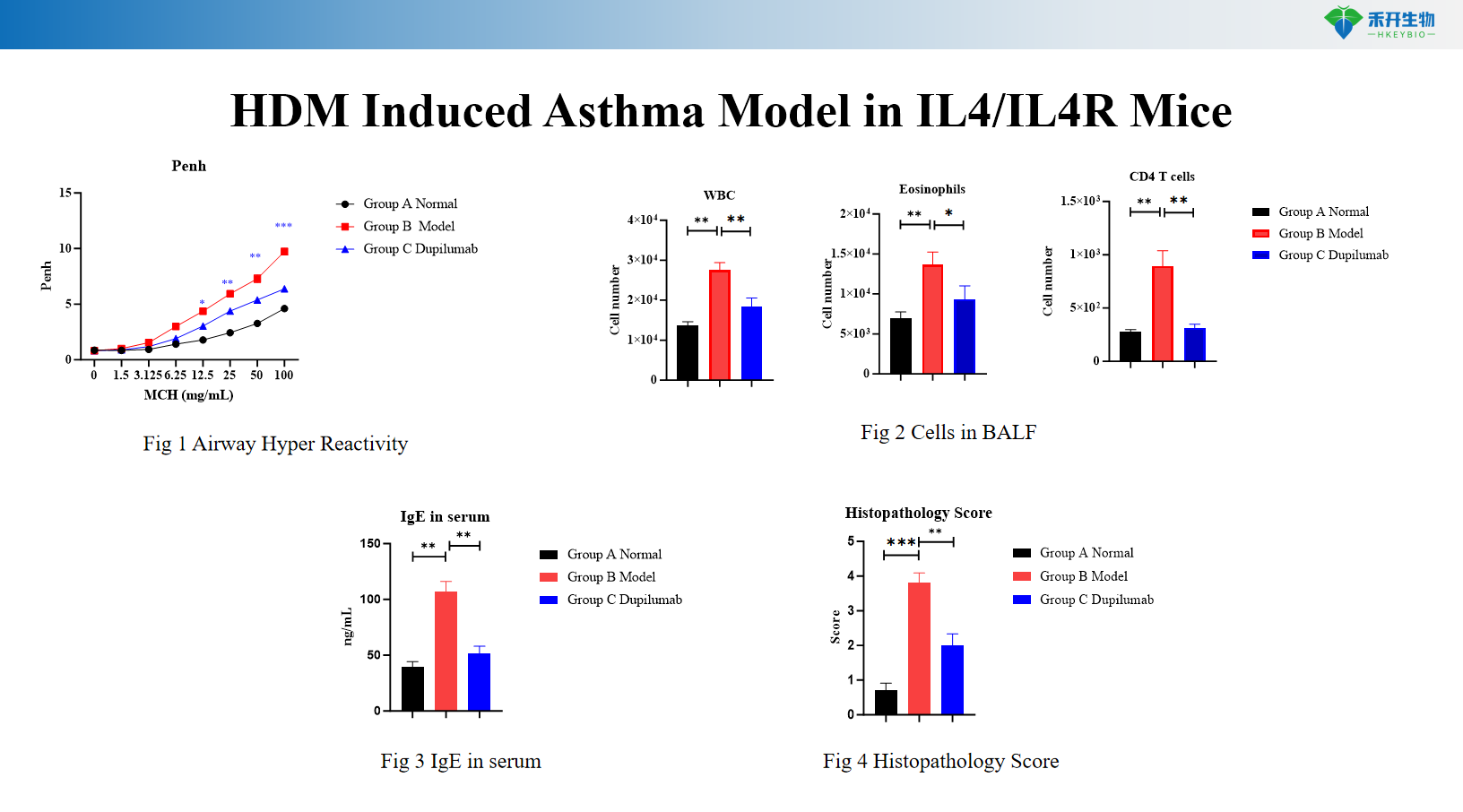
Modelo de asma inducida por HDM+LPS en ratones C57BL/6
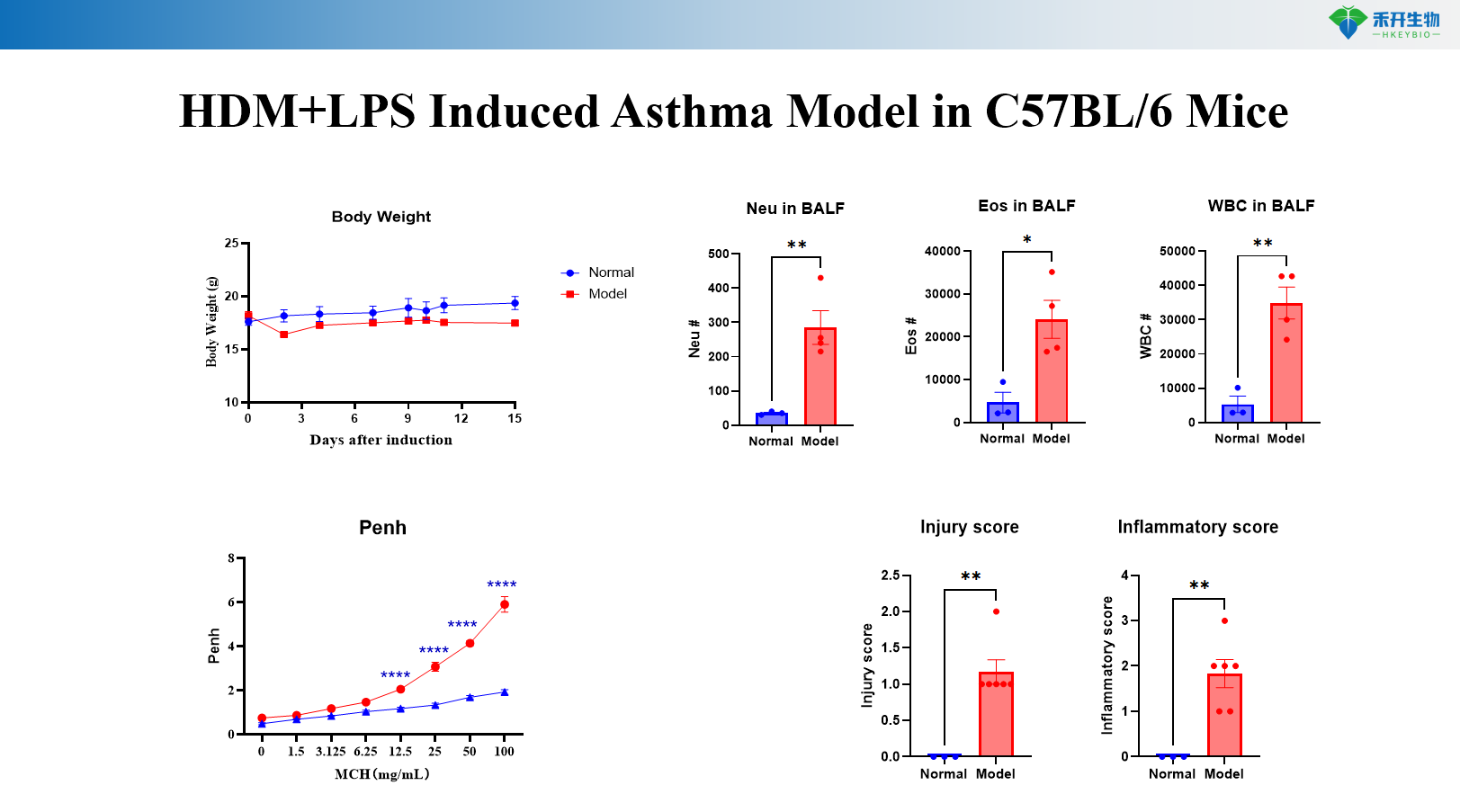
Modelo de asma inducida HDM+MC903 en ratones C57BL/6

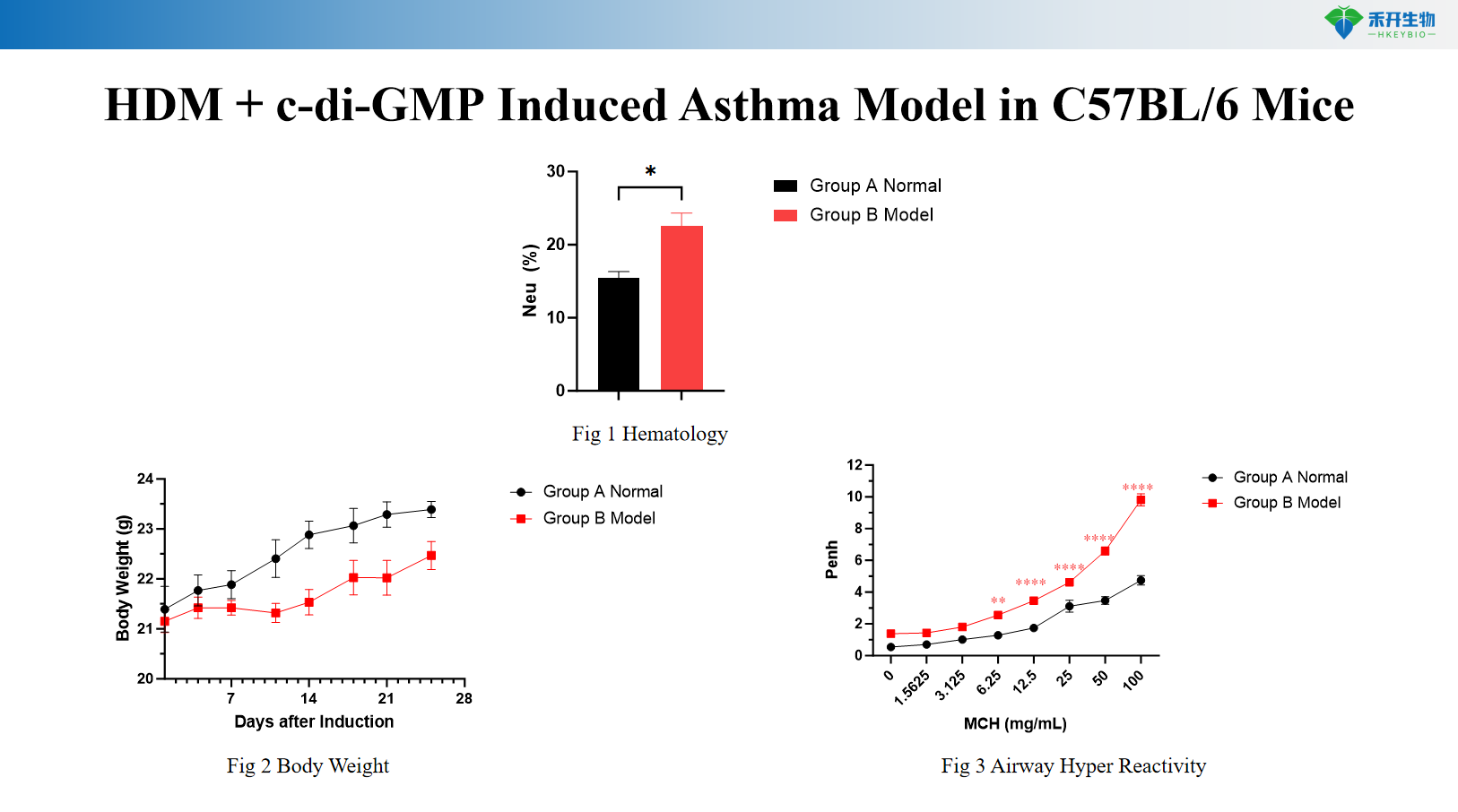
Modelo de asma inducida por HDM + c-di-GMP en ratones C57BL/6
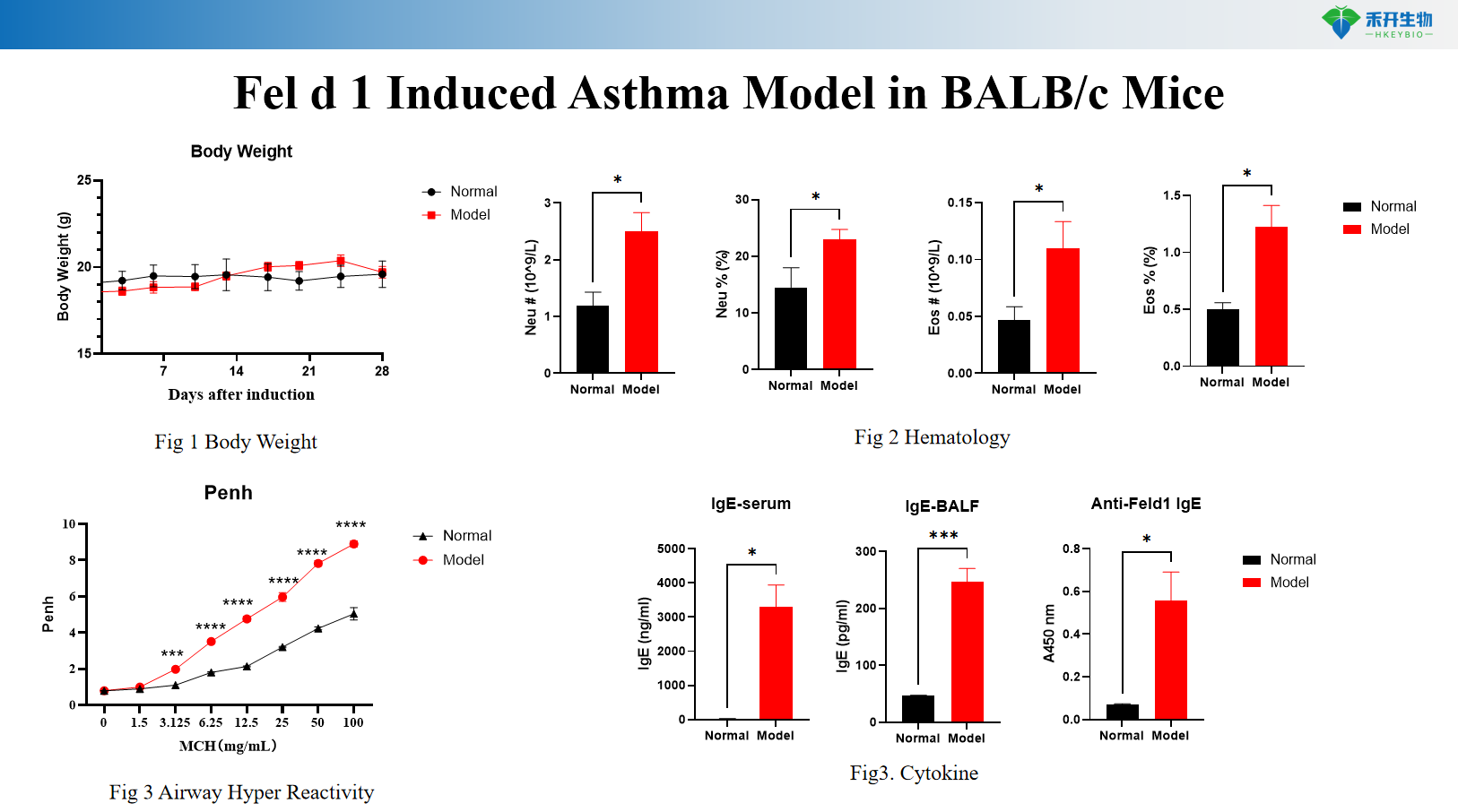
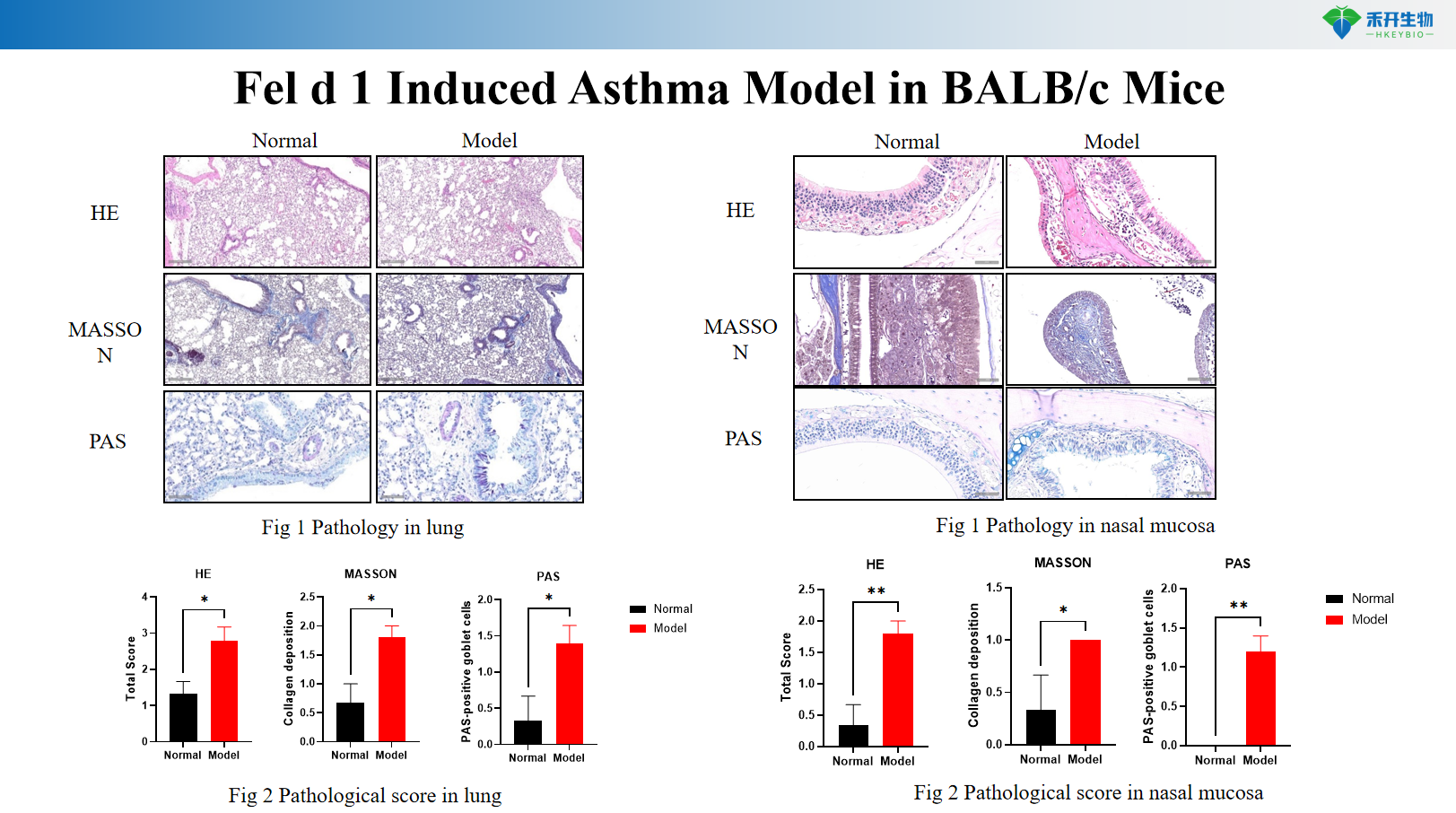
Modelo de asma inducida por Fel d 1 en ratones BALB/c
• Pruebas de eficacia de productos biológicos (anti-IL-4Rα, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33)
• Evaluación de inhibidores de moléculas pequeñas (inhibidores de JAK, inhibidores de PDE4, antagonistas de CRTH2)
• Validación de objetivos para Th2, Th17 y las vías de citocinas derivadas del epitelio.
• Descubrimiento de biomarcadores (IgE, firmas de citocinas, marcadores de eosinófilos/neutrófilos)
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Especificaciones |
Especie/Cepa |
C57BL/6, BALB/c, HIS humanizado, transgénico IL4/IL4R |
Método de inducción |
OVA ± alumbre ± MC903 ± LPS; HDM ± LPS ± MC903 ± c‑di‑GMP; Fel d 1 + alumbre |
Duración del estudio |
3 a 8 semanas (fases de sensibilización + desafío) |
Puntos finales clave |
Peso corporal, AHR (invasivo/no invasivo), citología BALF (eosinófilos, neutrófilos, macrófagos), IgE total sérica e IgE específica de alérgeno, niveles de citoquinas (IL-4, IL-5, IL-13, IL-17, IFN-γ), histopatología pulmonar (HE, Masson, PAS) con puntuación, hematología (opcional) |
| control positivo | Dexametasona o anticuerpo anti-IL-4Rα disponibles como compuestos de referencia |
Paquete de datos |
Datos sin procesar, informes de análisis, recuentos de células BALF, resultados de ELISA, portaobjetos de histología, datos de función pulmonar, bioinformática (opcional) |
P: ¿Cómo elijo el modelo de AD adecuado para mi medicamento candidato?
R: Para el asma eosinofílica (Th2-alta), se recomiendan los modelos OVA o HDM en BALB/c o C57BL/6. Para el asma neutrofílica o granulocítica mixta, los modelos OVA+LPS o HDM+c‑di‑GMP en C57BL/6 son apropiados. Los ratones humanizados HIS son ideales para probar productos biológicos específicos para humanos. Los ratones transgénicos IL4/IL4R son adecuados para estudios de la vía Th2. Nuestro equipo científico puede guiar la selección del modelo en función de su objetivo específico.
P: ¿Cuál es la diferencia entre los modelos inducidos por OVA y HDM?
R: OVA es un alérgeno modelo que requiere adyuvante para la sensibilización, lo que produce respuestas Th2 sólidas. HDM es un alérgeno humano clínicamente relevante que contiene proteasas que activan la inmunidad tanto innata como adaptativa, imitando más fielmente la patogénesis del asma alérgica humana.
P: ¿Se pueden utilizar estos modelos para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes programas de sensibilización/desafío, terapias combinadas)?
R: Absolutamente. Nuestro equipo científico adapta los protocolos de inducción, los programas de tratamiento y los análisis de criterios de valoración a su fármaco candidato específico.
P: ¿Cuál es el cronograma típico para un estudio piloto de eficacia?
R: La mayoría de los modelos de asma se completan en un plazo de 4 a 6 semanas, incluida la sensibilización, la provocación, el tratamiento y el análisis de criterios de valoración.
