| Disponibilità: | |
|---|---|
| Quantità: | |











Clinicamente rilevante – Riepiloga l’ipersensibilità umana di tipo I con attivazione dei mastociti mediata da IgE, vasodilatazione e prurito.
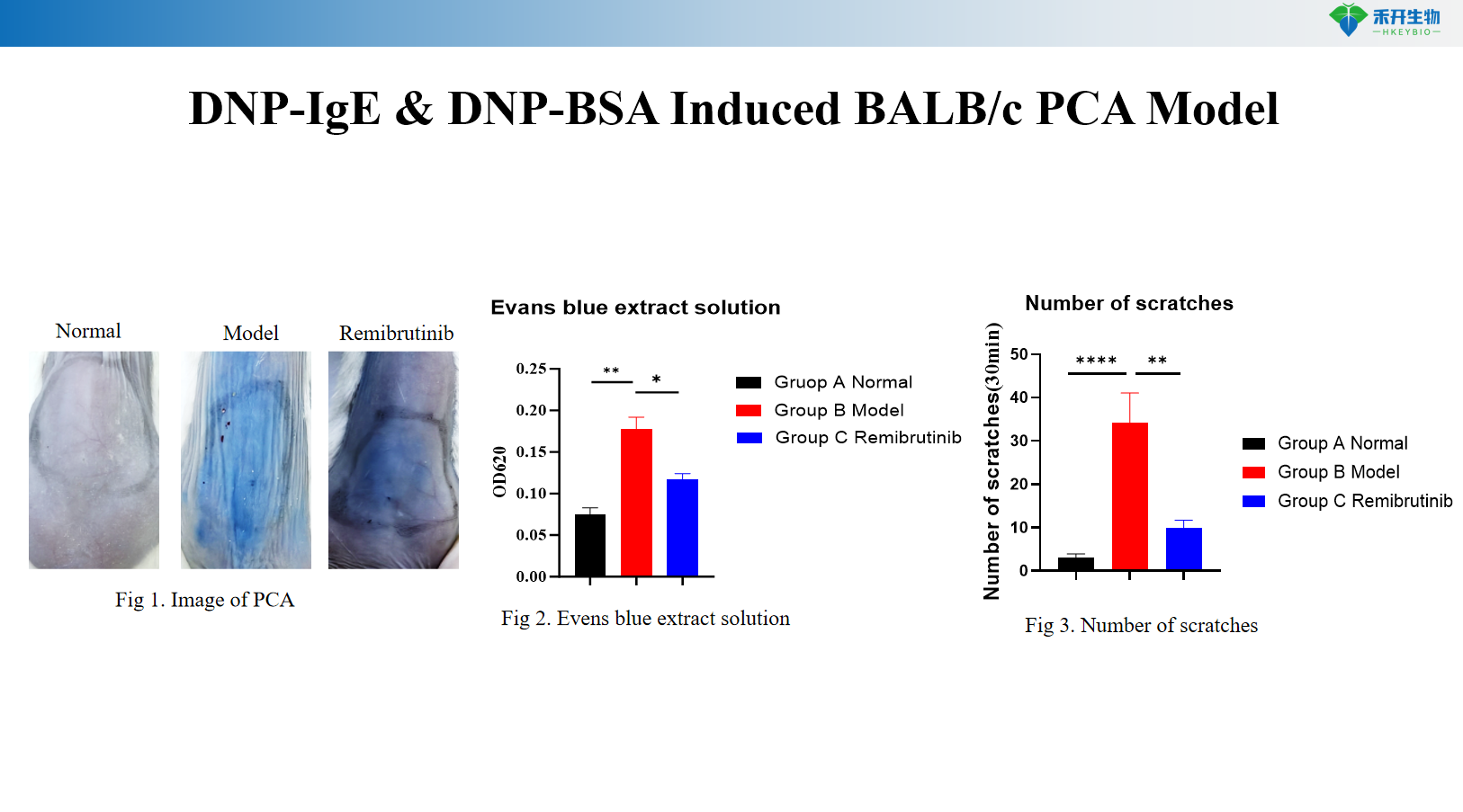
Endpoint quantificabili – Stravaso blu di Evans (diametro del punto blu o misurazione della OD), conteggio del comportamento di grattamento, spessore dell'orecchio, livelli sierici di IgE.
Due opzioni di specie : modelli di topo (BALB/c) e ratto (Wistar) disponibili per soddisfare le diverse esigenze sperimentali.
Valore traslazionale – Ideale per testare farmaci biologici anti-IgE (omalizumab), stabilizzatori dei mastociti (cromolina), antistaminici H1 e altri agenti antiallergici.
Pacchetti dati pronti per IND – Gli studi possono essere condotti in conformità con i principi GLP.
Modello PCA BALB/c indotto da DNP-IgE e DNP-BSA
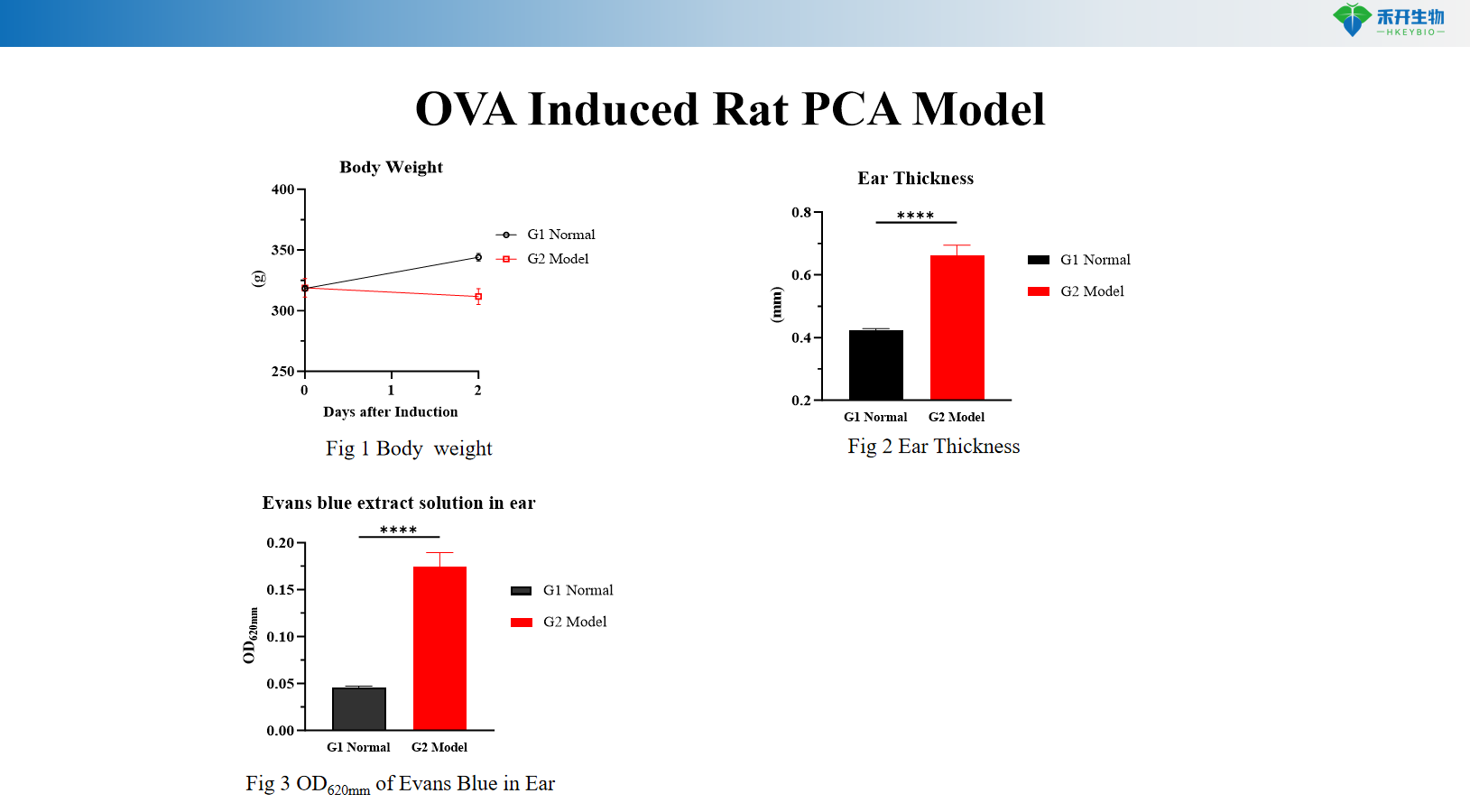
Modello PCA di ratto indotto da OVA
• Test di efficacia di farmaci biologici anti-IgE (omalizumab, ligelizumab) e stabilizzatori dei mastociti (cromolina, ketotifene)
• Valutazione degli antistaminici H1 (cetirizina, fexofenadina) e di altri agenti antiallergici
• Convalida del target per la via IgE/FcεRI e la biologia dei mastociti
• Scoperta di biomarcatori (IgE, istamina, mediatori dei mastociti)
• Studi farmacologici e tossicologici che consentono l'IND
Parametro |
Modello PCA del mouse |
Modello PCA del ratto |
Specie/ceppo |
Mouse BALB/c |
Ratto Wistar |
Metodo di induzione |
Iniezione intradermica di DNP-IgE (sensibilizzazione passiva) + iv DNP-BSA con Evans blue | Iniezione intradermica di siero sensibilizzato OVA + iv OVA con Evans blue |
Durata dello studio |
24–48 ore (sensibilizzazione + sfida) | 24–72 ore |
Endpoint chiave |
Conteggio dello stravaso blu di Evans (diametro della macchia blu o OD), comportamento di grattamento |
Peso corporeo, spessore dell'orecchio, stravaso di blu di Evans (OD 620 nm), IgE sieriche specifiche per OVA, istopatologia cutanea (blu di toluidina) |
| Controllo positivo | Anticorpo anti-IgE o antistaminico (ad esempio cetirizina) disponibili come composti di riferimento | |
Pacchetto dati |
Dati grezzi, rapporti di analisi, fotografie cliniche, risultati ELISA, vetrini istologici, bioinformatica (opzionale) | |
D: Quali sono le differenze tra i modelli PCA del topo e del ratto?
R: Il modello murino utilizza DNP-IgE per la sensibilizzazione passiva e DNP-BSA per il challenge, ideale per studiare le reazioni pure mediate da IgE. Il modello di ratto utilizza il siero di donatori sensibilizzati agli OVA, fornendo una risposta anticorpale policlonale più complessa e consentendo la valutazione dello spessore dell'orecchio e del comportamento di grattamento.
D: Come viene quantificata la reazione allergica nei modelli PCA?
R: Il colorante blu Evans viene iniettato per via endovenosa con l'antigene. L'aumento della permeabilità vascolare provoca uno stravaso di colorante nel sito sensibilizzato, formando una macchia blu. La reazione viene quantificata misurando il diametro del punto blu, asportando la pelle per l'estrazione del colorante e la misurazione della densità ottica o valutando lo spessore dell'orecchio (modello di ratto).
D: Questi modelli possono essere utilizzati per studi abilitanti all’IND?
R: Sì. Gli studi possono essere condotti in conformità con i principi GLP per le richieste normative (FDA, EMA).
D: Offrite protocolli di studio personalizzati (ad esempio, diversi allergeni, concentrazioni di anticorpi)?
R: Assolutamente. Il nostro team scientifico adatta protocolli di sensibilizzazione, programmi di sfida e analisi degli endpoint al tuo specifico farmaco candidato.
D: Qual è la tempistica tipica per uno studio pilota sull'efficacia?
R: Entrambi i modelli sono acuti, con studi generalmente completati entro 24-72 ore dalla sensibilizzazione passiva e dal test antigenico.
