| Saatavuus: | |
|---|---|
| Määrä: | |











Kliinisesti merkityksellinen – Toistaa ihmisen tyypin I yliherkkyyden IgE-välitteisellä syöttösoluaktivaatiolla, vasodilataatiolla ja kutinalla.
Mitattavissa olevat päätepisteet – Evansin sinisen ekstravasaatio (sinisen täplän halkaisija tai OD-mittaus), naarmuuntumiskäyttäytymisen määrä, korvan paksuus, seerumin IgE-tasot.
Kaksi lajivaihtoehtoa – Hiiri (BALB/c) ja rotta (Wistar) -mallit saatavilla erilaisiin kokeellisiin tarpeisiin.
Käännösarvo – Ihanteellinen anti-IgE-biologisten aineiden (omalitsumabi), syöttösolujen stabilointiaineiden (kromolynin), H1-antihistamiinien ja muiden antiallergisten aineiden testaamiseen.
IND-valmiit tietopaketit – Tutkimukset voidaan suorittaa GLP-periaatteiden mukaisesti.
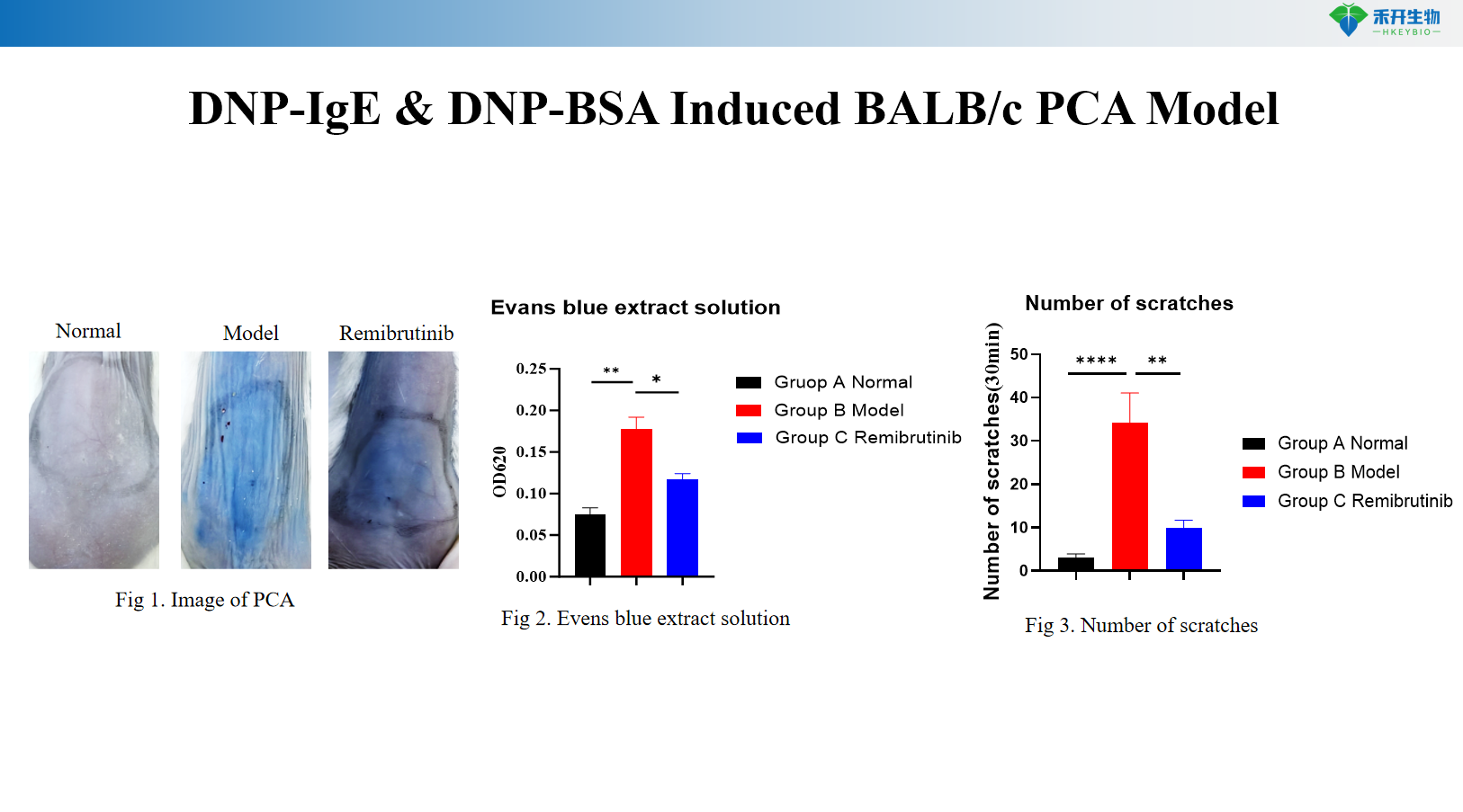
DNP-IgE- ja DNP-BSA-indusoitu BALB/c PCA -malli
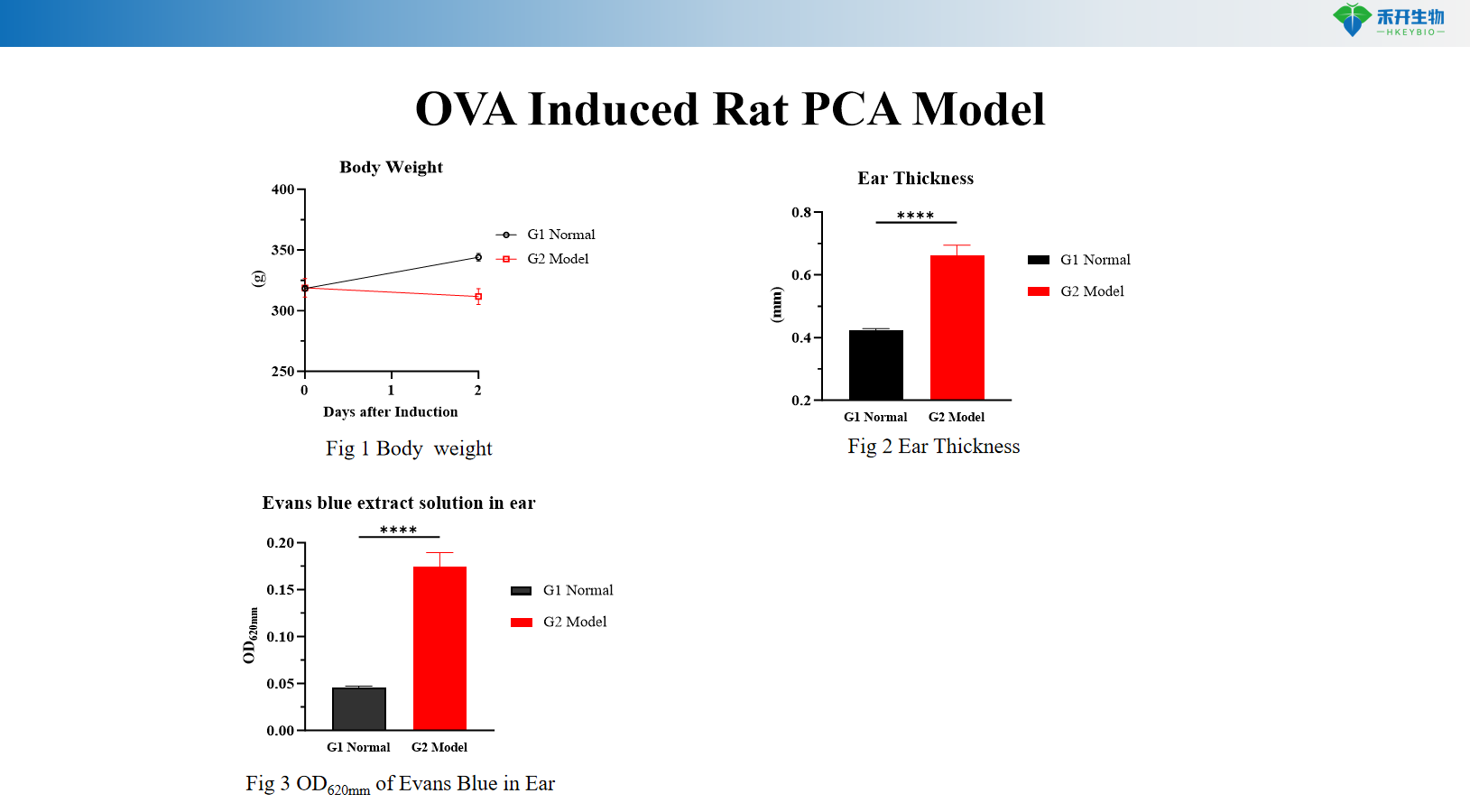
OVA-indusoitu rotan PCA-malli
• Anti-IgE-biologisten aineiden (omalitsumabi, ligelitsumabi) ja syöttösolujen stabilointiaineiden (kromolyni, ketotifeeni) tehokkuuden testaus
• H1-antihistamiinien (setiritsiini, feksofenadiini) ja muiden allergiaa ehkäisevien aineiden arviointi
• IgE/FcεRI-reitin ja syöttösolubiologian kohdevalidointi
• Biomarkkerien löytäminen (IgE, histamiini, syöttösoluvälittäjät)
• IND:n mahdollistavat farmakologiset ja toksikologiset tutkimukset
Parametri |
Hiiren PCA malli |
Rotan PCA malli |
Laji/kanta |
BALB/c hiiri |
Wistar rotta |
Induktiomenetelmä |
DNP-IgE:n intradermaalinen injektio (passiivinen herkistys) + iv DNP-BSA Evansin sinisellä | OVA-herkistetyn seerumin intradermaalinen injektio + iv OVA Evansin sinisellä |
Opintojen kesto |
24-48 tuntia (herkistys + haaste) | 24-72 tuntia |
Tärkeimmät päätepisteet |
Evansin sinisen ekstravasaatio (sinisen pisteen halkaisija tai OD), naarmuuntumiskäyttäytymislaskenta |
Paino, korvan paksuus, Evansin sinisen ekstravasaatio (OD 620 nm), seerumin OVA-spesifinen IgE, ihon histopatologia (toluidiinisininen) |
| Positiivinen ohjaus | Anti-IgE-vasta-aine tai antihistamiini (esim. setiritsiini) saatavilla vertailuyhdisteinä | |
Datapaketti |
Raakadata, analyysiraportit, kliiniset valokuvat, ELISA-tulokset, histologiset objektilasit, bioinformatiikka (valinnainen) | |
K: Mitä eroja on hiiren ja rotan PCA-mallien välillä?
V: Hiirimalli käyttää DNP-IgE:tä passiiviseen herkistymiseen ja DNP-BSA:ta haasteeseen, mikä on ihanteellinen puhtaiden IgE-välitteisten reaktioiden tutkimiseen. Rottamallissa käytetään OVA-herkistettyjen luovuttajien seerumia, mikä tarjoaa monimutkaisemman polyklonaalisen vasta-ainevasteen ja mahdollistaa korvan paksuuden ja naarmuuntumiskäyttäytymisen arvioinnin.
K: Miten allerginen reaktio mitataan PCA-malleissa?
V: Evansin sinistä väriainetta ruiskutetaan suonensisäisesti antigeenin kanssa. Lisääntynyt verisuonten läpäisevyys aiheuttaa väriaineen ekstravasaatiota herkistyneeseen kohtaan, jolloin muodostuu sininen täplä. Reaktio kvantifioidaan mittaamalla sinisen täplän halkaisija, leikkaamalla iho värin uuttamista ja OD-mittausta varten tai arvioimalla korvan paksuus (rottamalli).
K: Voidaanko näitä malleja käyttää IND:n mahdollistaviin tutkimuksiin?
V: Kyllä. Tutkimukset voidaan suorittaa GLP-periaatteiden mukaisesti viranomaisilmoituksia varten (FDA, EMA).
K: Tarjoatko räätälöityjä tutkimusprotokollia (esim. erilaiset allergeenit, vasta-ainepitoisuudet)?
V: Ehdottomasti. Tieteellinen tiimimme räätälöi herkistysprotokollat, haasteaikataulut ja päätepisteanalyysit sinun lääkekandidaatillesi.
K: Mikä on tyypillinen aikajana pilottitehokkuustutkimukselle?
V: Molemmat mallit ovat akuutteja, ja tutkimukset valmistuvat tyypillisesti 24–72 tunnin kuluessa passiivisen herkistymisen ja antigeenialtistuksen jälkeen.
