| Tillgänglighet: | |
|---|---|
| Kvantitet: | |











Kliniskt relevant – Rekapitulerar human typ I-överkänslighet med IgE-medierad mastcellsaktivering, vasodilatation och klåda.
Kvantifierbara endpoints – Evans blå extravasation (blåfläcksdiameter eller OD-mätning), antal repbeteende, örontjocklek, serum-IgE-nivåer.
Två artalternativ – Mus (BALB/c) och råtta (Wistar) modeller tillgängliga för att passa olika experimentella behov.
Translationsvärde – Idealiskt för att testa biologiska anti-IgE (omalizumab), mastcellsstabilisatorer (cromolyn), H1-antihistaminer och andra antiallergiska medel.
IND-färdiga datapaket – Studier kan utföras i enlighet med GLP-principer.
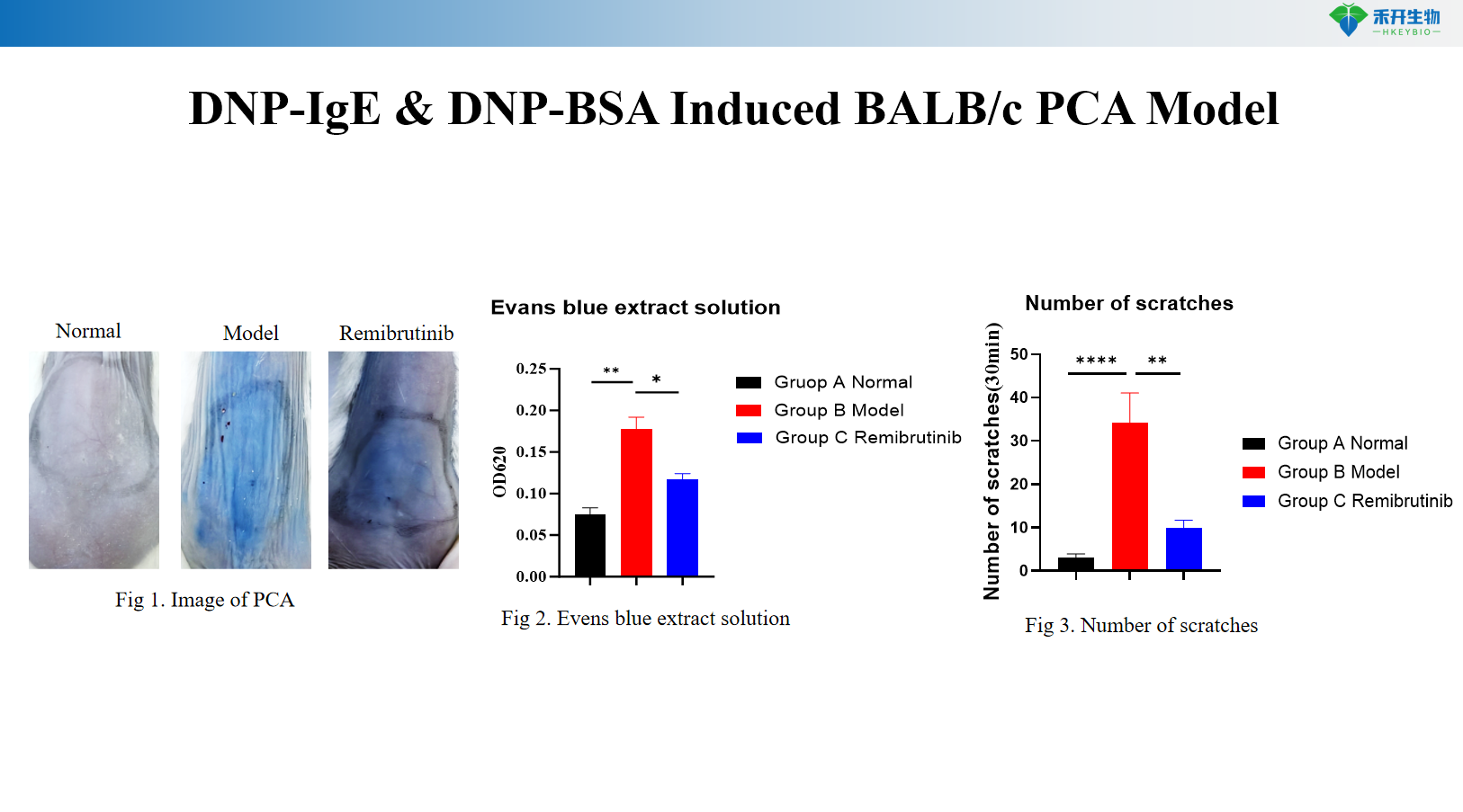
DNP-IgE & DNP-BSA-inducerad BALB/c PCA-modell
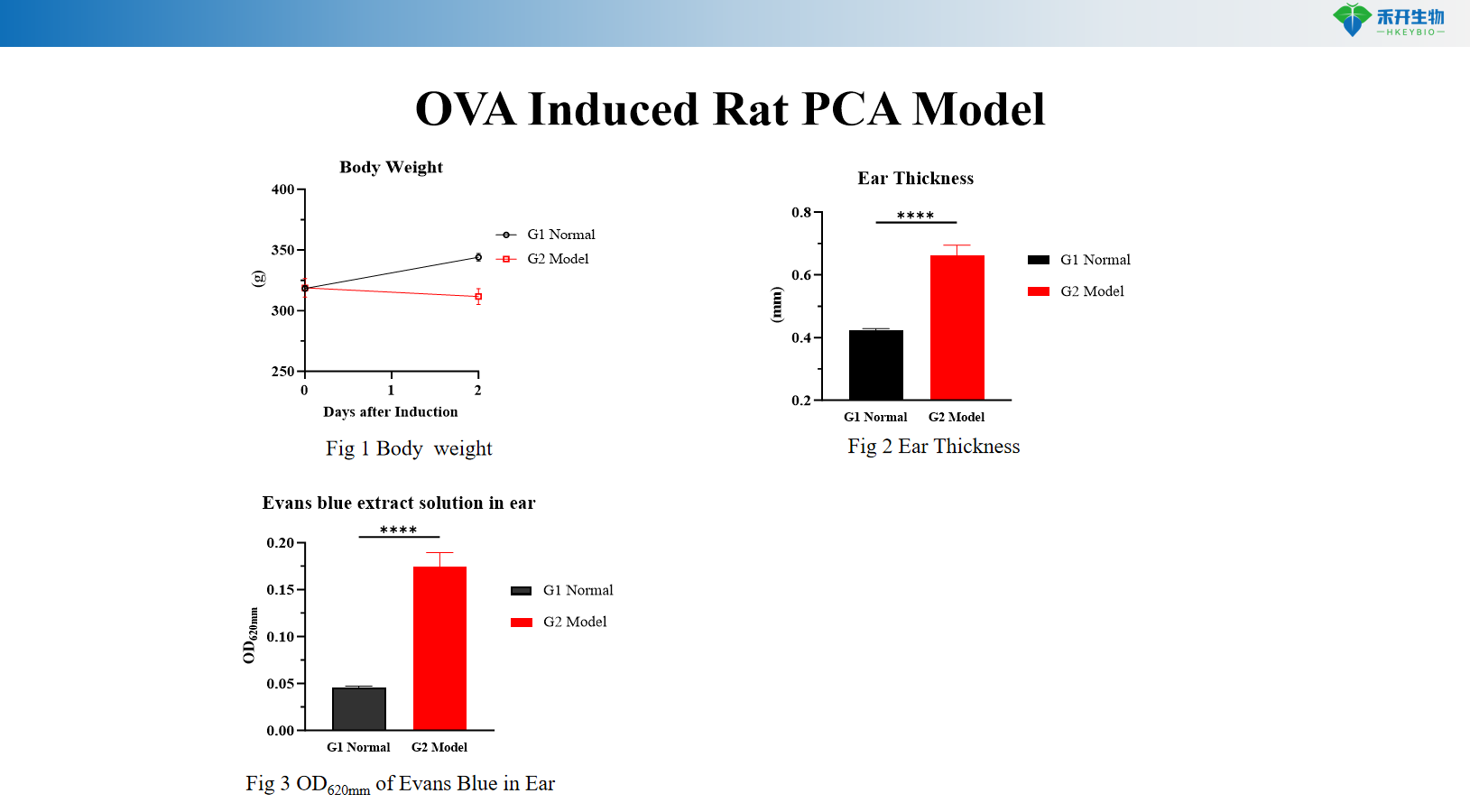
OVA-inducerad PCA-modell för råtta
• Effekttester av anti-IgE biologiska läkemedel (omalizumab, ligelizumab) och mastcellsstabilisatorer (kromolyn, ketotifen)
• Utvärdering av H1-antihistaminer (cetirizin, fexofenadin) och andra antiallergiska medel
• Målvalidering för IgE/FcεRI-väg och mastcellbiologi
• Upptäckt av biomarkörer (IgE, histamin, mastcellsmediatorer)
• IND-möjliggörande farmakologi och toxikologistudier
Parameter |
Mus PCA-modell |
Råtta PCA-modell |
Art/Stam |
BALB/c-mus |
Wistar råtta |
Induktionsmetod |
Intradermal injektion av DNP-IgE (passiv sensibilisering) + iv DNP-BSA med Evans blå | Intradermal injektion av OVA-sensibiliserat serum + iv OVA med Evans blue |
Studietid |
24–48 timmar (sensibilisering + utmaning) | 24–72 timmar |
Viktiga slutpunkter |
Evans blå extravasation (blå fläckdiameter eller OD), repningsbeteende räknas |
Kroppsvikt, örontjocklek, Evans blue extravasation (OD 620 nm), serum OVA-specifikt IgE, hudhistopatologi (toluidinblått) |
| Positiv kontroll | Anti-IgE-antikropp eller antihistamin (t.ex. cetirizin) tillgänglig som referensföreningar | |
Datapaket |
Rådata, analysrapporter, kliniska fotografier, ELISA-resultat, histologibilder, bioinformatik (valfritt) | |
F: Vilka är skillnaderna mellan PCA-modellerna för mus och råttor?
S: Musmodellen använder DNP-IgE för passiv sensibilisering och DNP-BSA för utmaning, perfekt för att studera rena IgE-medierade reaktioner. Råttmodellen använder serum från OVA-sensibiliserade donatorer, vilket ger ett mer komplext polyklonalt antikroppssvar och möjliggör bedömning av örontjocklek och repbeteende.
F: Hur kvantifieras den allergiska reaktionen i PCA-modeller?
S: Evans blå färg injiceras intravenöst med antigenet. Ökad vaskulär permeabilitet orsakar extravasering av färgämne på det sensibiliserade stället, vilket bildar en blå fläck. Reaktionen kvantifieras genom att mäta blå fläckdiameter, skära ut huden för färgextraktion och OD-mätning, eller genom att bedöma örontjocklek (råttmodell).
F: Kan dessa modeller användas för IND-aktiverande studier?
A: Ja. Studier kan utföras i enlighet med GLP-principer för regulatoriska inlämningar (FDA, EMA).
F: Erbjuder ni skräddarsydda studieprotokoll (t.ex. olika allergener, antikroppskoncentrationer)?
A: Absolut. Vårt forskarteam skräddarsyr sensibiliseringsprotokoll, utmaningsscheman och slutpunktsanalyser för din specifika läkemedelskandidat.
F: Vilken är den typiska tidslinjen för en pilotstudie om effektivitet?
S: Båda modellerna är akuta, med studier som vanligtvis slutförs inom 24–72 timmar efter passiv sensibilisering och antigenutmaning.
