| Tilgjengelighet: | |
|---|---|
| Antall: | |











Klinisk relevant – Rekapitulerer human type I overfølsomhet med IgE-mediert mastcelleaktivering, vasodilatasjon og kløe.
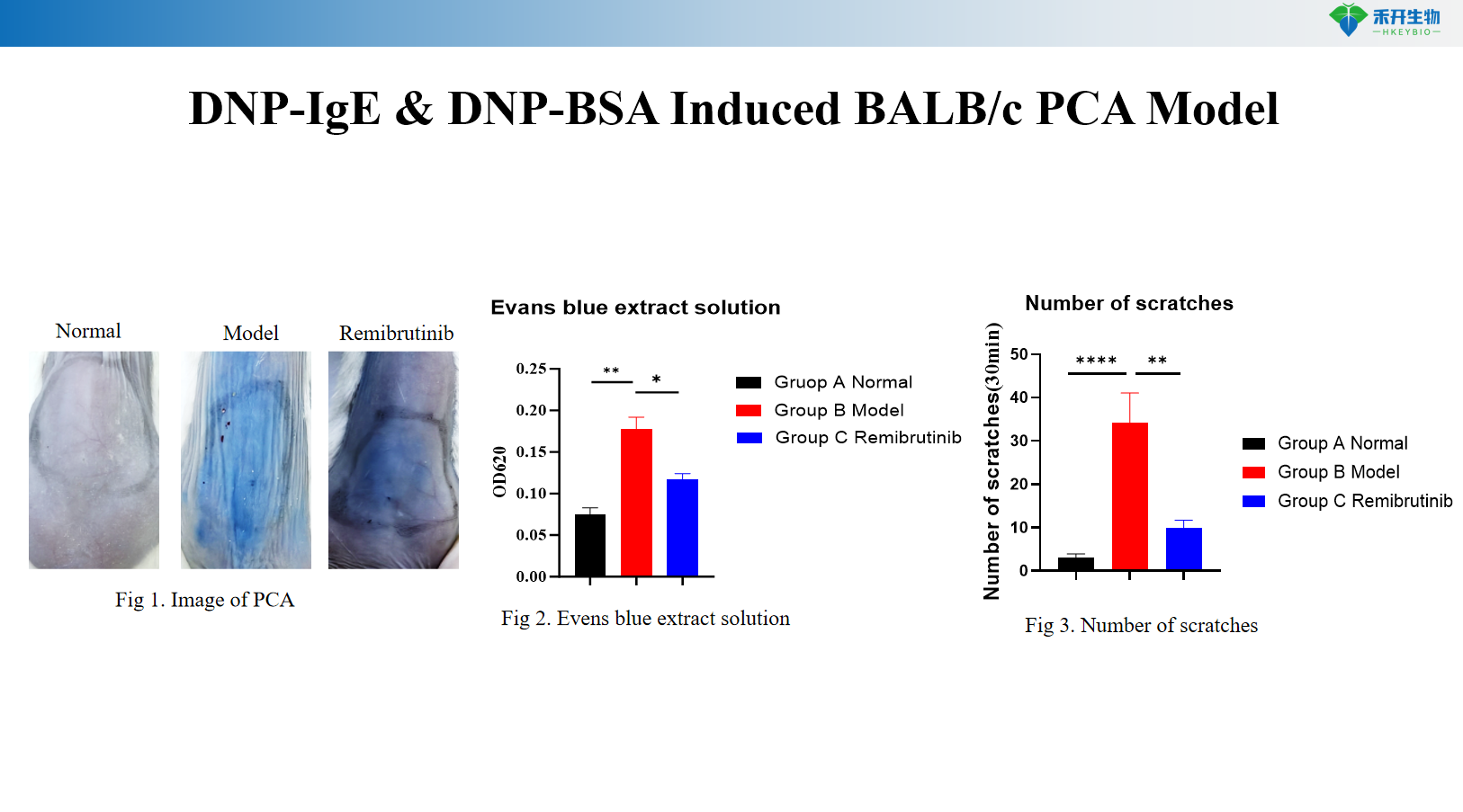
Kvantifiserbare endepunkter – Evans blå ekstravasasjon (blå flekkdiameter eller OD-måling), antall ripeadferd, øretykkelse, serum-IgE-nivåer.
To arter alternativer - Mus (BALB/c) og rotte (Wistar) modeller tilgjengelig for å passe forskjellige eksperimentelle behov.
Translasjonsverdi – Ideell for testing av biologiske anti-IgE (omalizumab), mastcellestabilisatorer (cromolyn), H1-antihistaminer og andre antiallergiske midler.
IND-klare datapakker – Studier kan utføres i henhold til GLP-prinsipper.
DNP-IgE & DNP-BSA-indusert BALB/c PCA-modell
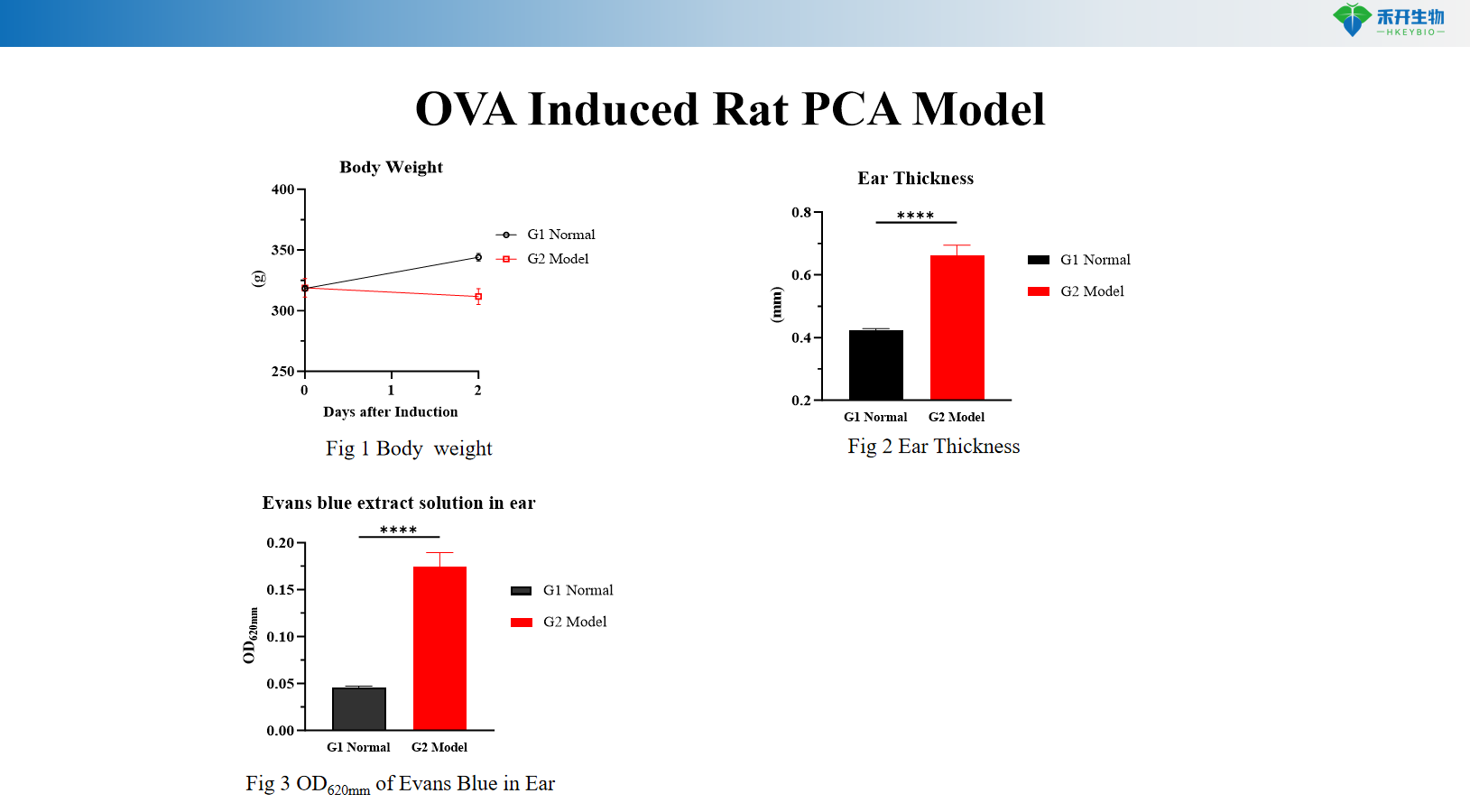
OVA-indusert rotte PCA-modell
• Effekttesting av biologiske anti-IgE (omalizumab, ligelizumab) og mastcellestabilisatorer (cromolyn, ketotifen)
• Evaluering av H1-antihistaminer (cetirizin, fexofenadin) og andre antiallergiske midler
• Målvalidering for IgE/FcεRI-vei og mastcellebiologi
• Biomarkørfunn (IgE, histamin, mastcellemediatorer)
• IND-aktiverende farmakologi og toksikologistudier
Parameter |
Mus PCA-modell |
Rotte PCA-modell |
Arter/Stamme |
BALB/c mus |
Wistar rotte |
Induksjonsmetode |
Intradermal injeksjon av DNP-IgE (passiv sensibilisering) + iv DNP-BSA med Evans blå | Intradermal injeksjon av OVA-sensibilisert serum + iv OVA med Evans blå |
Studievarighet |
24–48 timer (sensibilisering + utfordring) | 24–72 timer |
Viktige endepunkter |
Evans blå ekstravasasjon (blå flekkdiameter eller OD), antall riper |
Kroppsvekt, øretykkelse, Evans blå ekstravasasjon (OD 620 nm), serum OVA-spesifikk IgE, hudhistopatologi (toluidinblått) |
| Positiv kontroll | Anti-IgE-antistoff eller antihistamin (f.eks. cetirizin) tilgjengelig som referanseforbindelser | |
Datapakke |
Rådata, analyserapporter, kliniske fotografier, ELISA-resultater, histologiske lysbilder, bioinformatikk (valgfritt) | |
Spørsmål: Hva er forskjellene mellom PCA-modellene for mus og rotter?
A: Musemodellen bruker DNP-IgE for passiv sensibilisering og DNP-BSA for utfordring, ideell for å studere rene IgE-medierte reaksjoner. Rottemodellen bruker serum fra OVA-sensibiliserte donorer, og gir en mer kompleks polyklonal antistoffrespons og tillater vurdering av øretykkelse og skrapeadferd.
Spørsmål: Hvordan kvantifiseres den allergiske reaksjonen i PCA-modeller?
Sv: Evans blå fargestoff injiseres intravenøst med antigenet. Økt vaskulær permeabilitet forårsaker ekstravasering av fargestoff på det sensibiliserte stedet, og danner en blå flekk. Reaksjonen kvantifiseres ved å måle blåflekkdiameter, klippe ut huden for fargestoffekstraksjon og OD-måling, eller ved å vurdere øretykkelse (rottemodell).
Spørsmål: Kan disse modellene brukes til IND-aktiverende studier?
A: Ja. Studier kan utføres i samsvar med GLP-prinsipper for regulatoriske innleveringer (FDA, EMA).
Spørsmål: Tilbyr du tilpassede studieprotokoller (f.eks. forskjellige allergener, antistoffkonsentrasjoner)?
A: Absolutt. Vårt vitenskapelige team skreddersyr sensibiliseringsprotokoller, utfordringsplaner og endepunktsanalyser til din spesifikke medikamentkandidat.
Spørsmål: Hva er den typiske tidslinjen for en piloteffektstudie?
A: Begge modellene er akutte, med studier som vanligvis fullføres innen 24–72 timer etter passiv sensibilisering og antigenutfordring.
