| Disponibilidade: | |
|---|---|
| Quantidade: | |











Clinicamente relevante – Recapitula a hipersensibilidade humana tipo I com ativação de mastócitos mediada por IgE, vasodilatação e prurido.
Endpoints quantificáveis – extravasamento de azul de Evans (diâmetro do ponto azul ou medição de DO), contagem de comportamento de coçar, espessura da orelha, níveis séricos de IgE.
Duas opções de espécies – modelos de camundongo (BALB/c) e rato (Wistar) disponíveis para atender a diferentes necessidades experimentais.
Valor translacional – Ideal para testar produtos biológicos anti-IgE (omalizumabe), estabilizadores de mastócitos (cromolina), anti-histamínicos H1 e outros agentes antialérgicos.
Pacotes de dados prontos para IND – Os estudos podem ser conduzidos de acordo com os princípios das BPL.
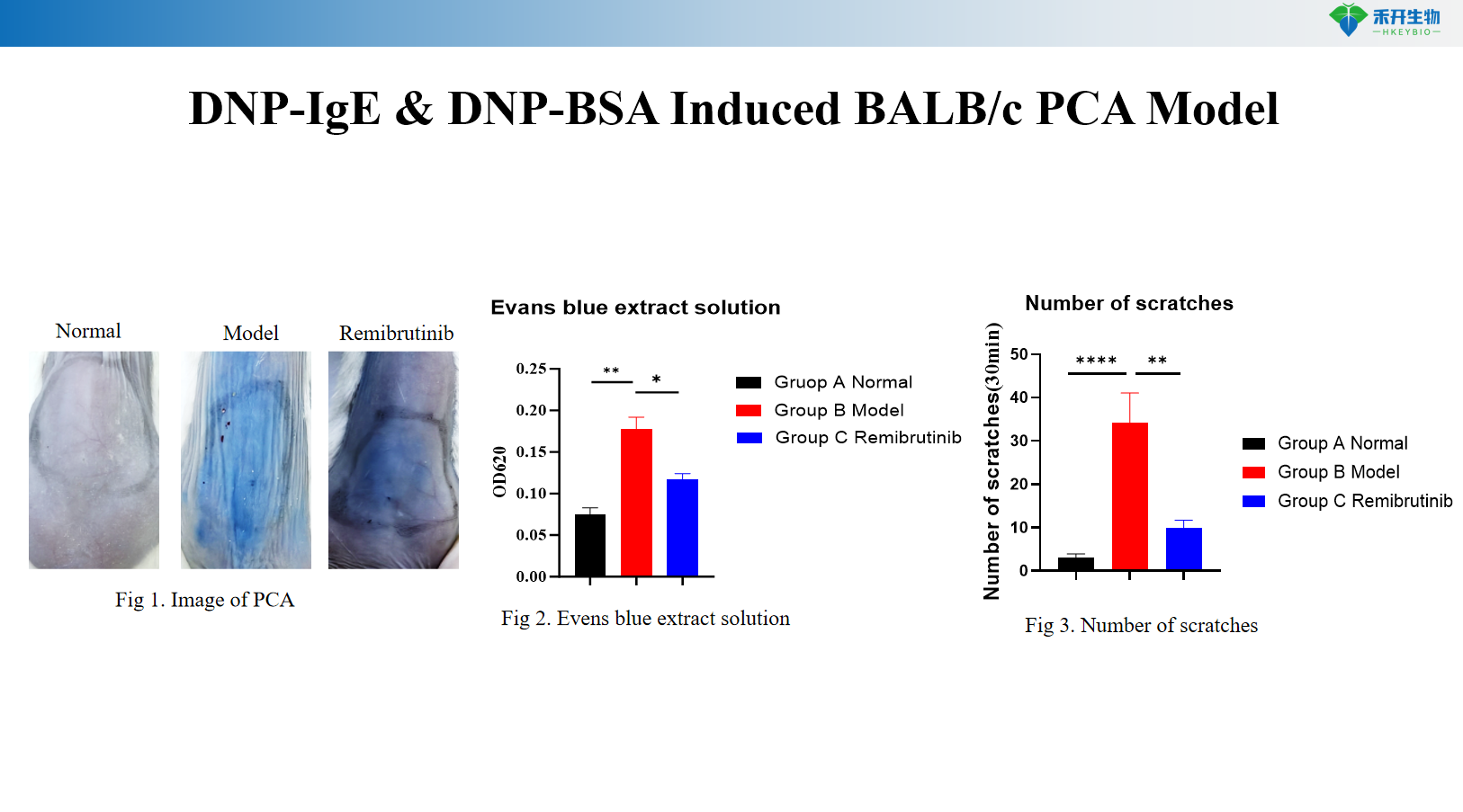
Modelo BALB/c PCA induzido por DNP-IgE e DNP-BSA
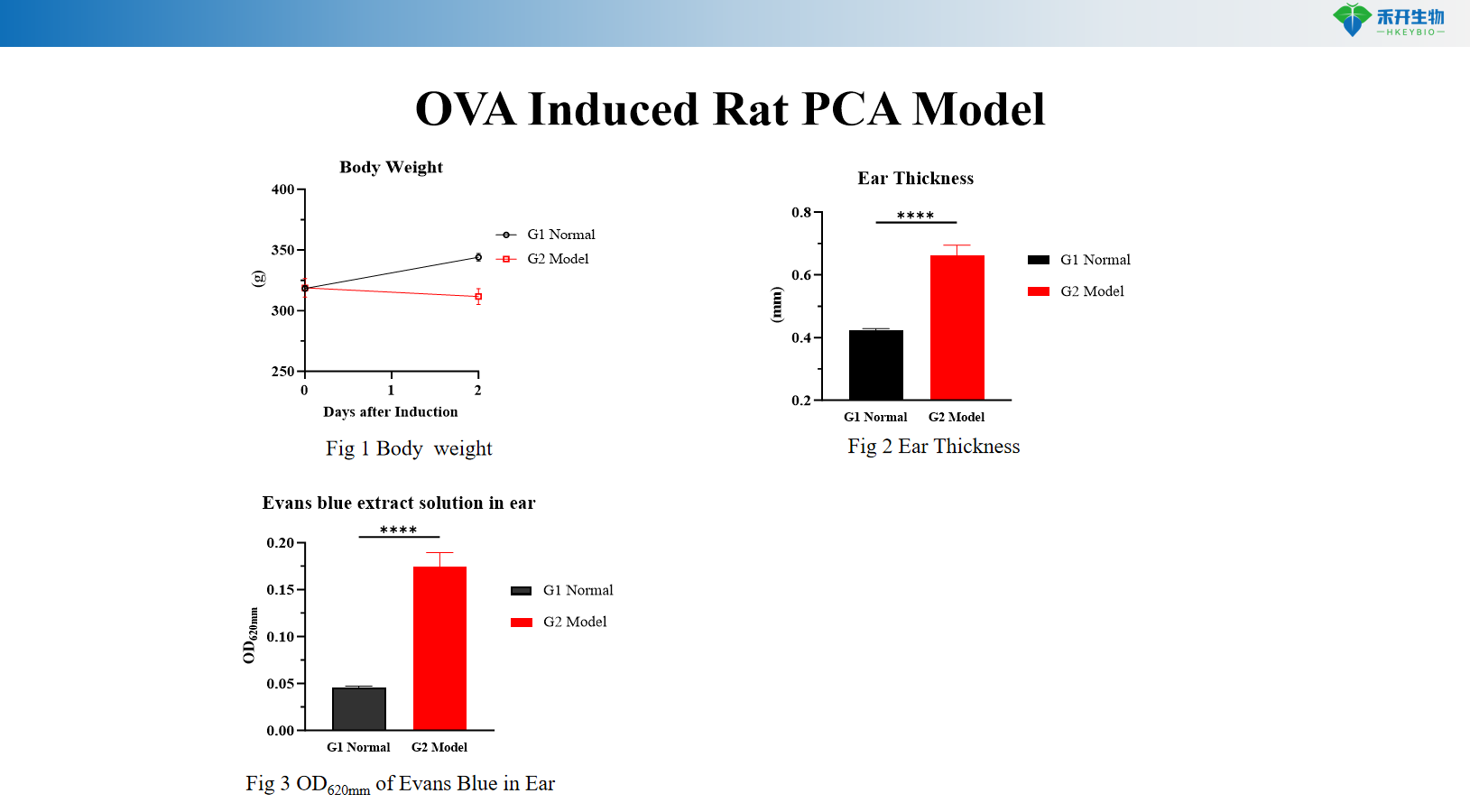
Modelo PCA de rato induzido por OVA
• Teste de eficácia de produtos biológicos anti-IgE (omalizumabe, ligelizumabe) e estabilizadores de mastócitos (cromolina, cetotifeno)
• Avaliação de anti-histamínicos H1 (cetirizina, fexofenadina) e outros agentes antialérgicos
• Validação de alvo para via IgE/FcεRI e biologia de mastócitos
• Descoberta de biomarcadores (IgE, histamina, mediadores de mastócitos)
• Estudos de farmacologia e toxicologia que permitem IND
Parâmetro |
Modelo PCA de mouse |
Modelo PCA de rato |
Espécie/Estirpe |
Rato BALB/c |
Rato Wistar |
Método de indução |
Injeção intradérmica de DNP-IgE (sensibilização passiva) + DNP-BSA iv com azul de Evans | Injeção intradérmica de soro sensibilizado com OVA + OVA iv com azul de Evans |
Duração do estudo |
24–48 horas (sensibilização + desafio) | 24–72 horas |
Principais pontos de extremidade |
Extravasamento de azul de Evans (diâmetro da mancha azul ou OD), contagem de comportamento de coçar |
Peso corporal, espessura da orelha, extravasamento de azul de Evans (DO 620 nm), IgE sérica específica para OVA, histopatologia da pele (azul de toluidina) |
| Controle positivo | Anticorpo anti-IgE ou anti-histamínico (por exemplo, cetirizina) disponíveis como compostos de referência | |
Pacote de dados |
Dados brutos, relatórios de análise, fotografias clínicas, resultados de ELISA, lâminas histológicas, bioinformática (opcional) | |
P: Quais são as diferenças entre os modelos PCA de camundongo e rato?
R: O modelo de camundongo usa DNP-IgE para sensibilização passiva e DNP-BSA para desafio, ideal para estudar reações mediadas por IgE pura. O modelo de rato utiliza soro de doadores sensibilizados com OVA, proporcionando uma resposta de anticorpos policlonais mais complexa e permitindo a avaliação da espessura da orelha e do comportamento de coçar.
P: Como a reação alérgica é quantificada nos modelos PCA?
A: O corante azul de Evans é injetado por via intravenosa com o antígeno. O aumento da permeabilidade vascular causa extravasamento de corante no local sensibilizado, formando uma mancha azul. A reação é quantificada medindo o diâmetro da mancha azul, extirpando a pele para extração de corante e medição de DO, ou avaliando a espessura da orelha (modelo de rato).
P: Esses modelos podem ser usados para estudos que permitem o IND?
R: Sim. Os estudos podem ser conduzidos de acordo com os princípios das BPL para submissões regulatórias (FDA, EMA).
P: Vocês oferecem protocolos de estudo personalizados (por exemplo, diferentes alérgenos, concentrações de anticorpos)?
R: Absolutamente. Nossa equipe científica adapta protocolos de sensibilização, cronogramas de desafio e análises de endpoints para seu medicamento candidato específico.
P: Qual é o cronograma típico para um estudo piloto de eficácia?
R: Ambos os modelos são agudos, com estudos normalmente concluídos dentro de 24 a 72 horas após a sensibilização passiva e o desafio antigênico.
