| Tilgængelighed: | |
|---|---|
| Antal: | |











Klinisk relevant – Rekapitulerer human type I overfølsomhed med IgE-medieret mastcelleaktivering, vasodilatation og kløe.
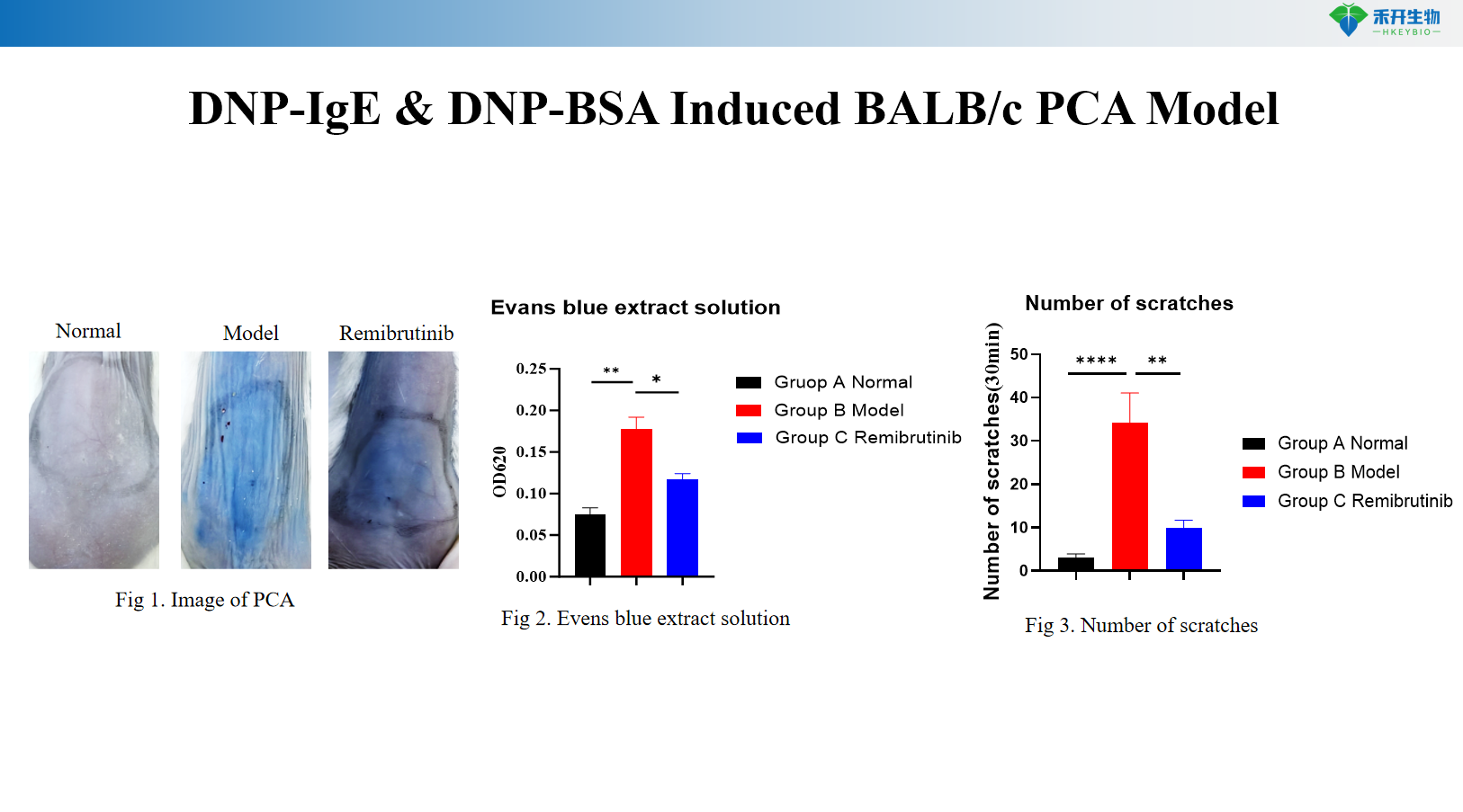
Kvantificerbare endepunkter – Evans blå ekstravasation (blå pletdiameter eller OD-måling), ridseadfærdstælling, øretykkelse, serum-IgE-niveauer.
To arter muligheder - Mus (BALB/c) og rotte (Wistar) modeller tilgængelige for at passe til forskellige eksperimentelle behov.
Translationel værdi – Ideel til test af biologiske anti-IgE (omalizumab), mastcellestabilisatorer (cromolyn), H1-antihistaminer og andre anti-allergiske midler.
IND-klare datapakker – Undersøgelser kan udføres i overensstemmelse med GLP principper.
DNP-IgE & DNP-BSA-induceret BALB/c PCA-model
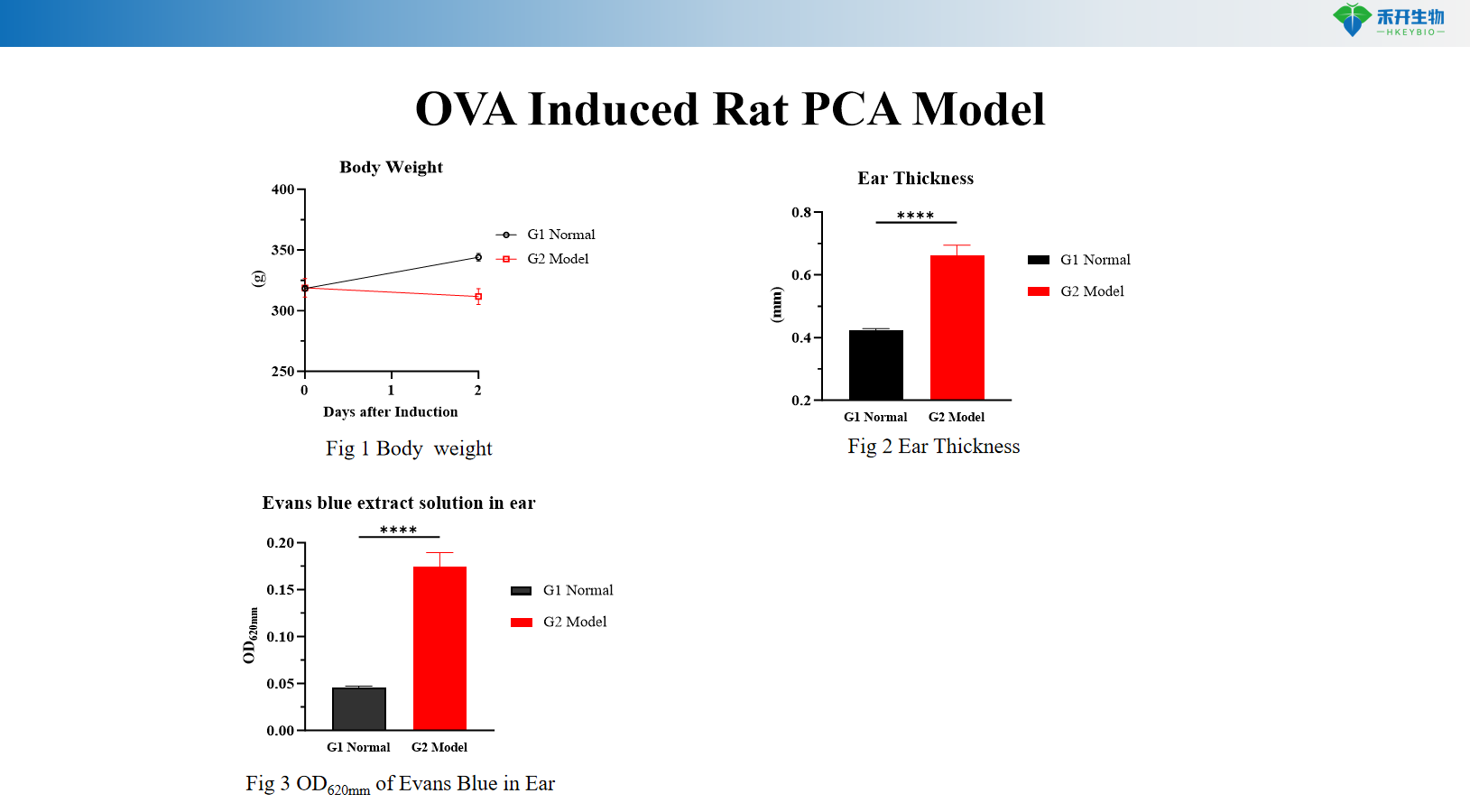
OVA-induceret rotte PCA-model
• Effektivitetstest af anti-IgE biologiske lægemidler (omalizumab, ligelizumab) og mastcellestabilisatorer (cromolyn, ketotifen)
• Evaluering af H1-antihistaminer (cetirizin, fexofenadin) og andre anti-allergiske midler
• Målvalidering for IgE/FcεRI pathway og mastcellebiologi
• Biomarkøropdagelse (IgE, histamin, mastcellemediatorer)
• IND-aktiverende farmakologi og toksikologiske undersøgelser
Parameter |
Mus PCA model |
Rotte PCA-model |
Art/Stamme |
BALB/c mus |
Wistar rotte |
Induktionsmetode |
Intradermal injektion af DNP-IgE (passiv sensibilisering) + iv DNP-BSA med Evans blå | Intradermal injektion af OVA-sensibiliseret serum + iv OVA med Evans blue |
Studievarighed |
24-48 timer (sensibilisering + udfordring) | 24-72 timer |
Nøgleendepunkter |
Evans blå ekstravasation (blå plet diameter eller OD), ridseadfærd tæller |
Kropsvægt, øretykkelse, Evans blå ekstravasation (OD 620 nm), serum OVA-specifik IgE, hudhistopatologi (toluidinblå) |
| Positiv kontrol | Anti-IgE-antistof eller antihistamin (f.eks. cetirizin) tilgængelig som referenceforbindelser | |
Datapakke |
Rådata, analyserapporter, kliniske fotografier, ELISA-resultater, histologiske dias, bioinformatik (valgfrit) | |
Q: Hvad er forskellene mellem muse- og rotte-PCA-modellerne?
A: Musemodellen bruger DNP-IgE til passiv sensibilisering og DNP-BSA til udfordring, ideel til at studere rene IgE-medierede reaktioner. Rottemodellen bruger serum fra OVA-sensibiliserede donorer, hvilket giver et mere komplekst polyklonalt antistofrespons og muliggør vurdering af øretykkelse og ridseadfærd.
Q: Hvordan kvantificeres den allergiske reaktion i PCA-modeller?
A: Evans blå farvestof injiceres intravenøst med antigenet. Øget vaskulær permeabilitet forårsager ekstravasation af farvestof på det sensibiliserede sted og danner en blå plet. Reaktionen kvantificeres ved at måle blå pletdiameter, udskære huden til farvestofekstraktion og OD-måling eller ved at vurdere øretykkelsen (rottemodel).
Q: Kan disse modeller bruges til IND-aktiverende undersøgelser?
A: Ja. Undersøgelser kan udføres i overensstemmelse med GLP-principperne for regulatoriske indsendelser (FDA, EMA).
Spørgsmål: Tilbyder du tilpassede undersøgelsesprotokoller (f.eks. forskellige allergener, antistofkoncentrationer)?
A: Absolut. Vores videnskabelige team skræddersyr sensibiliseringsprotokoller, udfordringsplaner og slutpunktsanalyser til din specifikke lægemiddelkandidat.
Q: Hvad er den typiske tidslinje for et piloteffektivitetsstudie?
A: Begge modeller er akutte, med undersøgelser, der typisk afsluttes inden for 24-72 timer efter passiv sensibilisering og antigenudfordring.
