| Наявність: | |
|---|---|
| Кількість: | |











Клінічно значущий – повторює гіперчутливість людини типу I з IgE-опосередкованою активацією тучних клітин, вазодилатацією та свербінням.
Кінцеві точки, що піддаються кількісному вимірюванню – синя екстравазація Еванса (діаметр синьої плями або вимірювання OD), кількість подряпин, товщина вуха, рівень IgE в сироватці крові.
Варіанти двох видів – миші (BALB/c) і щури (Wistar) доступні для різних експериментальних потреб.
Трансляційна цінність – ідеально підходить для тестування біологічних препаратів проти IgE (омалізумаб), стабілізаторів тучних клітин (кромолін), H1-антигістамінних препаратів та інших протиалергічних засобів.
Пакети даних, готові до IND – дослідження можна проводити відповідно до принципів GLP.
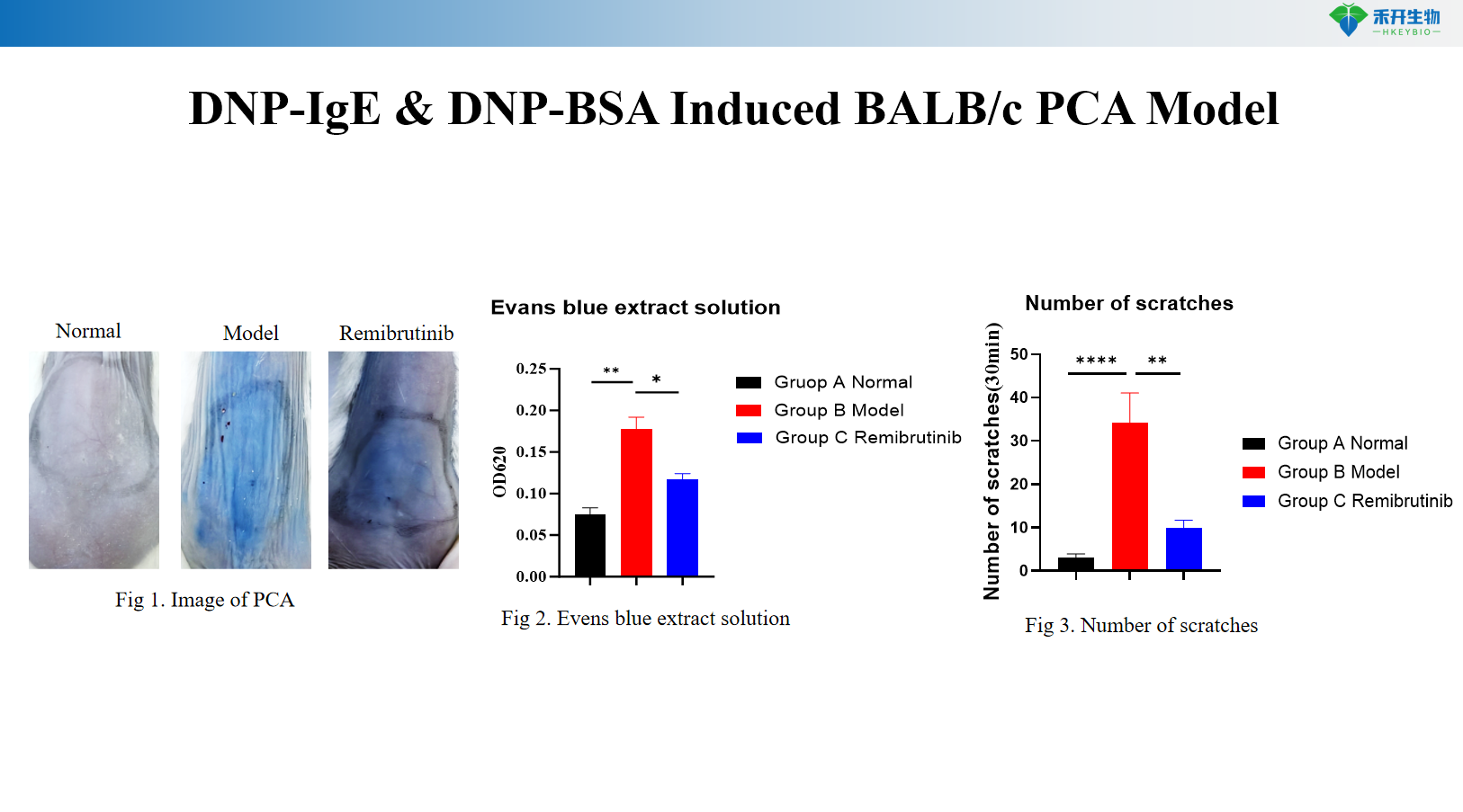
Модель BALB/c PCA, індукована DNP-IgE та DNP-BSA
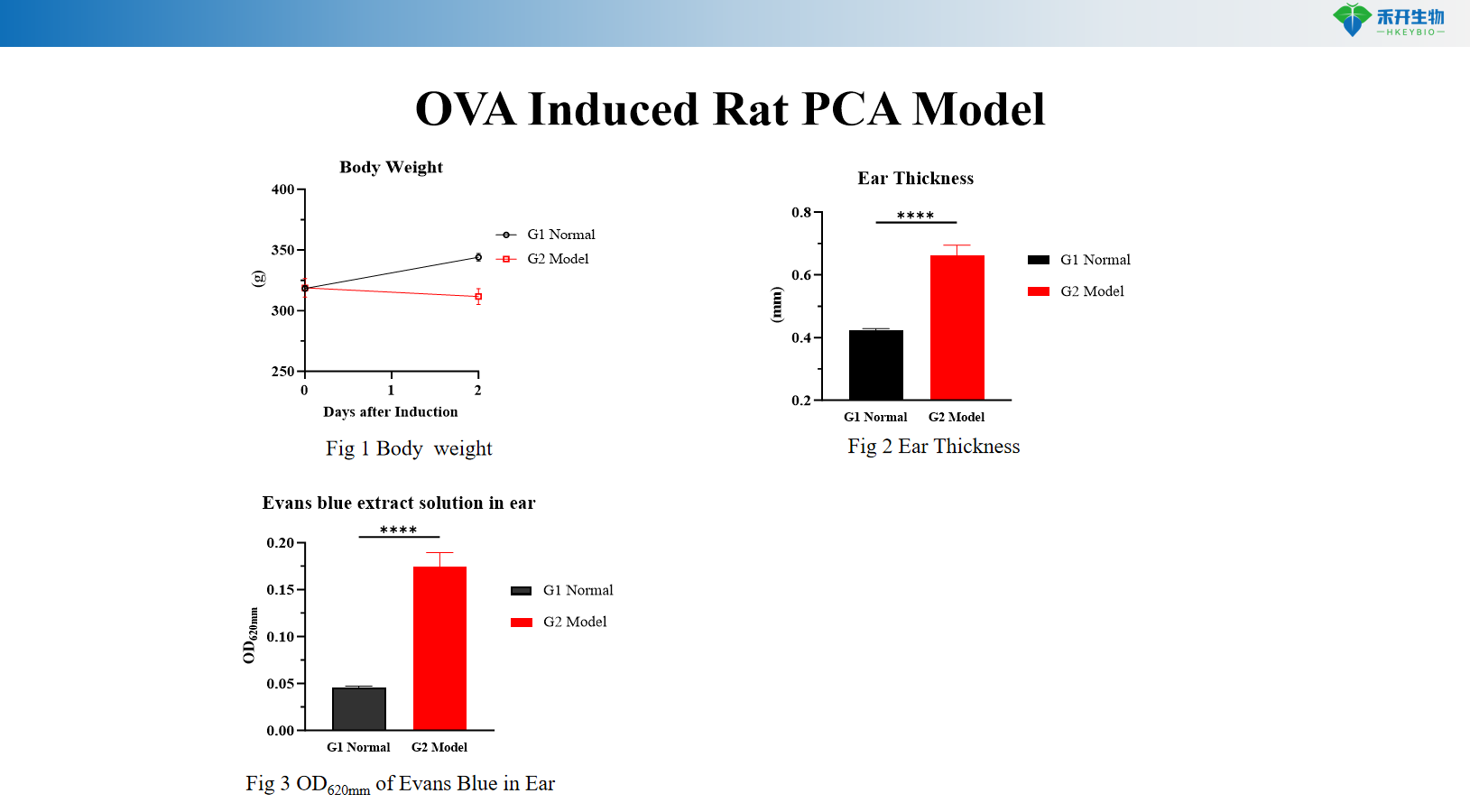
OVA-індукована модель PCA щурів
• Перевірка ефективності біологічних препаратів проти IgE (омалізумаб, лігелізумаб) і стабілізаторів тучних клітин (кромолін, кетотифен)
• Оцінка Н1-антигістамінних препаратів (цетиризину, фексофенадину) та інших протиалергічних засобів
• Цільова перевірка шляху IgE/FcεRI та біології тучних клітин
• Виявлення біомаркерів (IgE, гістамін, медіатори тучних клітин)
• Фармакологічні та токсикологічні дослідження, що сприяють IND
Параметр |
Модель миші PCA |
Щур PCA Модель |
Вид/штам |
Миша BALB/c |
Щур Вістар |
Індукційний метод |
Внутрішньошкірна ін’єкція DNP-IgE (пасивна сенсибілізація) + в/в DNP-BSA з синім Еванса | Внутрішньошкірна ін’єкція OVA-сенсибілізованої сироватки + в/в OVA з синім Еванса |
Тривалість дослідження |
24–48 годин (сенсибілізація + виклик) | 24–72 години |
Ключові кінцеві точки |
Синя екстравазація Еванса (діаметр блакитної плями або OD), підрахунок поведінки подряпин |
Маса тіла, товщина вуха, екстравазація синього Еванса (OD 620 нм), сироватковий OVA-специфічний IgE, гістопатологія шкіри (толуїдиновий синій) |
| Позитивний контроль | Антитіло проти IgE або антигістамін (наприклад, цетиризин) доступні як контрольні сполуки | |
Пакет даних |
Необроблені дані, звіти про аналізи, клінічні фотографії, результати ELISA, гістологічні слайди, біоінформатика (необов’язково) | |
Питання: Які відмінності між моделями PCA миші та щура?
A: Мишача модель використовує DNP-IgE для пасивної сенсибілізації та DNP-BSA для зараження, що ідеально підходить для вивчення чистих реакцій, опосередкованих IgE. Модель щурів використовує сироватку від OVA-сенсибілізованих донорів, забезпечуючи більш складну відповідь поліклональних антитіл і дозволяючи оцінити товщину вуха та поведінку подряпин.
З: Як кількісно визначається алергічна реакція в моделях PCA?
A: Синій барвник Еванса вводиться внутрішньовенно разом з антигеном. Підвищена проникність судин викликає екстравазацію барвника на сенсибілізованому місці, утворюючи синю пляму. Реакцію кількісно визначають шляхом вимірювання діаметра блакитної плями, вирізання шкіри для екстракції барвника та вимірювання OD або шляхом оцінки товщини вуха (модель на щурах).
З: Чи можна використовувати ці моделі для досліджень, що сприяють IND?
A: Так. Дослідження можна проводити відповідно до принципів GLP для нормативних документів (FDA, EMA).
З: Чи пропонуєте ви індивідуальні протоколи дослідження (наприклад, різні алергени, концентрації антитіл)?
A: Абсолютно. Наша наукова команда адаптує протоколи сенсибілізації, графіки викликів і аналізи кінцевих точок для вашого конкретного препарату-кандидата.
З: Який типовий графік пілотного дослідження ефективності?
A: Обидві моделі є гострими, дослідження зазвичай завершуються протягом 24–72 годин після пасивної сенсибілізації та зараження антигеном.
