| Disponibilité : | |
|---|---|
| Quantité : | |











Cliniquement pertinent – récapitule l'uvéite auto-immune humaine avec une inflammation médiée par les Th1/Th17, des lésions rétiniennes et une rupture de la barrière hémato-rétinienne.
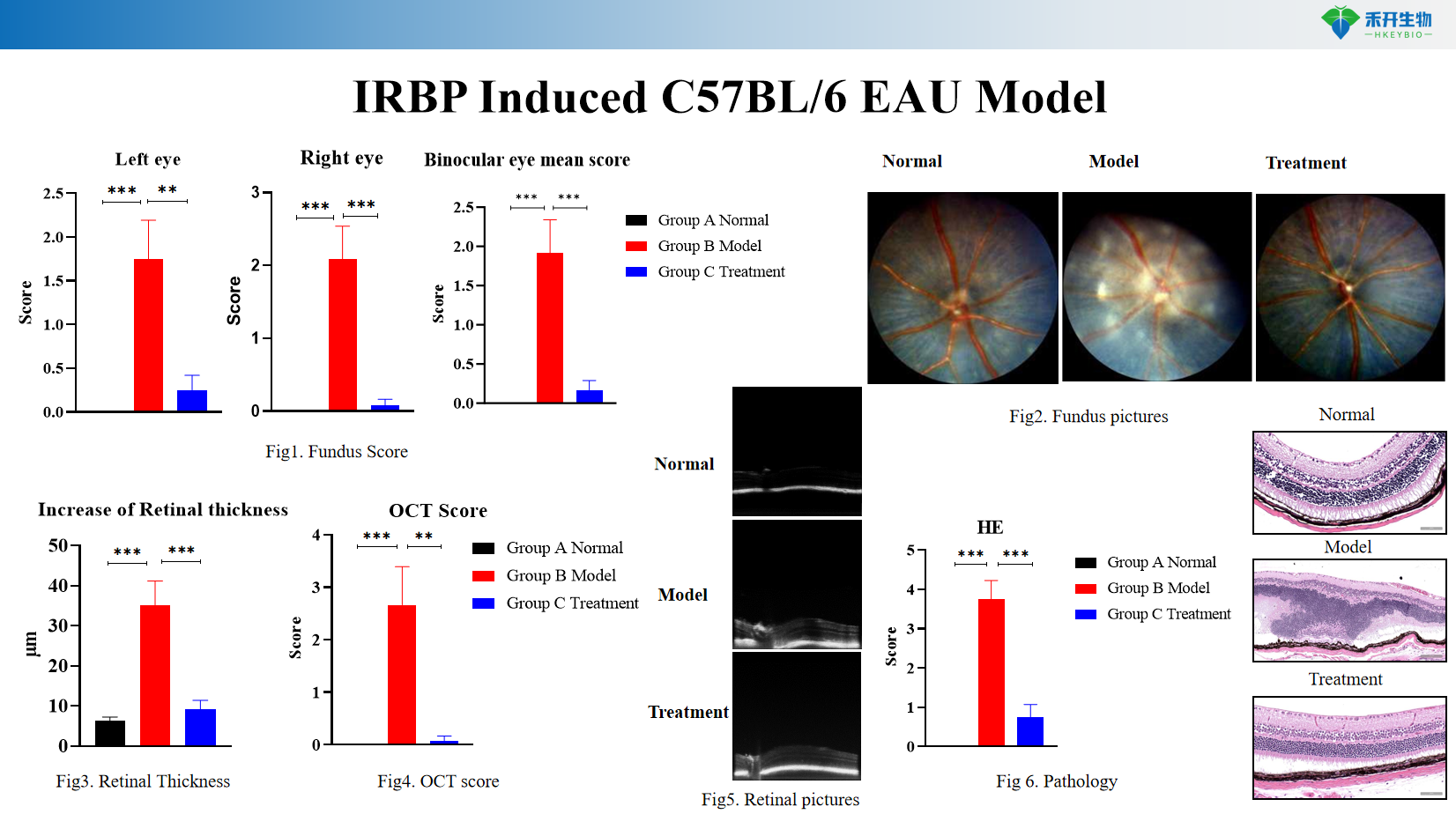
Paramètres d'imagerie avancés – Photographie et notation du fond d'œil, tomographie par cohérence optique (OCT) pour la mesure de l'épaisseur de la rétine.
Pathologie complète – Histopathologie (coloration HE) pour infiltration inflammatoire et dommages structurels rétiniens.
Axé sur un mécanisme : l'IRBP active les cellules présentatrices d'antigène, entraînant la différenciation Th1 et Th17 et la production de cytokines inflammatoires (IFN-γ, IL-17, TNF-α).
Ensembles de données prêts pour l'IND – Les études peuvent être menées conformément aux principes BPL.
Modèle C57BL/6 EAU induit par IRBP
• Tests d'efficacité des immunomodulateurs (corticostéroïdes, méthotrexate, mycophénolate) dans l'uvéite auto-immune
• Évaluation de produits biologiques ciblant les voies Th1/Th17 (anti-IL-17, anti-IL-23, anti-IFN-γ)
• Validation de la cible pour les réponses auto-immunes médiées par les lymphocytes T dans l'œil
• Découverte de biomarqueurs (cytokines inflammatoires, marqueurs de lésions rétiniennes)
• Études pharmacologiques et toxicologiques permettant l'IND
Paramètre |
Spécification |
Espèce/souche |
Souris C57BL/6 |
Méthode d'induction |
Immunisation sous-cutanée avec le peptide IRBP (par exemple, IRBP1-20, 200-300 μg) émulsionné dans du CFA complété par Mycobacterium tuberculosis, plus la toxine coquelucheuse intrapéritonéale (0,5-1 μg) au moment de l'immunisation |
Durée des études |
21 à 35 jours après la vaccination (pic de la maladie ~ 14 à 21 jours) |
Points de terminaison clés |
Photographie du fond d'œil et score clinique (échelle 0-4 pour disque optique, vascularite, infiltrats), tomographie par cohérence optique (OCT) pour la mesure de l'épaisseur de la rétine, score OCT, histopathologie (coloration HE de la rétine pour infiltration inflammatoire et dommages structurels), facultatif : cytométrie en flux des cellules immunitaires rétiniennes/ganglions lymphatiques (cellules T CD4+, sous-ensembles Th1/Th17), analyse des cytokines (IFN-γ, IL-17, TNF-α) |
Paquet de données |
Données brutes, rapports d'analyses, images du fond d'œil, données OCT, lames histologiques, bioinformatique (optionnel) Données brutes, rapports d'analyses, scores cliniques, lames histologiques, analyse sérique (IL-6, CRP), optionnel : anticorps anti-CII, imagerie micro-CT |
Q : Comment l’IRBP induit-elle l’EAU ?
R : L'IRBP est un antigène rétinien. L'immunisation avec le peptide IRBP dans l'adjuvant active les cellules présentatrices d'antigène, qui présentent l'antigène aux lymphocytes T naïfs, conduisant ainsi à leur différenciation en effecteurs pathogènes Th1 et Th17. Ces cellules infiltrent l’œil, libèrent des cytokines inflammatoires (IFN-γ, IL-17, TNF-α) et provoquent une inflammation et des lésions rétiniennes.
Q : Quelles sont les principales similitudes avec l’uvéite auto-immune humaine ?
R : Le modèle présente une inflammation médiée par les lymphocytes T (Th1/Th17), une rupture de la barrière hémato-rétinienne, une infiltration de cellules inflammatoires, des dommages structurels rétiniens et des signes cliniques visibles par fond d'œil et OCT, reflétant étroitement l'uvéite humaine non infectieuse.
Q : Ce modèle peut-il être utilisé pour des études permettant l’IND ?
R : Oui. Les études peuvent être menées conformément aux principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différents peptides IRBP, doses, calendrier du traitement) ?
R : Absolument. Notre équipe scientifique adapte les protocoles de vaccination, les calendriers de traitement et les analyses des paramètres à votre candidat-médicament spécifique.
