| Disponibilidad: | |
|---|---|
| Cantidad: | |











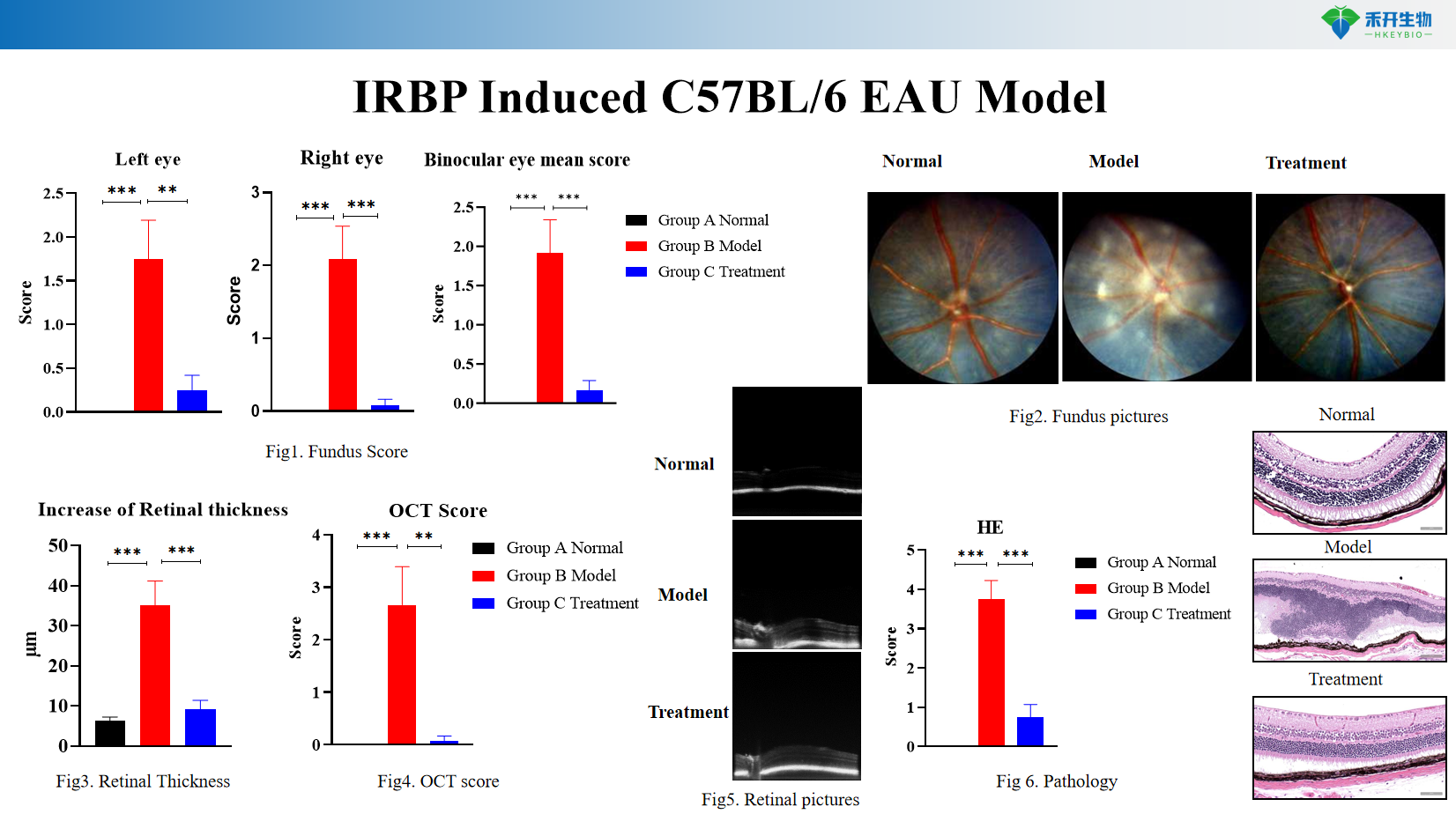
Clínicamente relevante : recapitula la uveítis autoinmune humana con inflamación mediada por Th1/Th17, daño retiniano y ruptura de la barrera hematorretiniana.
Criterios de valoración de imágenes avanzadas : fotografía y puntuación del fondo de ojo, tomografía de coherencia óptica (OCT) para medir el espesor de la retina.
Patología integral : histopatología (tinción HE) para infiltración inflamatoria y daño estructural de la retina.
Impulsado por mecanismos : la IRBP activa las células presentadoras de antígenos, impulsando la diferenciación de Th1 y Th17 y la producción de citoquinas inflamatorias (IFN-γ, IL-17, TNF-α).
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
Modelo EAU C57BL/6 inducido por IRBP
• Pruebas de eficacia de inmunomoduladores (corticosteroides, metotrexato, micofenolato) para la uveítis autoinmune
• Evaluación de productos biológicos dirigidos a las vías Th1/Th17 (anti-IL-17, anti-IL-23, anti-IFN-γ)
• Validación de objetivos para respuestas autoinmunes mediadas por células T en el ojo
• Descubrimiento de biomarcadores (citocinas inflamatorias, marcadores de daño retiniano)
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Especificación |
Especie/Cepa |
Ratón C57BL/6 |
Método de inducción |
Inmunización subcutánea con péptido IRBP (p. ej., IRBP1-20, 200-300 μg) emulsionado en CFA suplementado con Mycobacterium tuberculosis, más toxina pertussis intraperitoneal (0,5-1 μg) en el momento de la inmunización |
Duración del estudio |
21 a 35 días después de la inmunización (pico de enfermedad ~14 a 21 días) |
Puntos finales clave |
Fotografía del fondo de ojo y puntuación clínica (escala 0-4 para disco óptico, vasculitis, infiltrados), tomografía de coherencia óptica (OCT) para medir el grosor de la retina, puntuación OCT, histopatología (tinción HE de la retina para infiltración inflamatoria y daño estructural), opcional: citometría de flujo de células inmunes de la retina/nódulos linfáticos (células T CD4+, subconjuntos Th1/Th17), análisis de citoquinas (IFN-γ, IL-17, TNF-α) |
Paquete de datos |
Datos sin procesar, informes de análisis, imágenes de fondo de ojo, datos de OCT, portaobjetos de histología, bioinformática (opcional) Datos sin procesar, informes de análisis, puntuaciones clínicas, portaobjetos de histología, análisis de suero (IL-6, PCR), opcional: anticuerpos anti-CII, imágenes por micro-CT |
P: ¿Cómo induce la IRBP la EAU?
R: IRBP es un antígeno retiniano. La inmunización con péptido IRBP en adyuvante activa las células presentadoras de antígeno, que presentan el antígeno a las células T vírgenes, impulsando su diferenciación en efectores patógenos Th1 y Th17. Estas células se infiltran en el ojo, liberan citoquinas inflamatorias (IFN-γ, IL-17, TNF-α) y causan inflamación y daño a la retina.
P: ¿Cuáles son las similitudes clave con la uveítis autoinmune humana?
R: El modelo exhibe inflamación mediada por células T (Th1/Th17), ruptura de la barrera hematorretiniana, infiltración de células inflamatorias, daño estructural de la retina y signos clínicos visibles mediante fundoscopia y OCT, lo que refleja fielmente la uveítis humana no infecciosa.
P: ¿Se puede utilizar este modelo para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes péptidos IRBP, dosis, momento del tratamiento)?
R: Absolutamente. Nuestro equipo científico adapta los protocolos de vacunación, los programas de tratamiento y los análisis de criterios de valoración a su fármaco candidato específico.
