| Tilgjengelighet: | |
|---|---|
| Antall: | |











Klinisk relevant – Rekapitulerer human autoimmun uveitt med Th1/Th17-mediert betennelse, netthinneskade og nedbrytning av blod-retinal barriere.
Avanserte avbildningsendepunkter – Fundusfotografering og scoring, optisk koherenstomografi (OCT) for måling av netthinnetykkelse.
Omfattende patologi – Histopatologi (HE-farging) for inflammatorisk infiltrasjon og strukturell skade på netthinnen.
Mekanismedrevet – IRBP aktiverer antigenpresenterende celler, driver Th1- og Th17-differensiering og inflammatorisk cytokinproduksjon (IFN-γ, IL-17, TNF-α).
IND-klare datapakker – Studier kan utføres i henhold til GLP-prinsipper.
IRBP-indusert C57BL/6 EAU-modell
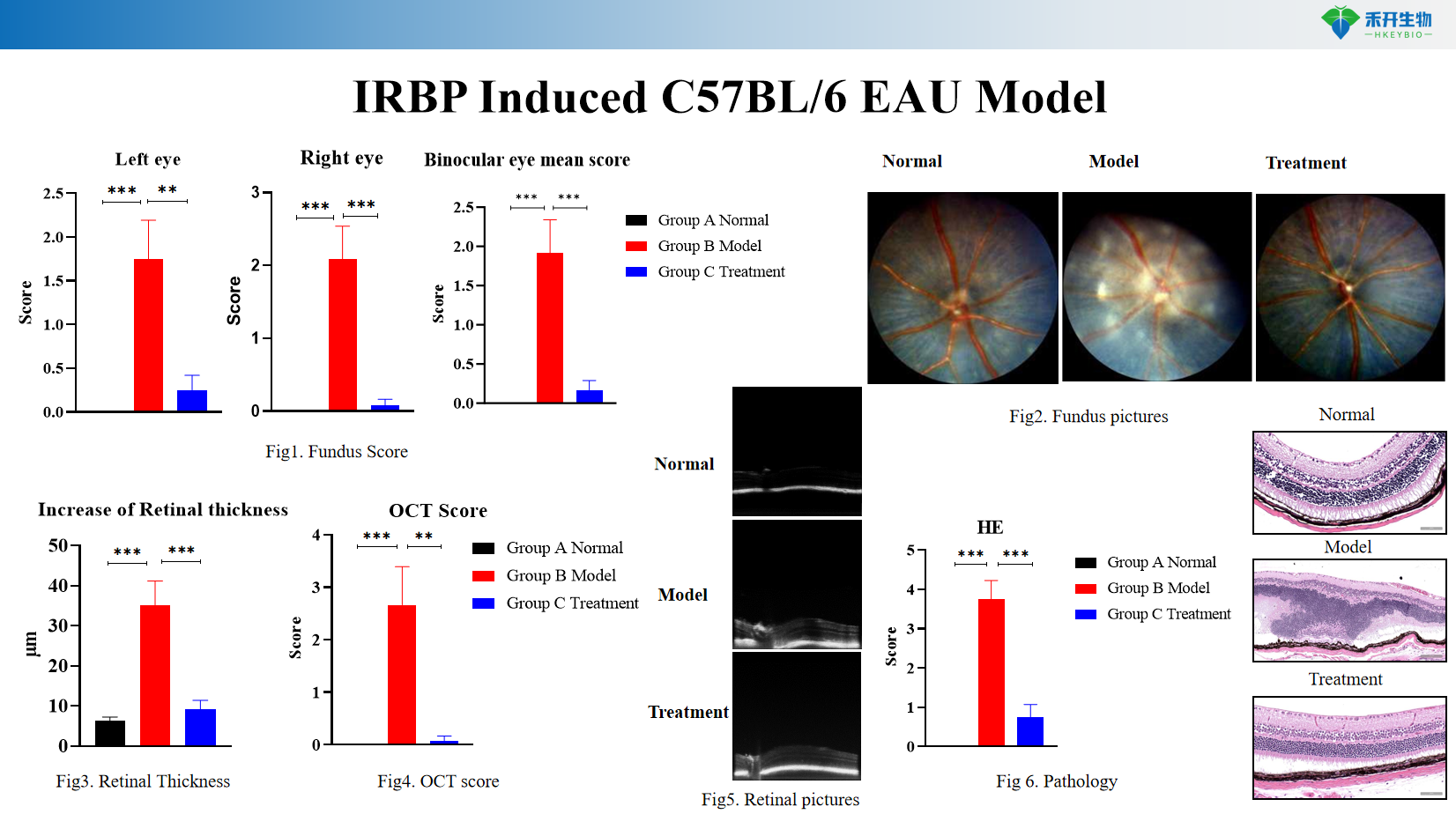
• Effekttesting av immunmodulatorer (kortikosteroider, metotreksat, mykofenolat) for autoimmun uveitt
• Evaluering av biologiske midler rettet mot Th1/Th17-veier (anti-IL-17, anti-IL-23, anti-IFN-γ)
• Målvalidering for T-cellemediert autoimmune responser i øyet
• Biomarkørfunn (inflammatoriske cytokiner, markører for netthinneskade)
• IND-aktiverende farmakologi og toksikologistudier
Parameter |
Spesifikasjon |
Arter/Stamme |
C57BL/6 mus |
Induksjonsmetode |
Subkutan immunisering med IRBP-peptid (f.eks. IRBP1-20, 200-300 μg) emulgert i CFA supplert med Mycobacterium tuberculosis, pluss intraperitonealt pertussis-toksin (0,5-1 μg) ved immunisering |
Studievarighet |
21–35 dager etter immunisering (toppsykdom ~14–21 dager) |
Viktige endepunkter |
Fundusfotografering og klinisk skåring (skala 0-4 for optisk skive, vaskulitt, infiltrater), optisk koherenstomografi (OCT) for måling av netthinnetykkelse, OCT-skåring, histopatologi (HE-farging av netthinnen for inflammatorisk infiltrasjon og strukturelle skader), valgfritt: flowcytometri av retinal/lymfeknute/t17-immunceller, cytokiner, subCD4+-immunceller (Th17) (IFN-y, IL-17, TNF-a) |
Datapakke |
Rådata, analyserapporter, fundusbilder, OCT-data, histologiske lysbilder, bioinformatikk (valgfritt) Rådata, analyserapporter, kliniske skårer, histologiske lysbilder, serumanalyse (IL-6, CRP), valgfritt: anti-CII-antistoffer, mikro-CT-avbildning |
Spørsmål: Hvordan induserer IRBP EAU?
A: IRBP er et retinalt antigen. Immunisering med IRBP-peptid i adjuvans aktiverer antigenpresenterende celler, som presenterer antigenet til naive T-celler, og driver deres differensiering til patogene Th1- og Th17-effektorer. Disse cellene infiltrerer øyet, frigjør inflammatoriske cytokiner (IFN-γ, IL-17, TNF-α), og forårsaker retinal betennelse og skade.
Spørsmål: Hva er de viktigste likhetene med human autoimmun uveitt?
A: Modellen viser T-celle-mediert betennelse (Th1/Th17), nedbrytning av blod-retinal barriere, inflammatorisk celleinfiltrasjon, retinal strukturell skade og kliniske tegn synlige ved fundoskopi og OCT, som tett speiler human ikke-infeksiøs uveitt.
Spørsmål: Kan denne modellen brukes til IND-aktiverende studier?
A: Ja. Studier kan utføres i samsvar med GLP-prinsipper for regulatoriske innleveringer (FDA, EMA).
Spørsmål: Tilbyr du tilpassede studieprotokoller (f.eks. forskjellige IRBP-peptider, doser, tidspunkt for behandling)?
A: Absolutt. Vårt vitenskapelige team skreddersyr immuniseringsprotokoller, behandlingsplaner og endepunktsanalyser til din spesifikke legemiddelkandidat.
