| Verfügbarkeit: | |
|---|---|
| Menge: | |











Klinisch relevant – Rekapituliert die menschliche Autoimmun-Uveitis mit Th1/Th17-vermittelter Entzündung, Netzhautschädigung und Zusammenbruch der Blut-Netzhaut-Schranke.
Erweiterte Bildgebungsendpunkte – Fundusfotografie und -bewertung, optische Kohärenztomographie (OCT) zur Messung der Netzhautdicke.
Umfassende Pathologie – Histopathologie (HE-Färbung) für entzündliche Infiltration und Netzhautstrukturschäden.
Mechanismusgesteuert – IRBP aktiviert Antigen-präsentierende Zellen und treibt die Th1- und Th17-Differenzierung sowie die Produktion entzündlicher Zytokine (IFN-γ, IL-17, TNF-α) voran.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen durchgeführt werden.
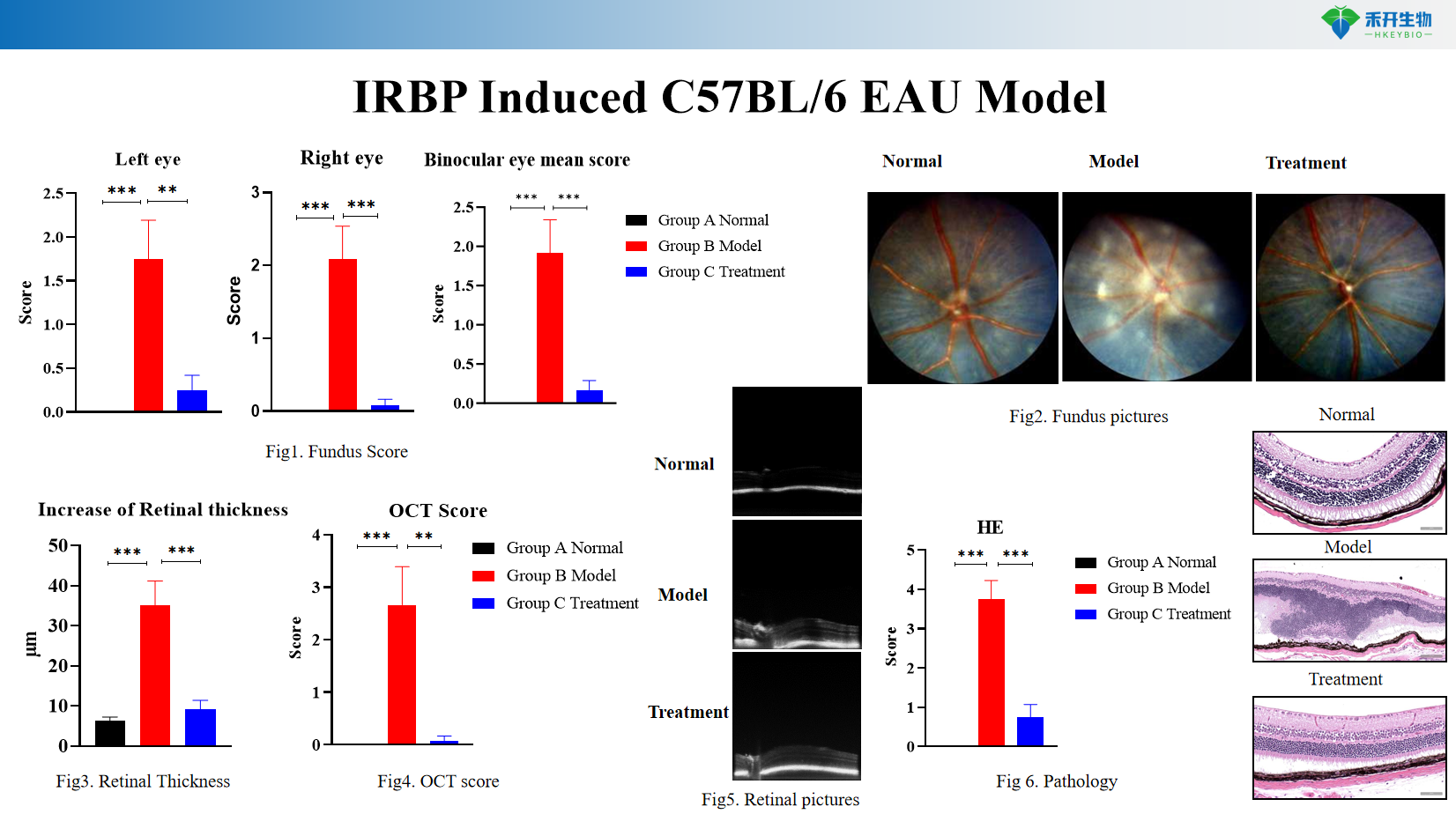
IRBP-induziertes C57BL/6 EAU-Modell
• Wirksamkeitsprüfung von Immunmodulatoren (Kortikosteroide, Methotrexat, Mycophenolat) bei Autoimmun-Uveitis
• Bewertung von Biologika, die auf Th1/Th17-Signalwege abzielen (Anti-IL-17, Anti-IL-23, Anti-IFN-γ)
• Zielvalidierung für T-Zell-vermittelte Autoimmunreaktionen im Auge
• Entdeckung von Biomarkern (entzündliche Zytokine, Marker für Netzhautschäden)
• IND-ermöglichende Pharmakologie- und Toxikologiestudien
Parameter |
Spezifikation |
Art/Stamm |
C57BL/6-Maus |
Induktionsmethode |
Subkutane Immunisierung mit IRBP-Peptid (z. B. IRBP1-20, 200–300 μg), emulgiert in CFA, ergänzt mit Mycobacterium tuberculosis, plus intraperitonealem Pertussis-Toxin (0,5–1 μg) bei der Immunisierung |
Studiendauer |
21–35 Tage nach der Impfung (Höhepunkt der Erkrankung ~14–21 Tage) |
Wichtige Endpunkte |
Fundusfotografie und klinische Bewertung (0-4-Skala für Papille, Vaskulitis, Infiltrate), optische Kohärenztomographie (OCT) zur Messung der Netzhautdicke, OCT-Bewertung, Histopathologie (HE-Färbung der Netzhaut auf entzündliche Infiltration und Strukturschäden), optional: Durchflusszytometrie von Netzhaut-/Lymphknoten-Immunzellen (CD4+ T-Zellen, Th1/Th17-Untergruppen), Zytokinanalyse (IFN-γ, IL-17, TNF-α) |
Datenpaket |
Rohdaten, Analyseberichte, Fundusbilder, OCT-Daten, histologische Objektträger, Bioinformatik (optional) Rohdaten, Analyseberichte, klinische Ergebnisse, histologische Objektträger, Serumanalyse (IL-6, CRP), optional: Anti-CII-Antikörper, Mikro-CT-Bildgebung |
F: Wie induziert IRBP EAU?
A: IRBP ist ein retinales Antigen. Die Immunisierung mit IRBP-Peptid im Adjuvans aktiviert Antigen-präsentierende Zellen, die das Antigen naiven T-Zellen präsentieren und so deren Differenzierung in pathogene Th1- und Th17-Effektoren vorantreiben. Diese Zellen dringen in das Auge ein, setzen entzündliche Zytokine (IFN-γ, IL-17, TNF-α) frei und verursachen eine Entzündung und Schädigung der Netzhaut.
F: Was sind die wichtigsten Gemeinsamkeiten mit der Autoimmun-Uveitis beim Menschen?
A: Das Modell weist eine T-Zell-vermittelte Entzündung (Th1/Th17), einen Zusammenbruch der Blut-Netzhaut-Schranke, eine entzündliche Zellinfiltration, eine Schädigung der Netzhautstruktur und klinische Anzeichen auf, die durch Fundoskopie und OCT sichtbar sind und die nicht-infektiöse Uveitis beim Menschen stark widerspiegeln.
F: Kann dieses Modell für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. verschiedene IRBP-Peptide, Dosen, Behandlungszeitpunkt)?
A: Absolut. Unser wissenschaftliches Team passt Immunisierungsprotokolle, Behandlungspläne und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
