| Disponibilidade: | |
|---|---|
| Quantidade: | |











Clinicamente relevante – Imita a dor pós-operatória humana com lesão incisional, alodinia mecânica e resposta inflamatória.
Endpoints quantificáveis – Limiar de retirada mecânica (filamentos de von Frey), pontuação de dor espontânea, assimetria de sustentação de peso, opcional: sensibilidade térmica.
Altamente reprodutível – O protocolo cirúrgico padronizado garante um comportamento consistente da dor em todos os experimentos.
Valor translacional – Ideal para testar analgésicos não opioides, AINEs, anestésicos locais e novas estratégias de controle da dor.
Pacotes de dados prontos para IND – Os estudos podem ser conduzidos de acordo com os princípios das BPL.
Modelo PSP induzido por incisão cirúrgica em C57BL/6
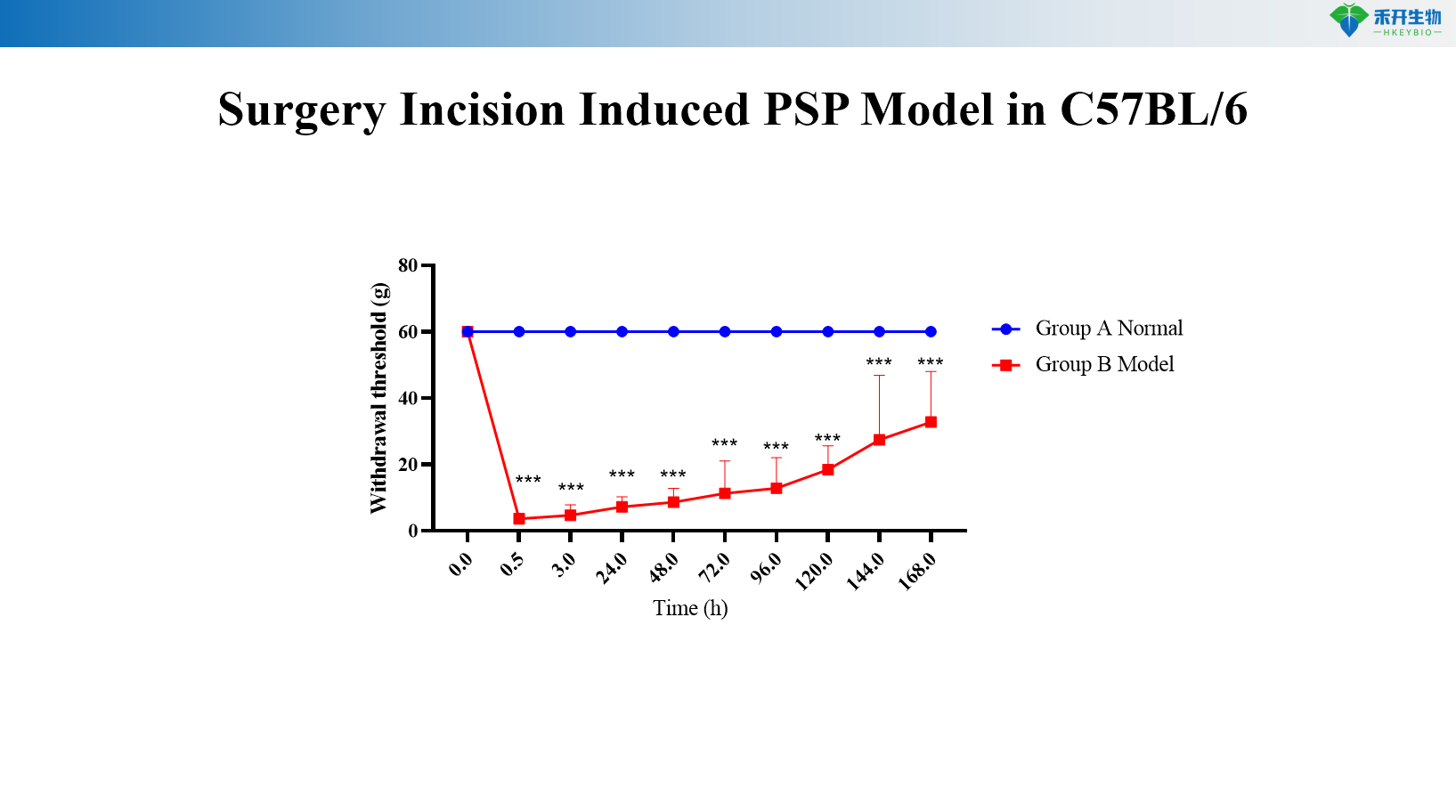
• Teste de eficácia de analgésicos não opioides (AINEs, inibidores da COX-2, paracetamol)
• Avaliação de novos analgésicos, incluindo bloqueadores dos canais de sódio, antagonistas do TRPV1 e antagonistas dos receptores de neurocinina
• Validação de alvo para vias de sensibilização periférica e central
• Descoberta de biomarcadores (mediadores inflamatórios, neuropeptídeos relacionados à dor)
• Estudos de farmacologia e toxicologia que permitem IND
Parâmetro |
Especificação |
Espécie/Estirpe |
Rato C57BL/6 |
Método de indução |
Incisão plantar (incisão longitudinal de 1 cm através da pele, fáscia e músculo da pata traseira) sob anestesia com isoflurano |
Duração do estudo |
1–14 dias (fase de dor aguda) |
Principais pontos de extremidade |
Limiar de retirada mecânica (filamentos de von Frey), pontuação de dor espontânea (proteção, lambida, levantamento), assimetria de sustentação de peso (medidor de incapacitância), opcional: hiperalgesia térmica (Hargreaves), análise de marcha, níveis de citocinas inflamatórias (ELISA/qPCR) |
| Controle positivo | AINEs (por exemplo, ibuprofeno, cetorolaco) ou gabapentina disponíveis como compostos de referência |
Pacote de dados |
Dados brutos, relatórios de análise, dados comportamentais, bioinformática (opcional) |
P: Como a incisão cirúrgica induz dor pós-operatória em ratos?
R: A incisão rompe a pele, a fáscia e os tecidos musculares, desencadeando inflamação aguda, sensibilização periférica e alterações no sistema nervoso central. Isso resulta em alodinia mecânica e comportamentos de dor espontânea que atingem o pico em horas e persistem por dias, imitando de perto a dor pós-operatória humana.
P: Quais são as principais semelhanças com a dor pós-operatória humana?
R: O modelo exibe alodinia mecânica (dor causada por estímulos normalmente não dolorosos), comportamento de defesa espontâneo e resposta inflamatória no local da incisão, todos eles características da dor pós-operatória humana.
P: Este modelo pode ser usado para estudos que habilitam o IND?
R: Sim. Os estudos podem ser conduzidos de acordo com os princípios das BPL para submissões regulatórias (FDA, EMA).
P: Vocês oferecem protocolos de estudo personalizados (por exemplo, diferentes tamanhos de incisão, tratamento preventivo versus pós-operatório)?
R: Absolutamente. Nossa equipe científica adapta protocolos de incisão, cronogramas de tratamento (preemptivo, pós-operatório) e análises de desfechos para seu medicamento candidato específico.
P: Qual é o cronograma típico para um estudo piloto de eficácia?
R: Os estudos de dor aguda são normalmente concluídos dentro de 7 dias após a incisão, com testes comportamentais no início do estudo, pós-cirurgia e vários momentos (por exemplo, 2h, 6h, 24h, 48h, 72h, 7d).
