| Verfügbarkeit: | |
|---|---|
| Menge: | |











Klinisch relevant – Imitiert den menschlichen postoperativen Schmerz mit Schnittverletzung, mechanischer Allodynie und Entzündungsreaktion.
Quantifizierbare Endpunkte – Mechanische Rückzugsschwelle (von Frey-Filamente), spontane Schmerzbewertung, Asymmetrie bei Belastung, optional: thermische Empfindlichkeit.
Hoch reproduzierbar – Das standardisierte chirurgische Protokoll gewährleistet ein konsistentes Schmerzverhalten über alle Experimente hinweg.
Translationaler Wert – Ideal zum Testen von Nicht-Opioid-Analgetika, NSAIDs, Lokalanästhetika und neuartigen Strategien zur Schmerzbehandlung.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen durchgeführt werden.
Durch chirurgische Inzision induziertes PSP-Modell in C57BL/6
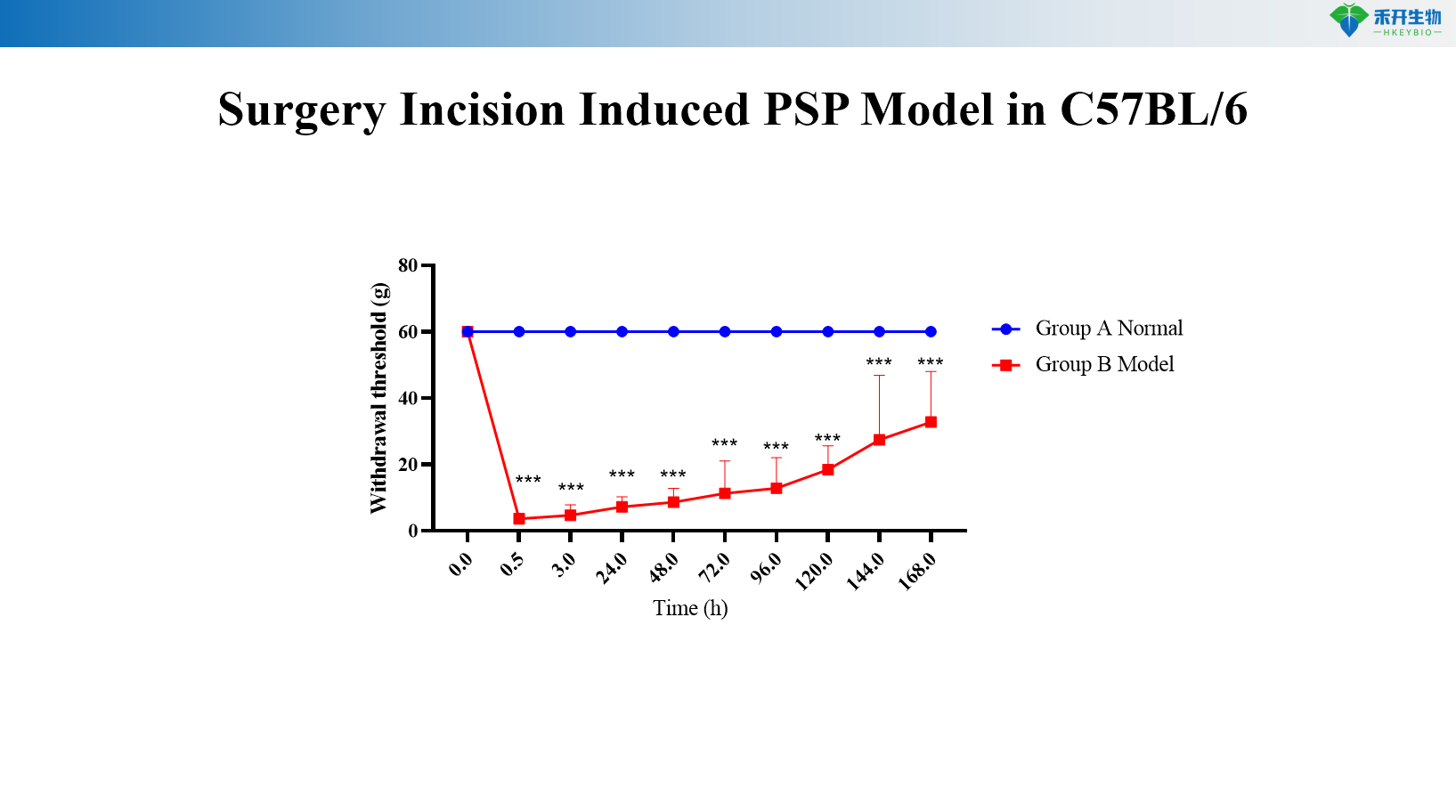
• Wirksamkeitsprüfung von Nicht-Opioid-Analgetika (NSAIDs, COX-2-Hemmer, Paracetamol)
• Bewertung neuartiger Analgetika, einschließlich Natriumkanalblockern, TRPV1-Antagonisten und Neurokininrezeptor-Antagonisten
• Zielvalidierung für periphere und zentrale Sensibilisierungswege
• Entdeckung von Biomarkern (Entzündungsmediatoren, schmerzbezogene Neuropeptide)
• IND-ermöglichende Pharmakologie- und Toxikologiestudien
Parameter |
Spezifikation |
Art/Stamm |
C57BL/6-Maus |
Induktionsmethode |
Plantarschnitt (1 cm Längsschnitt durch Haut, Faszie und Muskel der Hinterpfote) unter Isoflurananästhesie |
Studiendauer |
1–14 Tage (akute Schmerzphase) |
Wichtige Endpunkte |
Mechanische Rückzugsschwelle (von Frey-Filamente), spontane Schmerzbewertung (Schutz, Lecken, Heben), Asymmetrie der Gewichtsbelastung (Incapacitance Meter), optional: thermische Hyperalgesie (Hargreaves), Ganganalyse, inflammatorische Zytokinspiegel (ELISA/qPCR) |
| Positivkontrolle | Als Referenzverbindungen stehen NSAIDs (z. B. Ibuprofen, Ketorolac) oder Gabapentin zur Verfügung |
Datenpaket |
Rohdaten, Analyseberichte, Verhaltensdaten, Bioinformatik (optional) |
F: Wie verursacht ein chirurgischer Schnitt bei Mäusen postoperative Schmerzen?
A: Der Einschnitt zerstört Haut, Faszien und Muskelgewebe und löst akute Entzündungen, periphere Sensibilisierung und Veränderungen des Zentralnervensystems aus. Dies führt zu mechanischer Allodynie und spontanem Schmerzverhalten, das innerhalb von Stunden seinen Höhepunkt erreicht und tagelang anhält und den menschlichen postoperativen Schmerzen sehr ähnlich ist.
F: Was sind die wichtigsten Ähnlichkeiten mit postoperativen Schmerzen beim Menschen?
A: Das Modell zeigt mechanische Allodynie (Schmerzen durch normalerweise nicht schmerzhafte Reize), spontanes Schutzverhalten und eine entzündliche Reaktion an der Inzisionsstelle, allesamt Kennzeichen menschlicher postoperativer Schmerzen.
F: Kann dieses Modell für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche Schnittgrößen, präventive vs. postoperative Behandlung)?
A: Absolut. Unser wissenschaftliches Team passt Schnittprotokolle, Behandlungspläne (präventiv, postoperativ) und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
F: Wie sieht der typische Zeitplan für eine Pilot-Wirksamkeitsstudie aus?
A: Akute Schmerzstudien werden in der Regel innerhalb von 7 Tagen nach der Inzision abgeschlossen, mit Verhaltenstests zu Studienbeginn, nach der Operation und zu mehreren Zeitpunkten (z. B. 2 Stunden, 6 Stunden, 24 Stunden, 48 Stunden, 72 Stunden, 7 Tage).
