| Disponibilidad: | |
|---|---|
| Cantidad: | |











Clínicamente relevante : imita el dolor posoperatorio humano con lesión incisional, alodinia mecánica y respuesta inflamatoria.
Criterios de valoración cuantificables : umbral de retirada mecánica (filamentos de von Frey), puntuación del dolor espontáneo, asimetría en la carga de peso, opcional: sensibilidad térmica.
Altamente reproducible : el protocolo quirúrgico estandarizado garantiza un comportamiento consistente del dolor en todos los experimentos.
Valor traslacional : ideal para probar analgésicos no opioides, AINE, anestésicos locales y nuevas estrategias de manejo del dolor.
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
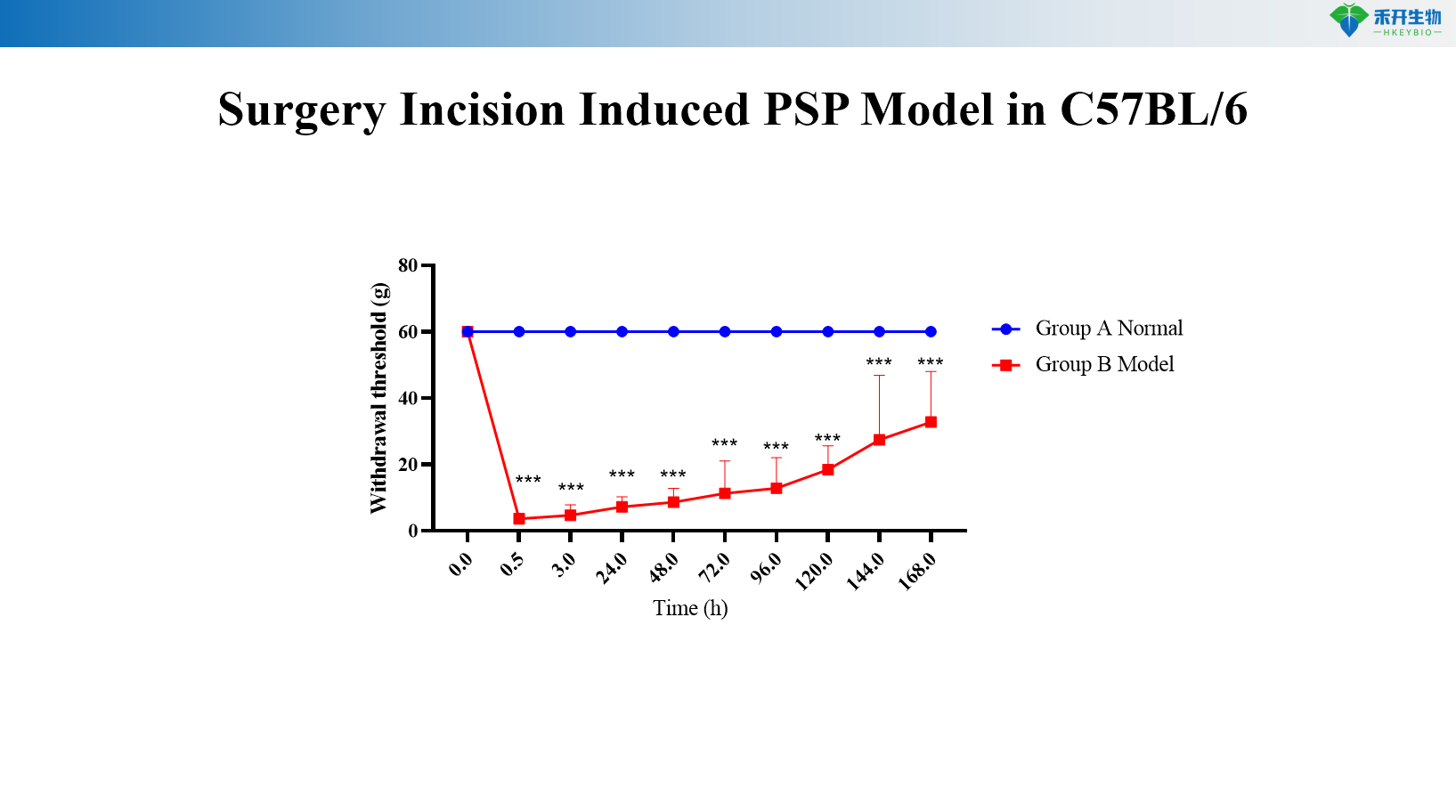
Modelo PSP inducido por incisión quirúrgica en C57BL/6
• Pruebas de eficacia de analgésicos no opioides (AINE, inhibidores de la COX-2, acetaminofén)
• Evaluación de nuevos analgésicos, incluidos bloqueadores de los canales de sodio, antagonistas de TRPV1 y antagonistas de los receptores de neuroquinina.
• Validación de objetivos para vías de sensibilización periférica y central.
• Descubrimiento de biomarcadores (mediadores inflamatorios, neuropéptidos relacionados con el dolor)
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Especificación |
Especie/Cepa |
Ratón C57BL/6 |
Método de inducción |
Incisión plantar (incisión longitudinal de 1 cm a través de la piel, la fascia y el músculo de la pata trasera) bajo anestesia con isoflurano |
Duración del estudio |
1 a 14 días (fase de dolor agudo) |
Puntos finales clave |
Umbral de retirada mecánica (filamentos de von Frey), puntuación del dolor espontáneo (guardar, lamer, levantar), asimetría de carga (medidor de incapacitancia), opcional: hiperalgesia térmica (Hargreaves), análisis de la marcha, niveles de citocinas inflamatorias (ELISA/qPCR) |
| control positivo | AINE (p. ej., ibuprofeno, ketorolaco) o gabapentina disponibles como compuestos de referencia |
Paquete de datos |
Datos brutos, informes de análisis, datos de comportamiento, bioinformática (opcional) |
P: ¿Cómo induce la incisión quirúrgica el dolor posoperatorio en ratones?
R: La incisión altera la piel, la fascia y los tejidos musculares, provocando inflamación aguda, sensibilización periférica y alteraciones del sistema nervioso central. Esto da como resultado alodinia mecánica y comportamientos espontáneos de dolor que alcanzan su punto máximo en cuestión de horas y persisten durante días, imitando fielmente el dolor posoperatorio humano.
P: ¿Cuáles son las similitudes clave con el dolor posoperatorio humano?
R: El modelo exhibe alodinia mecánica (dolor debido a estímulos que normalmente no son dolorosos), comportamiento protector espontáneo y respuesta inflamatoria en el sitio de la incisión, todos los cuales son características distintivas del dolor posoperatorio humano.
P: ¿Se puede utilizar este modelo para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes tamaños de incisión, tratamiento preventivo versus postoperatorio)?
R: Absolutamente. Nuestro equipo científico adapta los protocolos de incisión, los programas de tratamiento (preventivo, posoperatorio) y los análisis de criterios de valoración a su fármaco candidato específico.
P: ¿Cuál es el cronograma típico para un estudio piloto de eficacia?
R: Los estudios de dolor agudo generalmente se completan dentro de los 7 días posteriores a la incisión, con pruebas de comportamiento al inicio, después de la cirugía y en múltiples momentos (p. ej., 2 h, 6 h, 24 h, 48 h, 72 h, 7 días).
