| Verfügbarkeit: | |
|---|---|
| Menge: | |











Regulatorischer Goldstandard – TDAR wird von FDA, EMA und ICH S8 als Immunfunktionstest erster Wahl zur Immuntoxizitätsbewertung empfohlen.
Umfassende Immunbewertung Quantifizierbare Endpunkte – KLH-spezifische IgM- und IgG-Titer; B-Zell-Phänotypisierung (prozentuale und absolute Anzahl); primäre und sekundäre Reaktionskinetik.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen für behördliche Einreichungen durchgeführt werden.
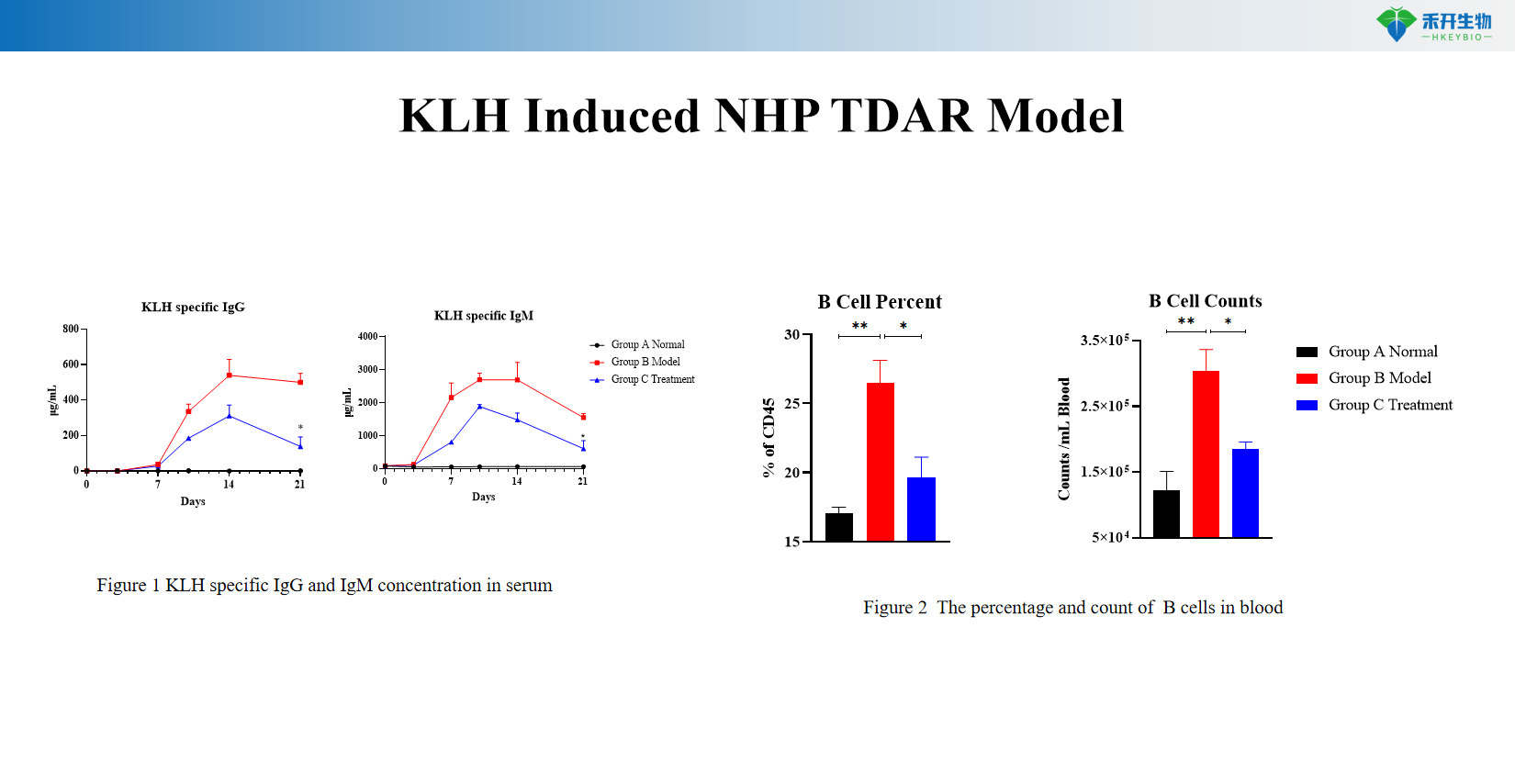
Repräsentative Daten aus unserem KLH-induzierten NHP-TDAR-Modell:
KLH-induziertes NHP-TDAR-Modell
• Bewertung der Immuntoxizität kleiner Moleküle, Biologika und Immunmodulatoren
• IND-fähige Studien, die eine Bewertung der Immunfunktion erfordern (ICH S8-Konformität)
• Wirkmechanismusstudien für immunsuppressive oder immunstimulierende Medikamente
• Bewertung des Impfstoff-Adjuvans
• Biomarker-Entdeckung für Immunkompetenz
Parameter |
Spezifikation |
Spezies |
Javaneraffe ( Macaca fascicularis ) |
Induktionsmethode |
Immunisierung mit Schlüssellochnapfschnecken-Hämocyanin (KLH), typischerweise mit adjuvanter, intramuskulärer oder subkutaner Verabreichung |
Studiendauer |
4–8 Wochen (Bewertung des primären und sekundären Ansprechens) |
Wichtige Endpunkte |
KLH-spezifisches IgM (Tag 7–14), KLH-spezifisches IgG (Tag 14–28), B-Zell-Phänotypisierung (Prozentsatz und absolute Anzahl), optional: T-Zell-Untergruppen, Zytokin-Profilierung |
Datenpaket |
Rohdaten, Analyseberichte, Durchflusszytometriedateien, Bioinformatik (optional) |
F: Warum gilt TDAR als Goldstandard für die Immuntoxizitätsbewertung?
A: TDAR integriert mehrere Komponenten der adaptiven Immunität (Antigenpräsentation, T-Zell-Hilfe, B-Zell-Aktivierung, Antikörperproduktion) in einem einzigen Funktionstest. Regulatorische Richtlinien (ICH S8, FDA, EMA) empfehlen TDAR als Immunfunktionstest erster Wahl.
F: Warum KLH als Antigen verwenden?
A: KLH ist ein hochimmunogenes Protein, das weder Menschen noch Labortieren zuvor ausgesetzt wurde. Dadurch wird sichergestellt, dass die gemessenen Antikörperreaktionen spezifisch für die Immunisierung sind und nicht durch eine bereits bestehende Immunität verfälscht werden.
F: Kann dieses Modell für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen durchgeführt werden, um behördliche Einreichungen (FDA, EMA) zu unterstützen und die ICH S8-Anforderungen an Immuntoxizitätstests zu erfüllen.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. verschiedene Adjuvanzien, Zeitpunkt der Impfungen)?
A: Absolut. Unser wissenschaftliches Team passt Immunisierungspläne, Adjuvansauswahl und Endpunktanalysen an Ihren spezifischen Arzneimittelkandidaten und die behördlichen Anforderungen an.
