| Verfügbarkeit: | |
|---|---|
| Menge: | |











Klinisch relevant – Rekapituliert menschliches KOA: Knorpeldegeneration, Gelenkschwellung und schmerzbedingtes Verhalten.
Quantifizierbare Endpunkte – Körpergewicht, Kniegelenkbreite (Messung der Dicke), Fußlastverteilung (Belastungsasymmetrie), Knorpelmatrix-Färbungsscore (Safranin O/Fast Green), Histopathologie (HE, Toluidinblau).
Mechanismusgesteuert – MIA hemmt die Chondrozyten-Glykolyse, induziert Apoptose und einen fortschreitenden Knorpelabbau und ahmt die metabolischen und strukturellen Veränderungen bei Arthrose nach.
Translationaler Wert – Ideal zum Testen von krankheitsmodifizierenden Osteoarthritis-Medikamenten (DMOADs), Analgetika (NSAIDs, Opioide) und entzündungshemmenden Mitteln.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen durchgeführt werden.
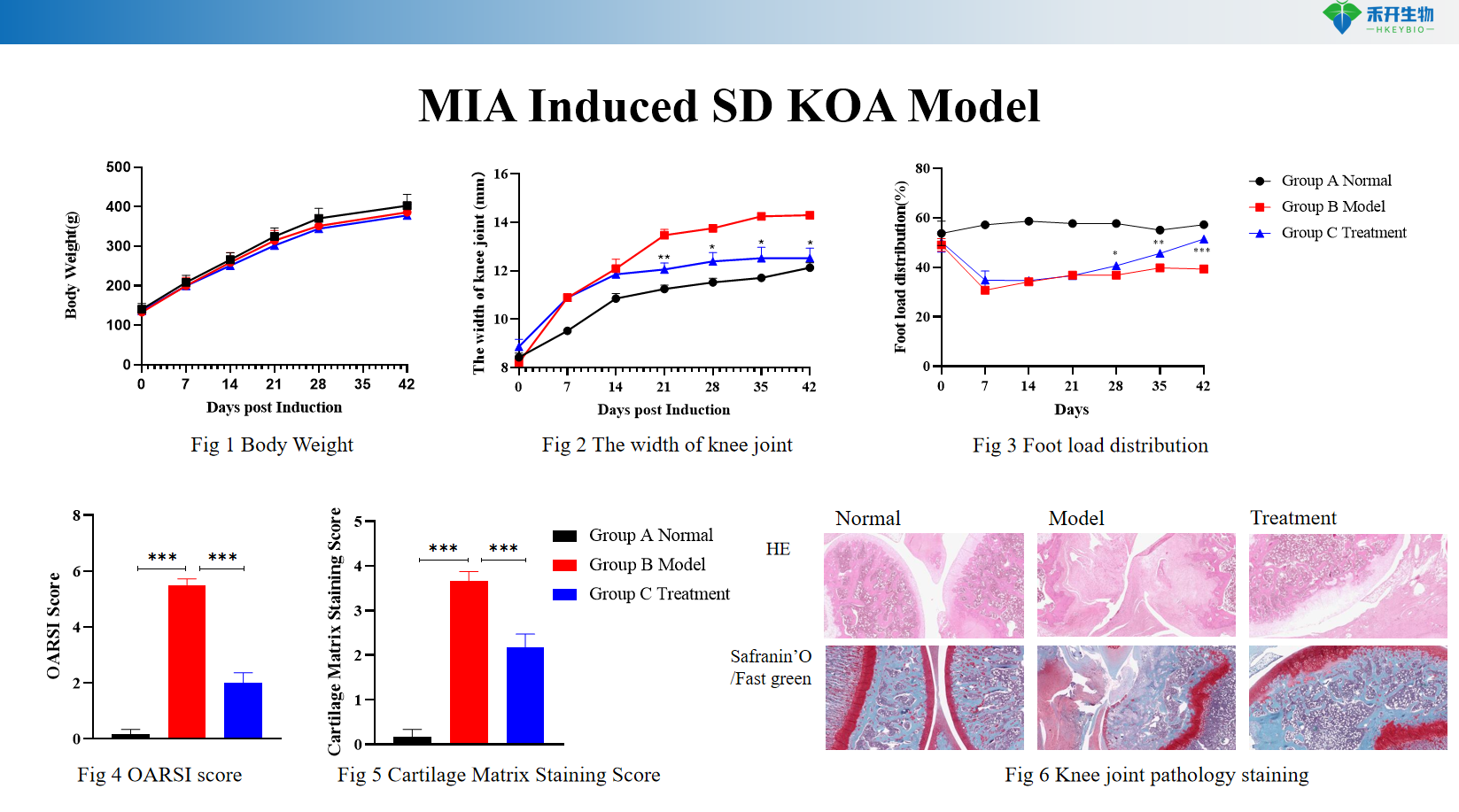
MIA-induziertes SD-KOA-Modell
• Wirksamkeitstests von krankheitsmodifizierenden Osteoarthritis-Medikamenten (DMOADs), einschließlich Cathepsin-K-Inhibitoren, Wnt-Signalweg-Modulatoren und anabolen Wirkstoffen
• Bewertung von Analgetika (NSAIDs, COX-2-Hemmer, Opioide, Cannabinoide) bei Arthroseschmerzen
• Zielvalidierung für Knorpelabbau und Schmerzpfade
• Biomarker-Entdeckung (Knorpelabbaumarker, Entzündungsmediatoren)
• IND-ermöglichende Pharmakologie- und Toxikologiestudien
Parameter |
Spezifikation |
Art/Stamm |
Sprague-Dawley (SD)-Ratte |
Induktionsmethode |
Intraartikuläre Injektion von Monoiodacetat (MIA, 1–3 mg in 50 μL Kochsalzlösung) in das Kniegelenk |
Studiendauer |
1–8 Wochen (akute bis chronische Phasen) |
Wichtige Endpunkte |
Körpergewicht, Kniegelenksbreite (Caliper), Fußlastverteilung (Belastungsasymmetrie), Knorpelmatrix-Färbungsscore (Safranin O/Fast Green), Histopathologie (HE, Toluidinblau, OARSI-Score), optional: mechanische Allodynie (von Frey), Ganganalyse, Serumbiomarker (COMP, CTX-II) |
| Positivkontrolle | Als Referenzverbindungen stehen NSAIDs (z. B. Indomethacin) oder DMOADs zur Verfügung |
Datenpaket |
Rohdaten, Analyseberichte, histologische Objektträger, Verhaltensdaten, Bioinformatik (optional) |
F: Wie löst MIA Arthrose aus?
A: Monoiodacetat (MIA) hemmt die Glycerinaldehyd-3-phosphat-Dehydrogenase, ein Schlüsselenzym bei der Glykolyse, was zu einer Störung des Chondrozyten-Stoffwechsels und zur Apoptose führt. Dies löst einen fortschreitenden Knorpelabbau, subchondrale Knochenveränderungen und ein Schmerzverhalten aus, das der Arthrose des Menschen sehr ähnlich ist.
F: Was sind die wichtigsten Gemeinsamkeiten mit der menschlichen Knie-Arthrose?
A: Das Modell weist Knorpelmatrixverlust, Gelenkschwellung, veränderte Gewichtsbelastung und histopathologische Veränderungen (Flimmern, Chondrozytenverlust, subchondrale Knochensklerose) auf, was der menschlichen KOA-Pathologie und schmerzbedingten Funktionsdefiziten sehr ähnlich ist.
F: Kann dieses Modell für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche MIA-Dosen, prophylaktische vs. therapeutische Dosierung)?
A: Absolut. Unser wissenschaftliches Team passt MIA-Dosen, Behandlungspläne und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
F: Wie sieht der typische Zeitplan für eine Pilot-Wirksamkeitsstudie aus?
A: Akute Schmerzstudien können in 1–2 Wochen abgeschlossen sein; Chronische Strukturstudien erfordern typischerweise 4–8 Wochen nach der MIA-Injektion.
