| Disponibilité : | |
|---|---|
| Quantité : | |











Large gamme de modèles – Modèles d'analogues d'haptène, de cytokines, d'allergènes et de vitamine D couvrant les endotypes de MA aigus, chroniques et à dominante Th2/Th17/Th22.
Plusieurs espèces/souches – BALB/c (à tendance Th2), C57BL/6 (à tendance Th1/Th17) et rat SD disponibles.
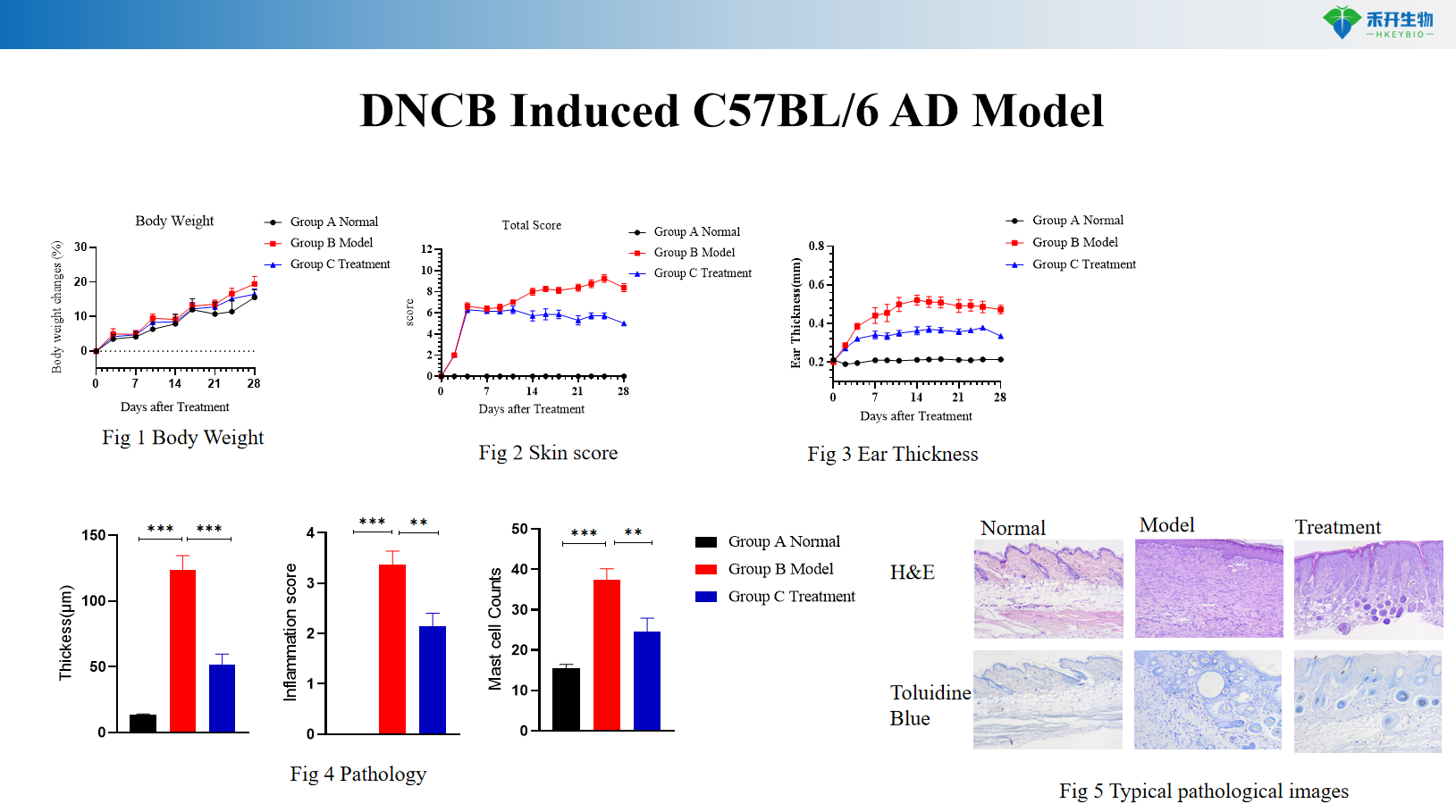
Critères d'évaluation complets : poids corporel, épaisseur de l'oreille, score cutané, démangeaisons, IgE sériques, profilage des cytokines (IL-4, IL-13, IL-17, IL-36), histopathologie (HE, bleu de toluidine), épaisseur de l'épiderme.
Valeur translationnelle – Idéal pour tester les inhibiteurs de JAK, les produits biologiques (anti‑IL‑4Rα, anti‑IL‑13), les inhibiteurs de la PDE4 et les agents topiques.
Ensembles de données prêts pour l'IND – Les études peuvent être menées conformément aux principes BPL.
Modèle C57BL/6 AD induit par DNCB
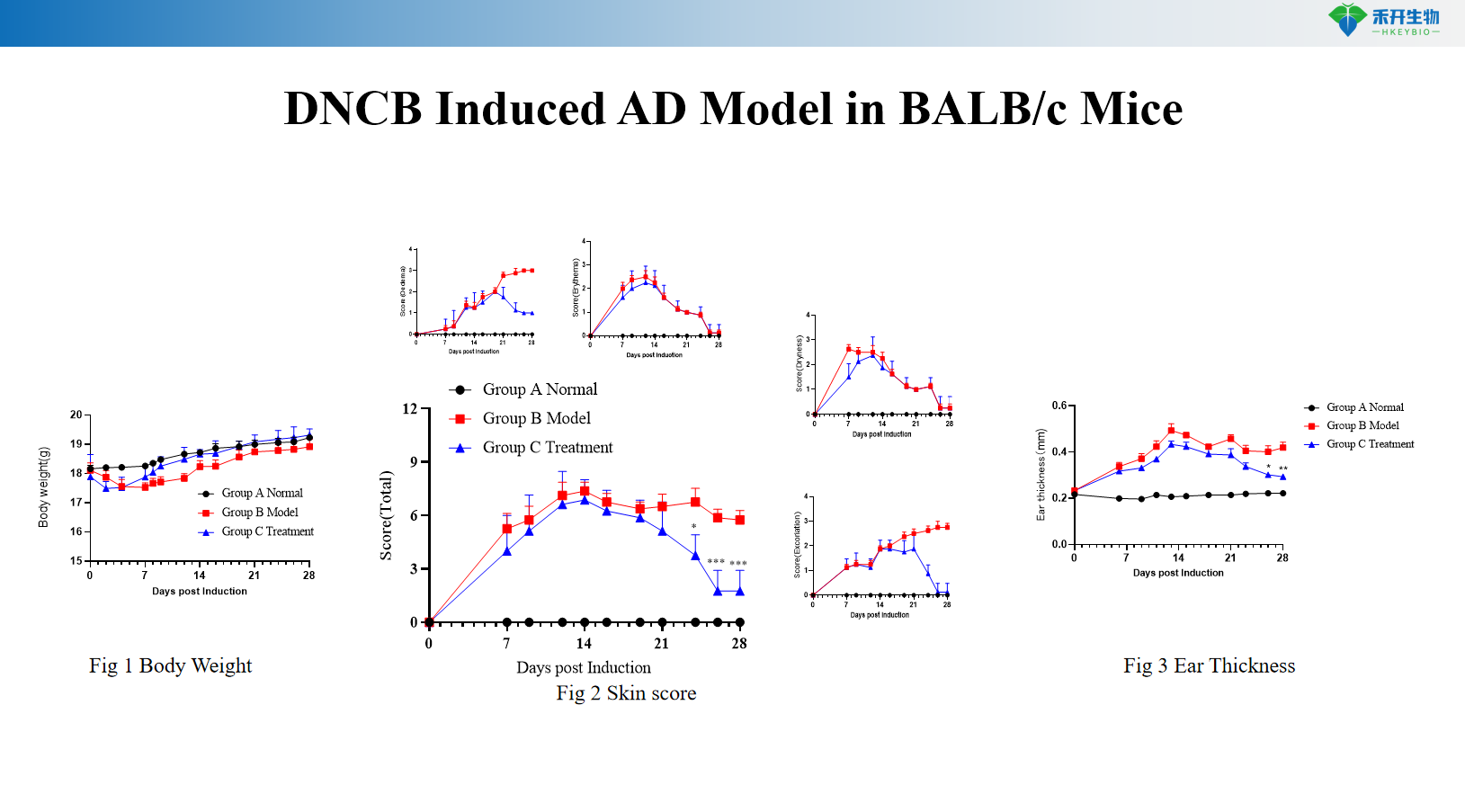
Modèle AD induit par le DNCB chez les souris BALB/c
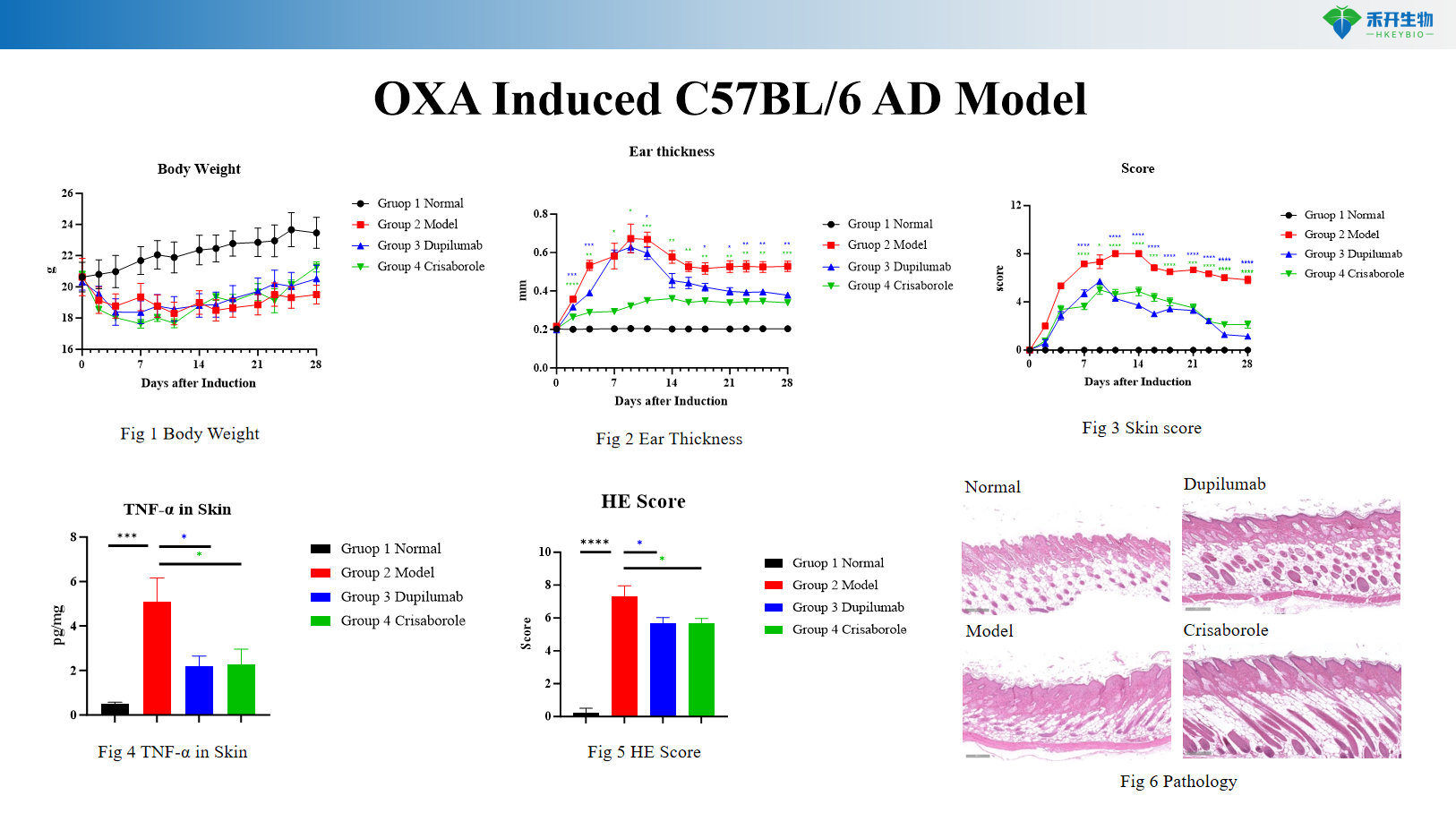
Modèle C57BL/6 AD induit par OXA
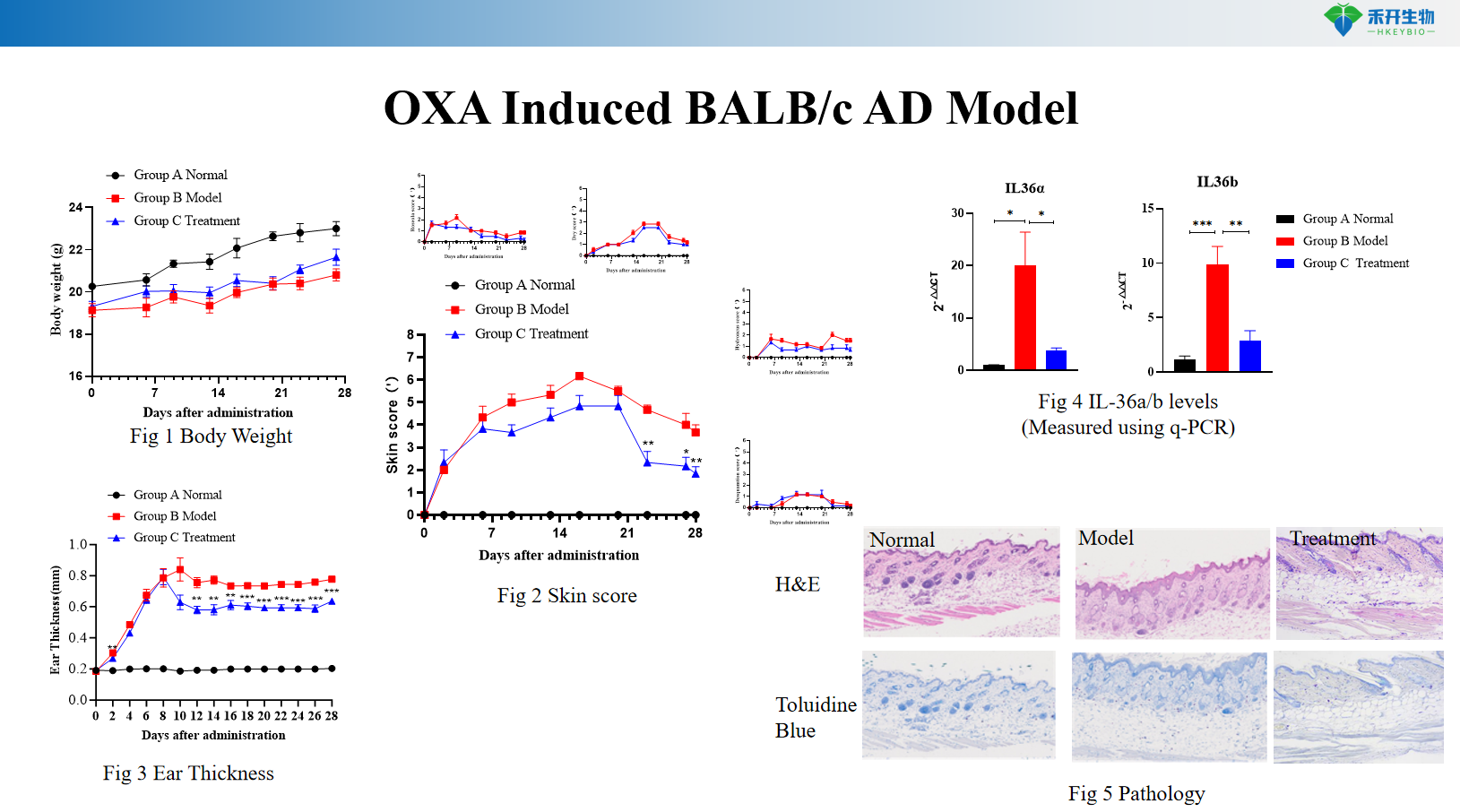
Modèle BALB/c AD induit par OXA
Modèle MC903 induit C57BL/6 AD

Modèle BALB/c AD induit MC903


Modèle AD induit par MC903 et OXA dans BALB/c

Modèle BALB/c AD induit par FITC
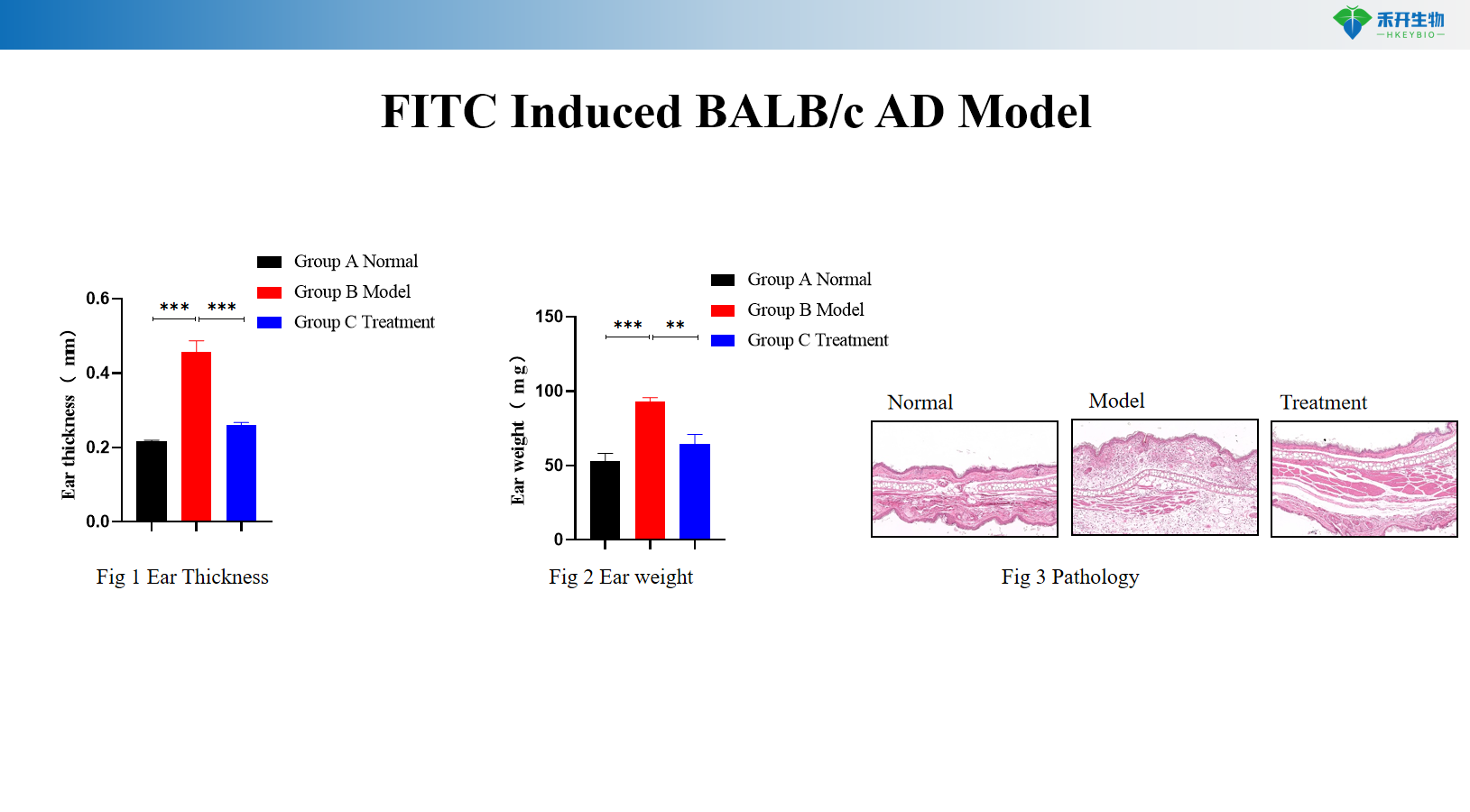
Modèle BALB/c AD induit par DNFB+OVA
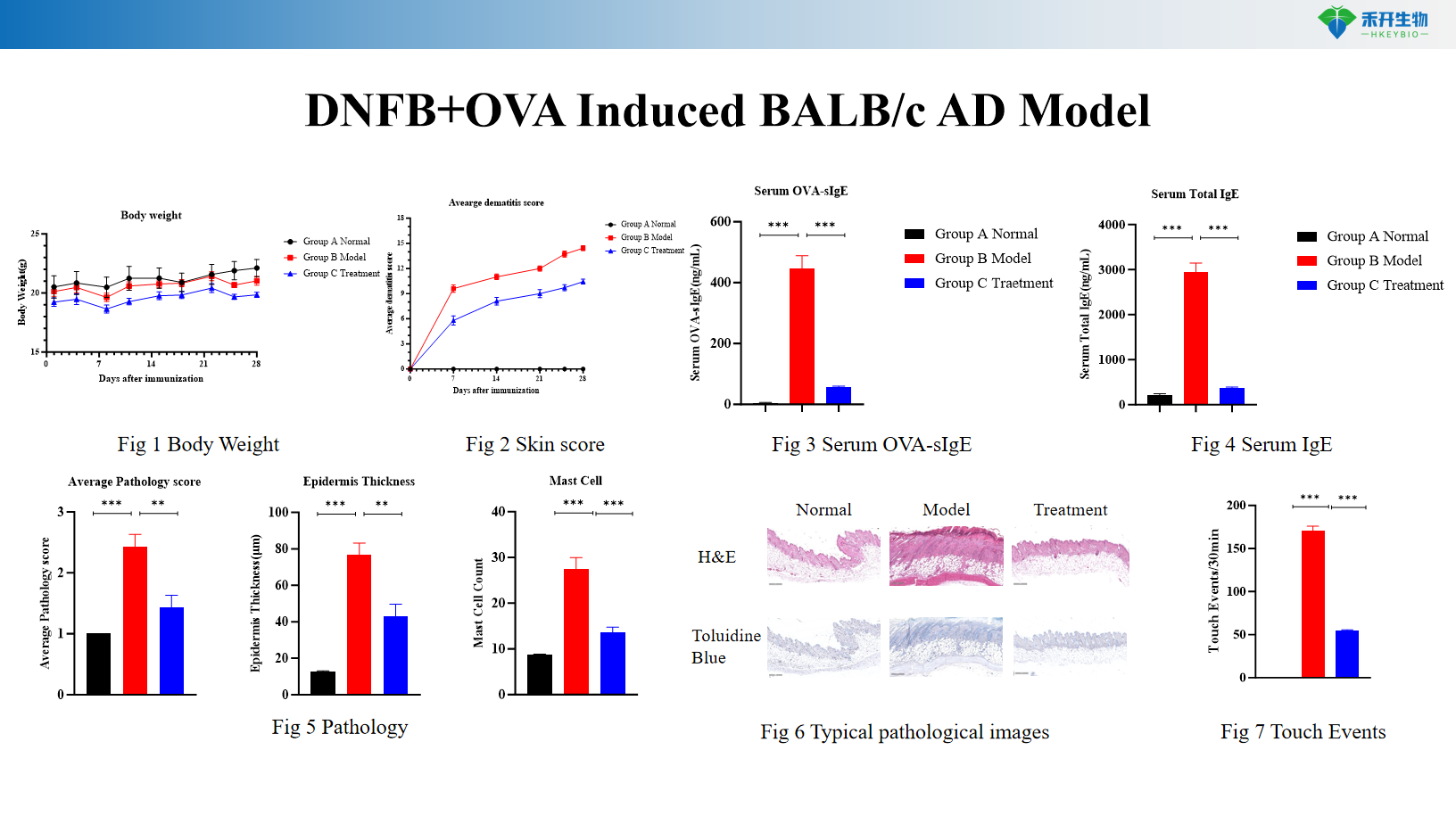
Modèle BALB/c AD induit par l’IL-33
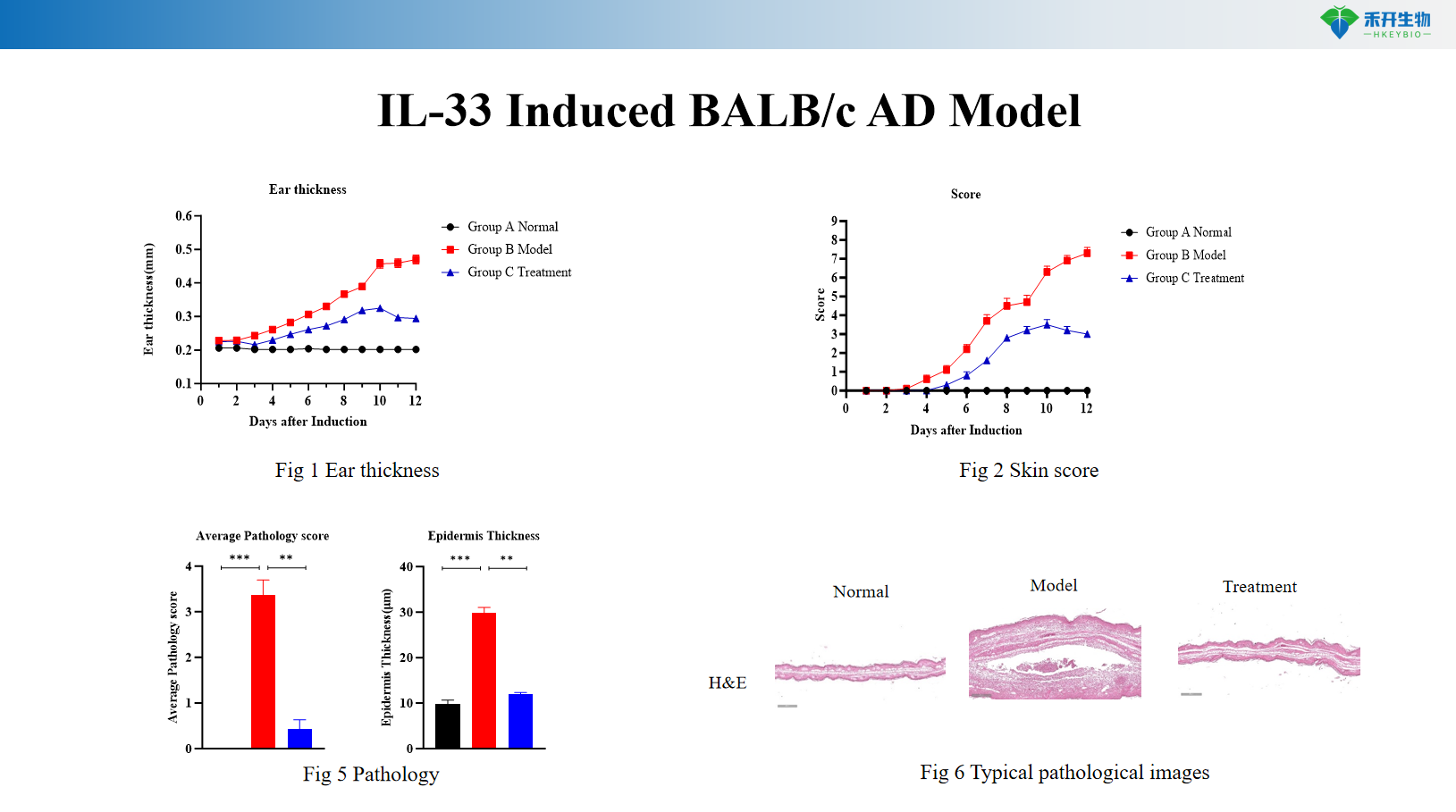
Modèle AD induit par l'IL-36 chez les souris C57BL/6
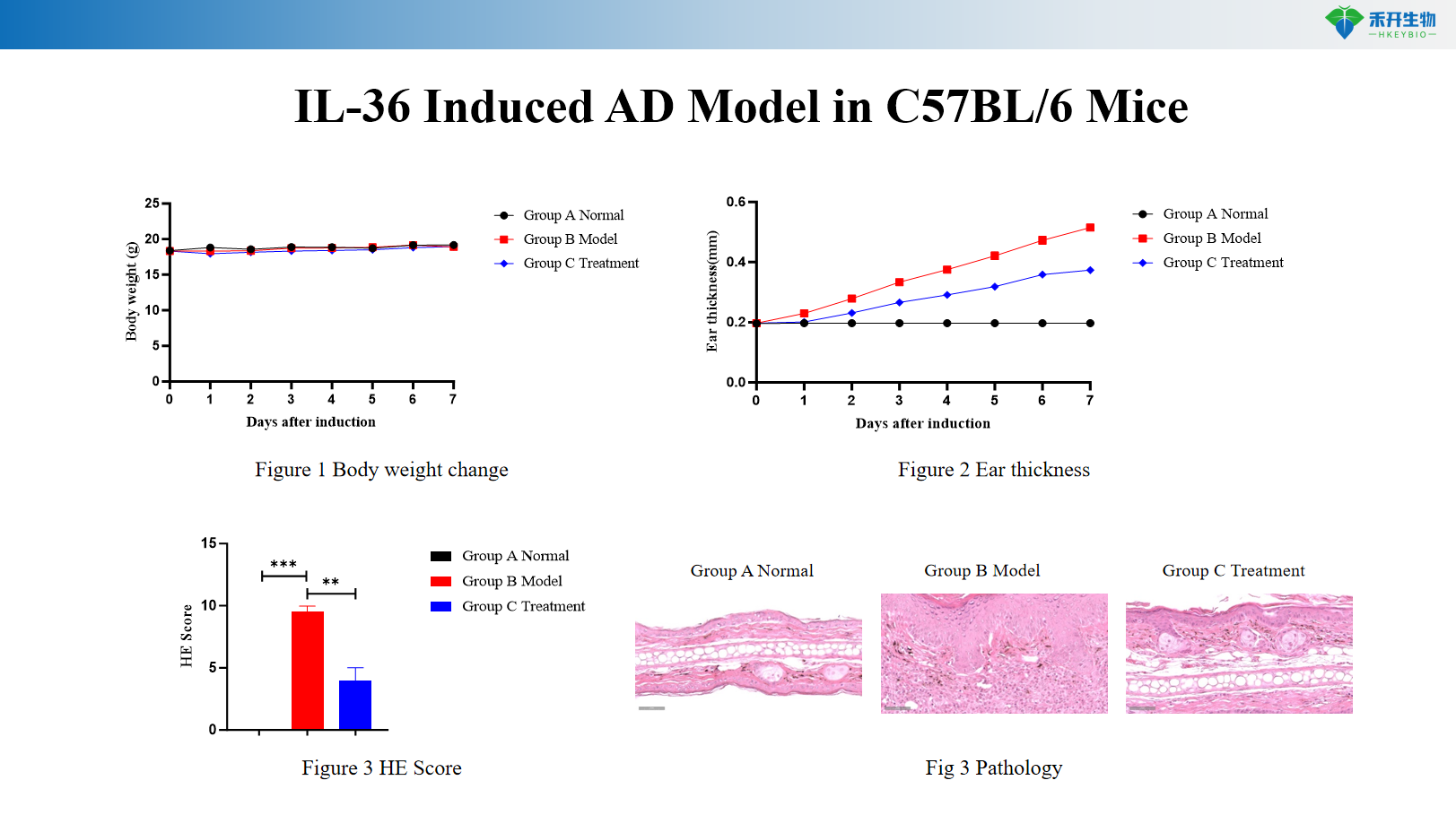
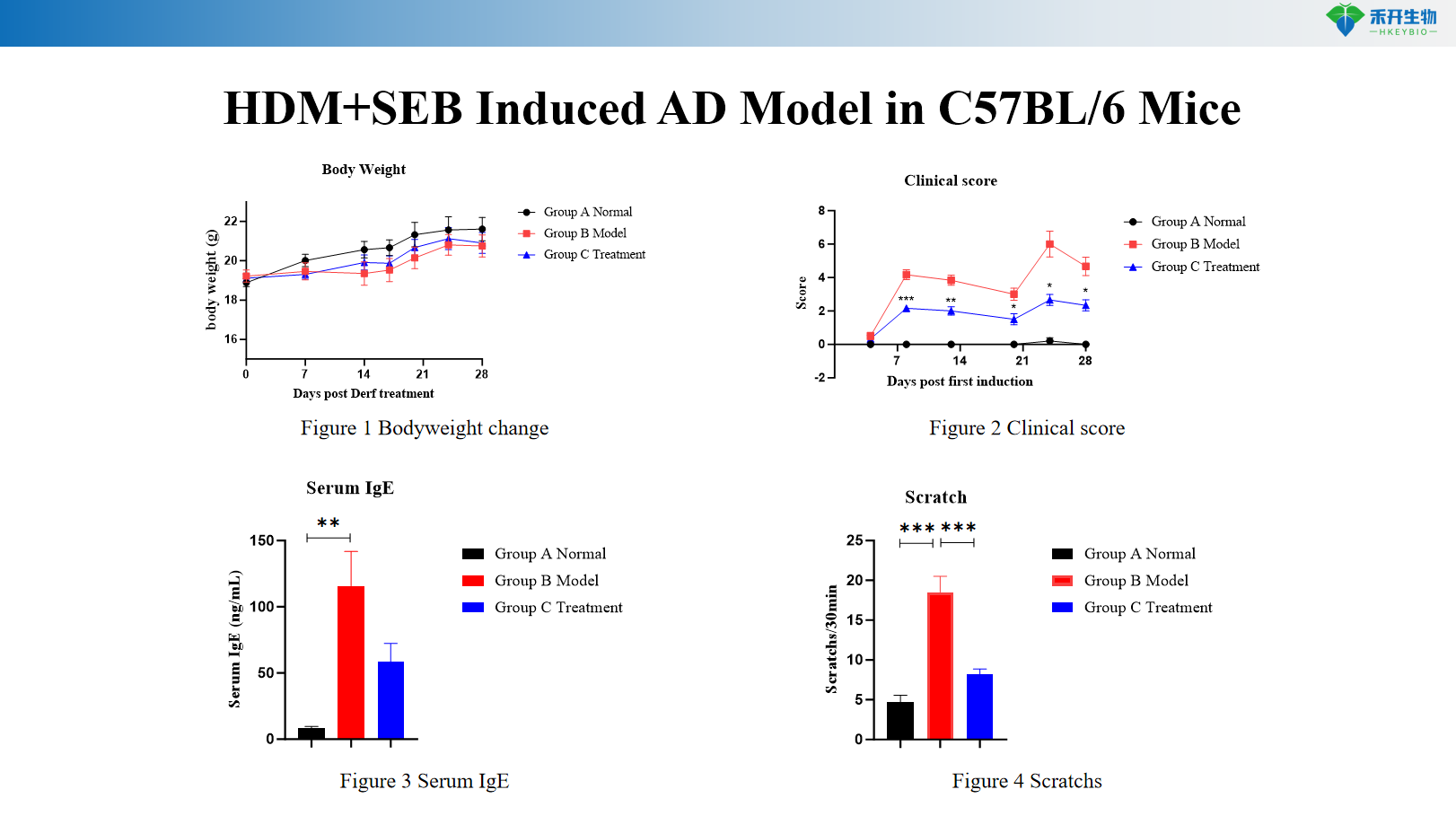
Modèle AD induit par HDM+SEB chez des souris C57BL/6
• Tests d'efficacité des thérapies topiques et systémiques contre la MA (inhibiteurs de JAK, inhibiteurs de PDE4, produits biologiques ciblant l'IL-4/13, l'IL-31, l'IL-33, le TSLP)
• Validation des cibles pour les voies Th2, Th17, Th22 et démangeaisons
• Découverte de biomarqueurs (IgE, signatures de cytokines, protéines de la barrière cutanée)
• Études sur le mécanisme d'action (MOA)
• Études pharmacologiques et toxicologiques permettant l'IND
Paramètre |
Spécification |
Espèce/souche |
Souris (BALB/c, C57BL/6) ; Rat (SD) |
Méthode d'induction |
Haptènes (DNCB, OXA, DNFB+OVA, FITC), analogue de la vitamine D (MC903), cytokines (IL-33, IL-36), allergènes (HDM+SEB), combinaisons (MC903+OXA) |
Durée des études |
7 à 28 jours (selon le modèle) |
Points de terminaison clés |
Poids corporel, épaisseur de l'oreille, score clinique cutané, démangeaisons (grattage), IgE totales sériques et IgE spécifiques de l'antigène, taux de cytokines (IL-4, IL-13, IL-17, IL-36, TNF-α), histopathologie (H&E, bleu de toluidine), épaisseur de l'épiderme, infiltration de cellules immunitaires (FACS/IHC) |
Paquet de données |
Données brutes, rapports d'analyses, photographies cliniques, lames histologiques, fichiers de cytométrie en flux, bioinformatique (facultatif) |
Q : Comment puis-je choisir le bon modèle AD pour mon candidat-médicament ?
R : Tenez compte du mécanisme de votre médicament : les produits biologiques ciblant les Th2 (par exemple, les anti-IL-4Rα) sont mieux évalués dans les modèles haptène ou MC903 ; Les composés liés au Th17 peuvent convenir aux modèles IL-36 ou HDM+SEB. Les souris BALB/c présentent des réponses Th2 plus fortes, tandis que les C57BL/6 présentent des profils Th1/Th17 plus équilibrés. Notre équipe scientifique peut guider la sélection de modèles en fonction de votre cible spécifique.
Q : Ces modèles peuvent-ils être utilisés pour des études permettant l’IND ?
R : Oui. Les études peuvent être menées conformément aux principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différents schémas posologiques, thérapies combinées) ?
R : Absolument. Notre équipe scientifique adapte les protocoles d’induction, les programmes de traitement et les analyses des paramètres à votre candidat-médicament spécifique.
Q : Quel est le calendrier typique d’une étude pilote d’efficacité ?
R : La plupart des modèles AD se terminent en 2 à 4 semaines, y compris les phases de sensibilisation/provocation et de traitement. Les délais spécifiques dépendent du choix du modèle et des points finaux.
