| Dostępność: | |
|---|---|
| Ilość: | |











Szerokie portfolio modeli – modele haptenów, cytokin, alergenów i analogów witaminy D obejmujące ostre, przewlekłe i endotypy AD z dominacją Th2/Th17/Th22.
Dostępnych jest wiele gatunków/szczepów – BALB/c (podatny na Th2), C57BL/6 (podatny na Th1/Th17) i szczur SD.
Kompleksowe punkty końcowe – masa ciała, grubość ucha, ocena skóry, zdarzenia swędzące, IgE w surowicy, profilowanie cytokin (IL-4, IL-13, IL-17, IL-36), histopatologia (HE, błękit toluidynowy), grubość naskórka.
Wartość translacyjna – idealny do testowania inhibitorów JAK, leków biologicznych (anty-IL-4Rα, anty-IL-13), inhibitorów PDE4 i środków do stosowania miejscowego.
Pakiety danych gotowe do IND – Badania mogą być prowadzone zgodnie z zasadami GLP.
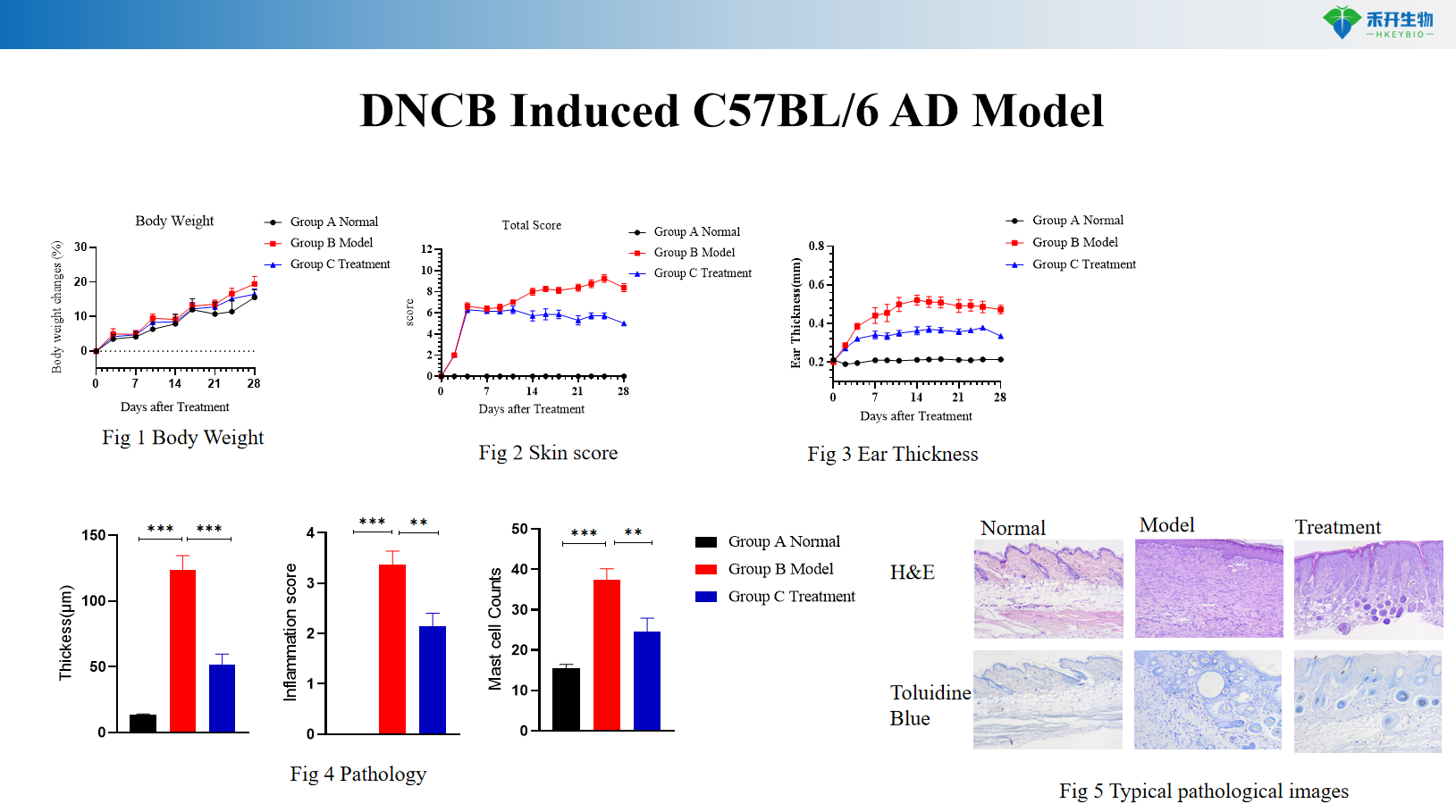
Model C57BL/6 AD indukowany DNCB
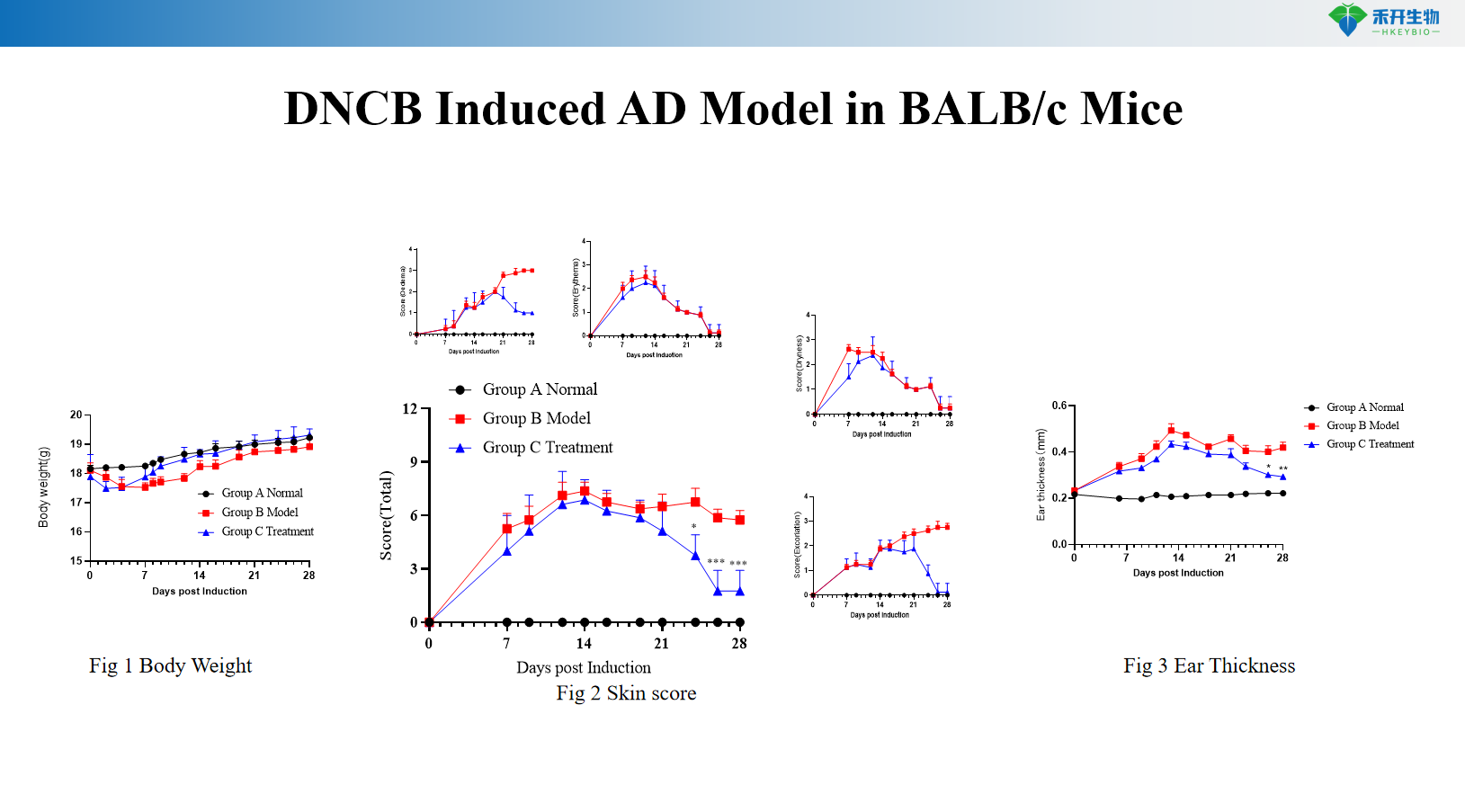
Model AD indukowany DNCB u myszy BALB/c
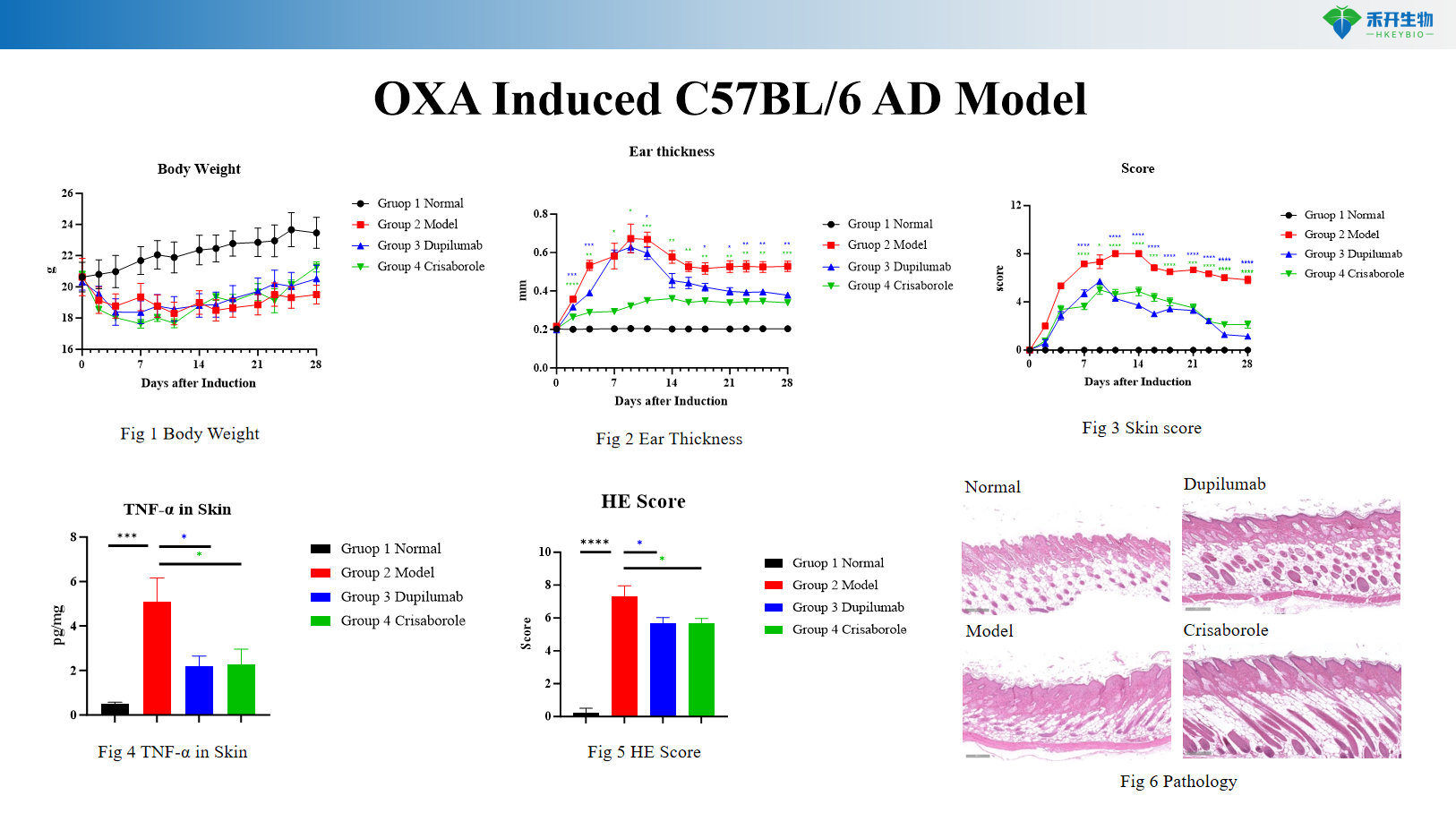
Model C57BL/6 AD indukowany OXA
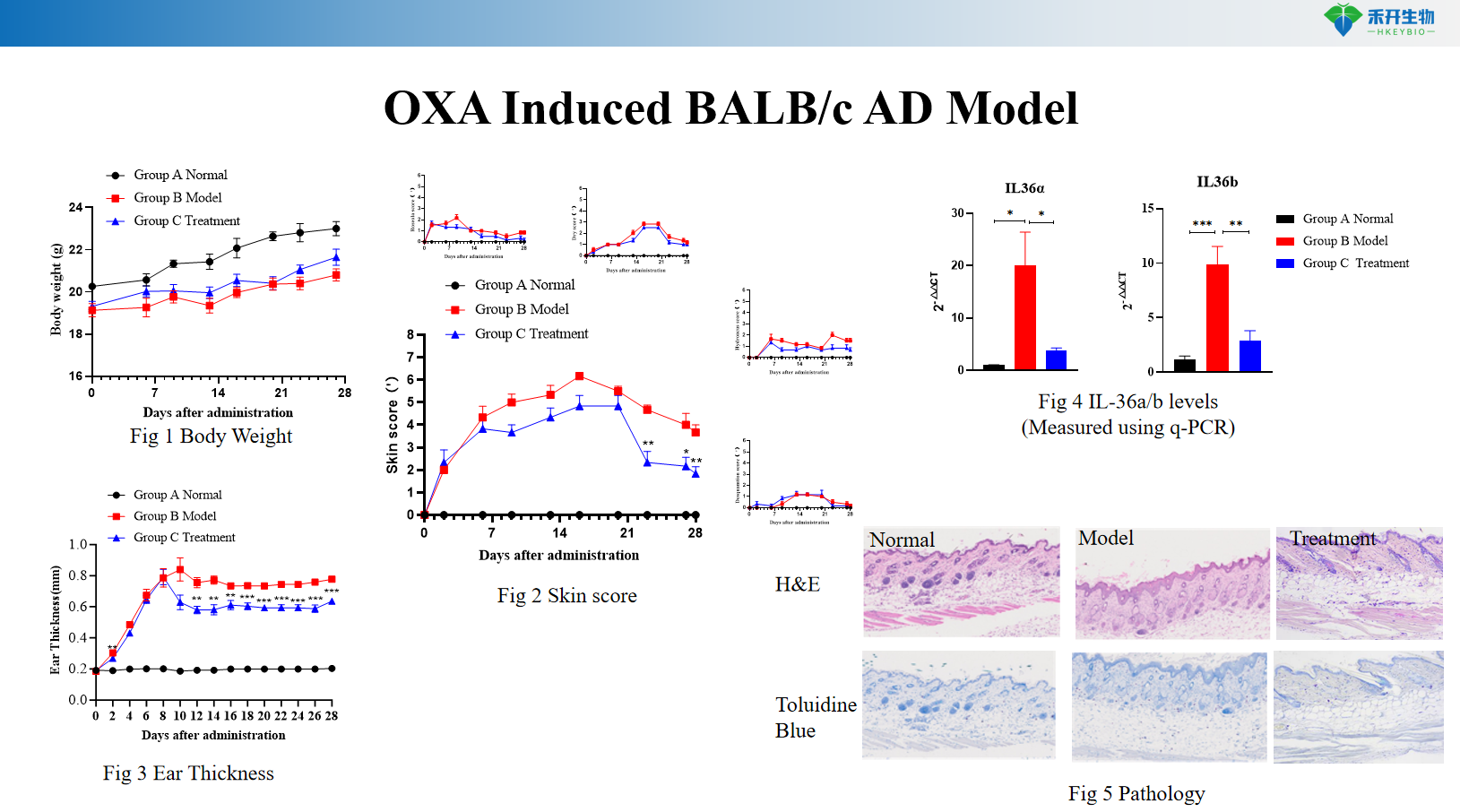
Model AD BALB/c indukowany OXA
Model MC903 indukowany C57BL/6 AD

Model MC903 z indukowanym BALB/c AD


Model AD indukowany MC903 i OXA w BALB/c

Model AD BALB/c indukowany FITC
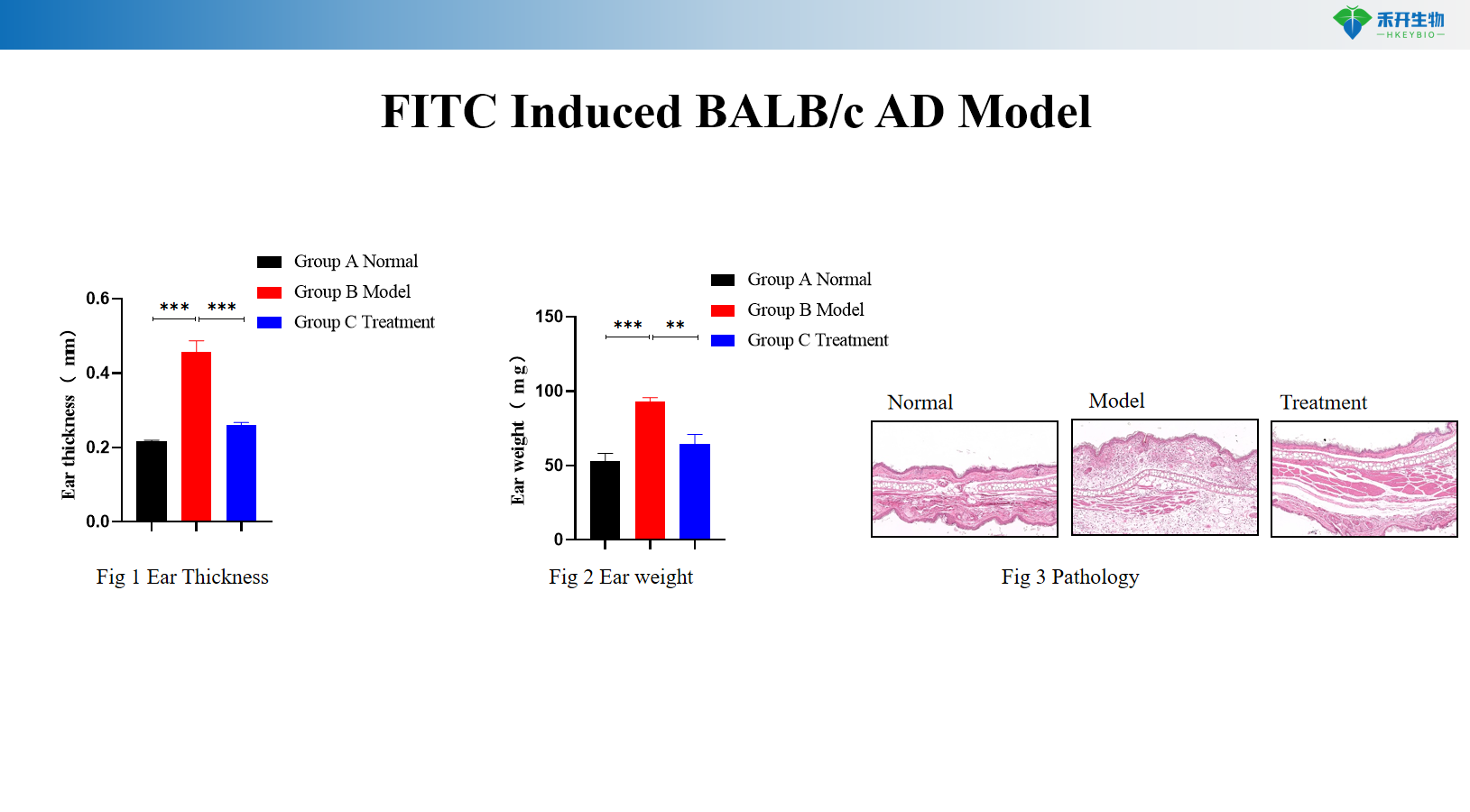
Model AD BALB/c indukowanego DNFB+OVA
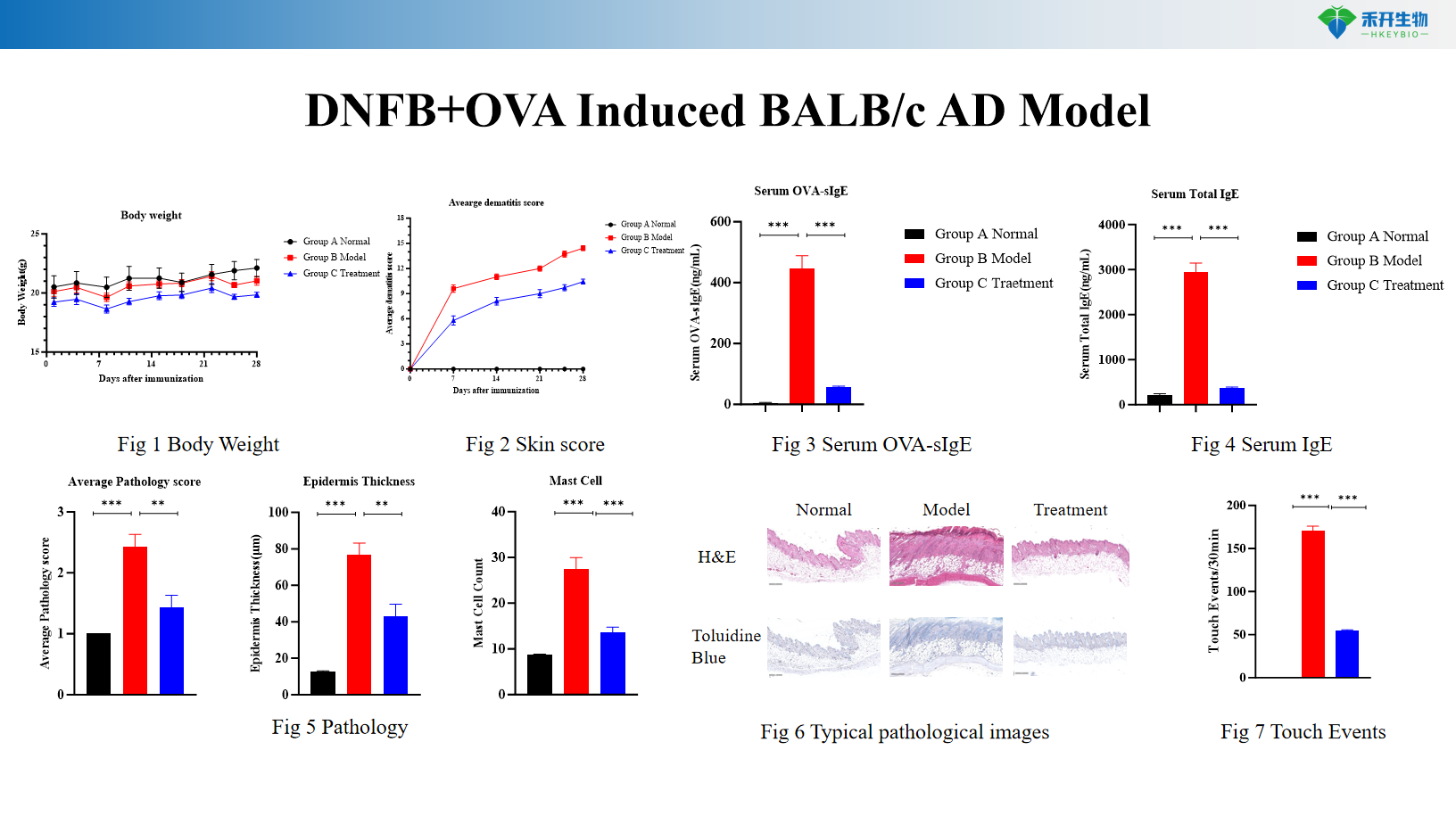
Model AD indukowanego IL-33 BALB/c
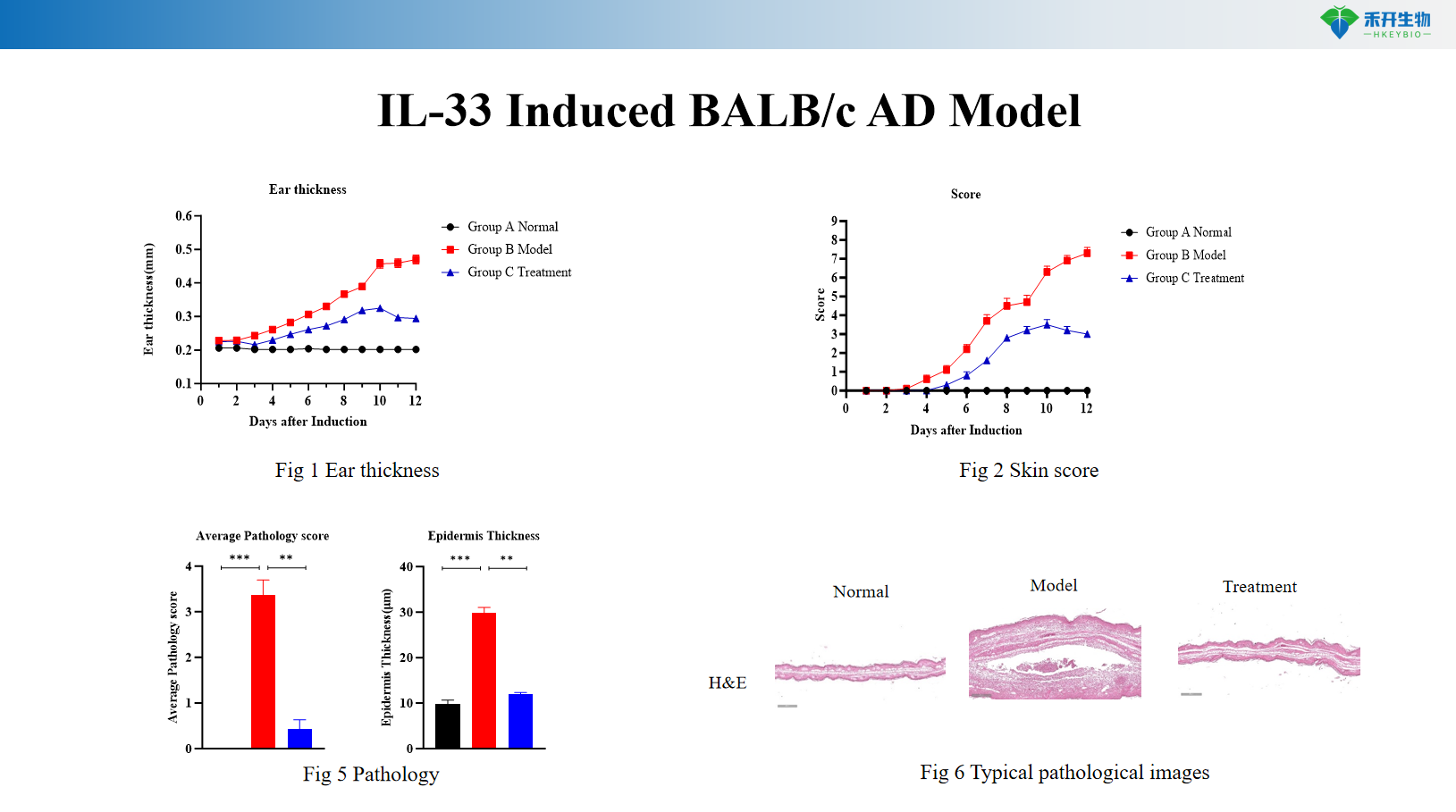
Model AD indukowanej IL-36 u myszy C57BL/6
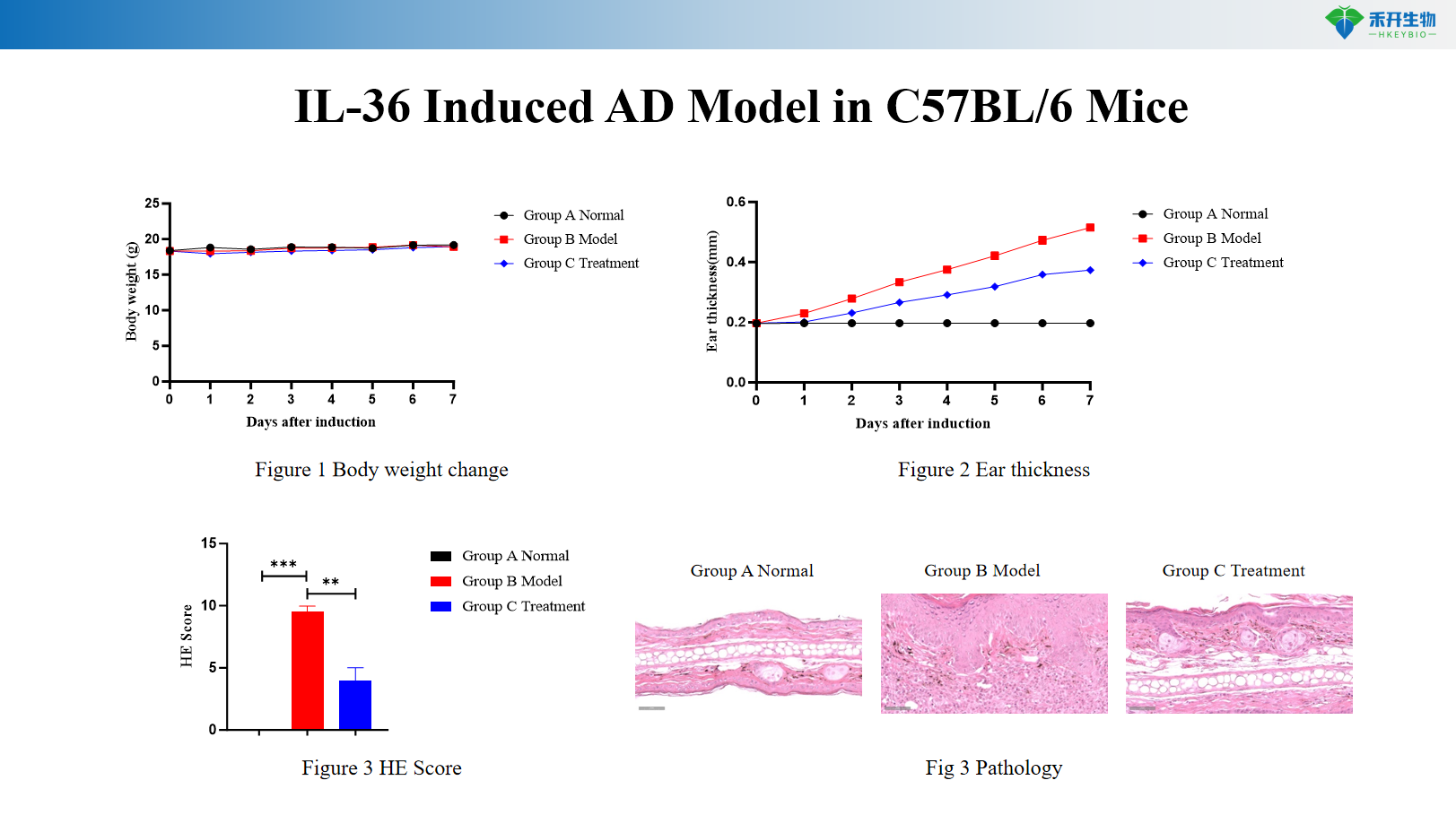
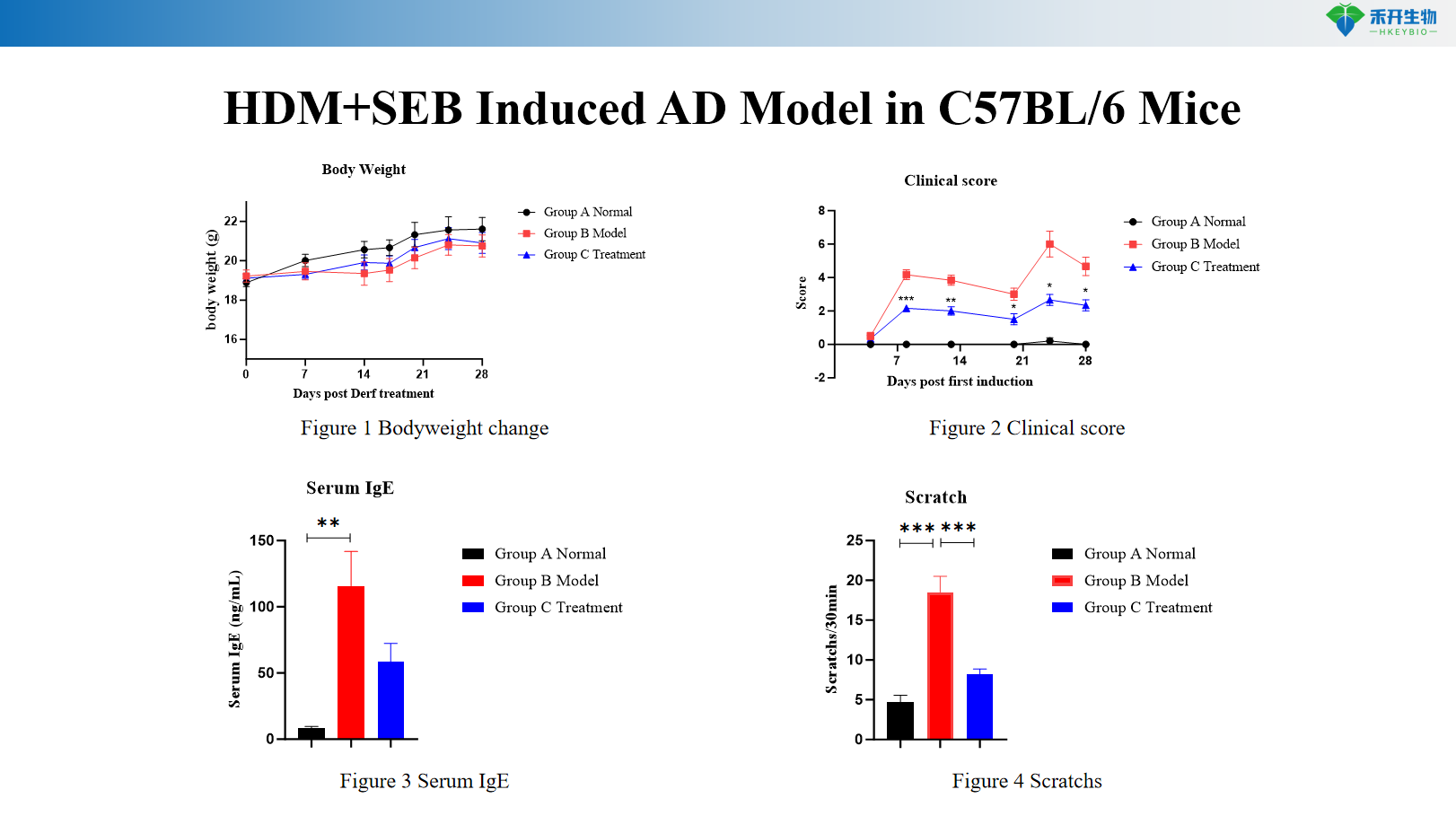
Model AD indukowany HDM+SEB u myszy C57BL/6
• Testowanie skuteczności terapii miejscowych i ogólnoustrojowych AD (inhibitory JAK, inhibitory PDE4, leki biologiczne ukierunkowane na IL-4/13, IL-31, IL-33, TSLP)
• Docelowa walidacja dla Th2, Th17, Th22 i szlaków swędzenia
• Odkrycie biomarkerów (IgE, sygnatury cytokin, białka bariery skórnej)
• Badania mechanizmu działania (MOA).
• IND umożliwiające badania farmakologiczne i toksykologiczne
Parametr |
Specyfikacja |
Gatunek/szczep |
Mysz (BALB/c, C57BL/6); Szczur (SD) |
Metoda indukcyjna |
Hapteny (DNCB, OXA, DNFB+OVA, FITC), analog witaminy D (MC903), cytokiny (IL-33, IL-36), alergeny (HDM+SEB), kombinacje (MC903+OXA) |
Czas trwania nauki |
7–28 dni (w zależności od modelu) |
Kluczowe punkty końcowe |
Masa ciała, grubość ucha, ocena kliniczna skóry, zdarzenia swędzące (drapanie), całkowite IgE w surowicy i IgE specyficzne dla antygenu, poziomy cytokin (IL-4, IL-13, IL-17, IL-36, TNF-α), histopatologia (H&E, błękit toluidynowy), grubość naskórka, naciek komórek odpornościowych (FACS/IHC) |
Pakiet danych |
Surowe dane, raporty z analiz, zdjęcia kliniczne, preparaty histologiczne, pliki cytometrii przepływowej, bioinformatyka (opcjonalnie) |
P: Jak wybrać odpowiedni model AD dla mojego kandydata na lek?
Odp.: Weź pod uwagę mechanizm działania swojego leku: leki biologiczne ukierunkowane na Th2 (np. anty-IL-4Rα) najlepiej oceniać w modelach haptenu lub MC903; Związki pokrewne Th17 mogą być odpowiednie dla modeli IL-36 lub HDM+SEB. Myszy BALB/c wykazują silniejsze odpowiedzi Th2, podczas gdy C57BL/6 wykazują bardziej zrównoważone profile Th1/Th17. Nasz zespół naukowy może pomóc w wyborze modelu w oparciu o konkretny cel.
P: Czy te modele można wykorzystać do badań umożliwiających IND?
O: Tak. Badania można przeprowadzić zgodnie z zasadami GLP dotyczącymi zgłoszeń regulacyjnych (FDA, EMA).
P: Czy oferujecie dostosowane protokoły badań (np. różne schematy dawkowania, terapie skojarzone)?
O: Absolutnie. Nasz zespół naukowy dostosowuje protokoły indukcji, harmonogramy leczenia i analizy punktów końcowych do konkretnego kandydata na lek.
P: Jaki jest typowy harmonogram pilotażowego badania skuteczności?
Odp.: Większość modeli AD kończy się w ciągu 2–4 tygodni, włączając etapy uwrażliwiania/prowokacji i leczenia. Konkretne ramy czasowe zależą od wyboru modelu i punktów końcowych.
