| Disponibilité : | |
|---|---|
| Quantité : | |











Cliniquement pertinent – récapitule la SSc-ILD humaine avec fibrose pulmonaire, fibrose cutanée et pathologie médiée par le TGF-β.
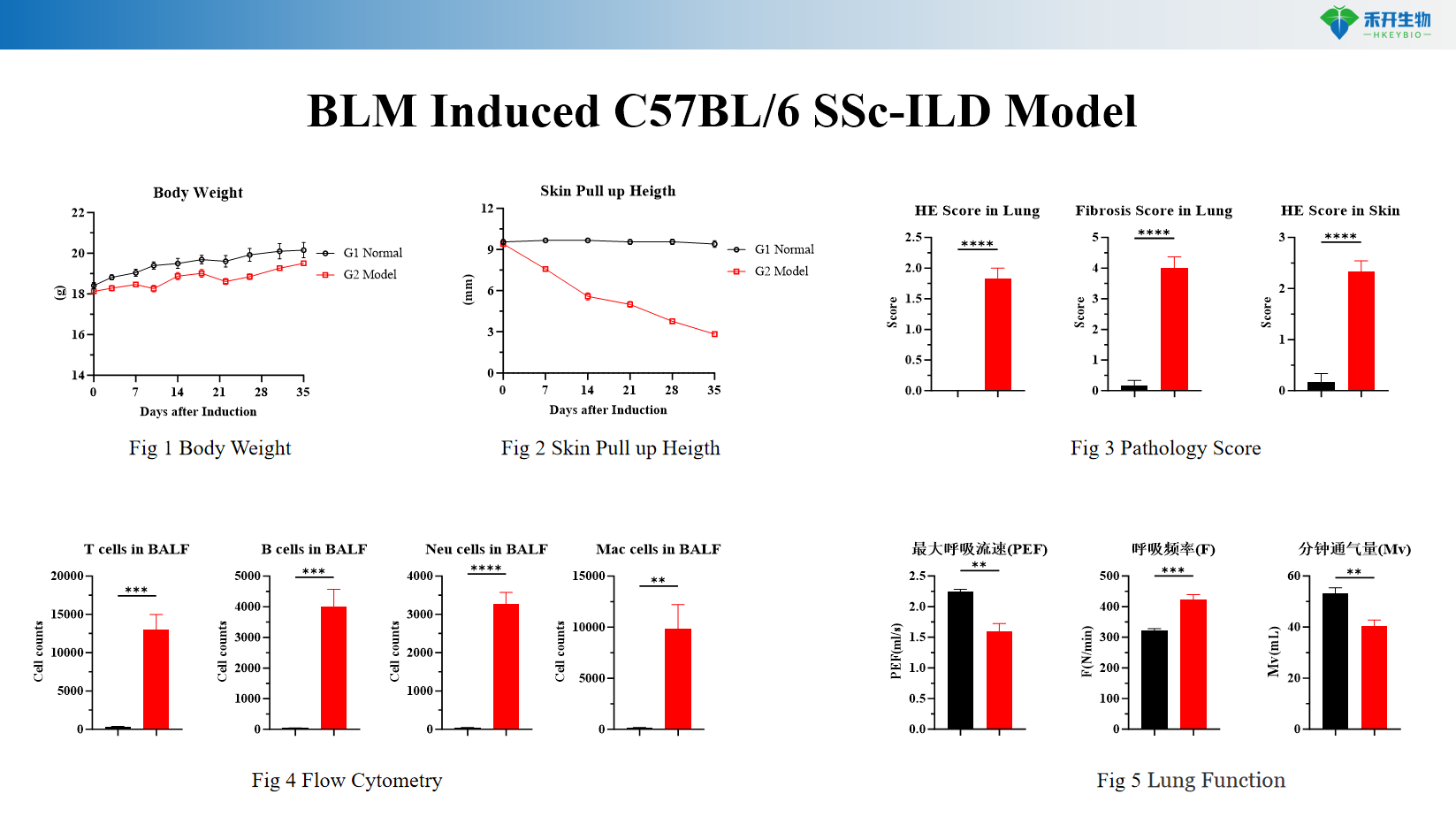
Critères d'évaluation complets : poids corporel, hauteur de traction cutanée (fibrose cutanée), fonction pulmonaire, cytométrie en flux (infiltration de cellules immunitaires), histopathologie pulmonaire (coloration HE et Masson).
Axé sur un mécanisme – Le BLM induit des dommages à l’ADN, un stress oxydatif et l’activation de la voie TGF-β, reflétant la pathogenèse humaine de la SSc-ILD.
Valeur translationnelle – Idéal pour tester les agents antifibrotiques (nintedanib, pirfénidone), les inhibiteurs du TGF-β et les immunomodulateurs.
Ensembles de données prêts pour l'IND – Les études peuvent être menées conformément aux principes BPL.
Modèle C57BL/6 SSc-ILD induit par BLM
• Tests d'efficacité des agents antifibrotiques (nintédanib, pirfénidone, inhibiteurs du TGF-β, inhibiteurs de la galectine-3)
• Évaluation d'immunomodulateurs ciblant l'inflammation et la fibrose
• Validation de cibles pour la signalisation du TGF-β et les voies fibrotiques
• Découverte de biomarqueurs (marqueurs de collagène, médiateurs inflammatoires, signatures de cellules immunitaires)
• Études pharmacologiques et toxicologiques permettant l'IND
Paramètre |
Spécification |
Espèce/souche |
Souris C57BL/6 |
Méthode d'induction |
Instillation intratrachéale de bléomycine (BLM, 1 à 2 U/kg) dans une solution saline, dose unique |
Durée des études |
14 à 28 jours (développement d'une fibrose) |
Points de terminaison clés |
Poids corporel, hauteur de traction cutanée (fibrose cutanée), fonction pulmonaire (observance, résistance), cytométrie en flux (infiltration de cellules immunitaires : macrophages, neutrophiles, cellules T), histopathologie pulmonaire (coloration HE et trichrome de Masson avec score d'Ashcroft), en option : teneur en hydroxyproline, nombre de cellules BALF, taux de cytokines |
| Contrôle positif | Nintedanib ou pirfénidone disponibles comme composés antifibrotiques de référence |
Paquet de données |
Données brutes, rapports d'analyses, données de fonction pulmonaire, fichiers de cytométrie en flux, lames histologiques (HE, Masson), bioinformatique (facultatif) |
Q : Comment la bléomycine induit-elle la SSc-ILD chez la souris ?
R : La bléomycine intratrachéale déclenche des dommages à l'ADN et un stress oxydatif dans le tissu pulmonaire, entraînant une inflammation persistante, l'activation de la voie de signalisation TGF-β et un dépôt excessif de matrice extracellulaire, imitant à la fois la fibrose cutanée et pulmonaire observée dans la SSc-ILD humaine.
Q : Quelles sont les principales similitudes avec la SSc-ILD humaine ?
R : Le modèle présente une fibrose pulmonaire progressive (coloration HE et Masson), un déclin de la fonction pulmonaire, une fibrose cutanée et une infiltration de cellules immunitaires, reflétant étroitement la pathologie humaine SSc-ILD.
Q : Ce modèle peut-il être utilisé pour des études permettant l’IND ?
R : Oui. Les études peuvent être menées conformément aux principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différentes doses de BLM, calendrier de traitement, combinaison avec d'autres agents) ?
R : Absolument. Notre équipe scientifique adapte les protocoles d’induction, les programmes de traitement et les analyses des paramètres à votre candidat-médicament spécifique.
Q : Quel est le calendrier typique d’une étude pilote d’efficacité ?
R : Les études pilotes se déroulent généralement 21 à 28 jours après l'instillation du BLM, avec une fibrose se développant sur 14 à 21 jours et un traitement administré pendant ou après l'induction.
